Hypocorticisme atypique chez le chien
Lorsqu’un chien est présenté pour des signes gastro-intestinaux, la maladie d’Addison n’est pas la première éventualité à envisager mais Romy Heilmann constate cependant qu’elle ne doit pas être écartée.
© Shutterstock

Points clés
En cas d’hypocorticisme typique, le tableau clinique et les résultats clinicopathologiques du chien sont généralement fortement évocateurs, ce qui simplifie le diagnostic.
L’hypocorticisme atypique est souvent associé à l’évolution irrégulière de signes gastro-intestinaux chroniques non spécifiques, pouvant être déclenchés ou exacerbés par le stress et qui répondent souvent à un traitement symptomatique.
Pour établir un diagnostic d’hypocorticisme atypique chez un chien, le vétérinaire doit adopter une approche d’enquêteur.
Les deux formes d’hypocorticisme sont généralement associées à un très bon pronostic à long terme.
Introduction
Dans sa forme typique (la maladie d’Addison), l’hypocorticisme est souvent simple à mettre en évidence car les signes cliniques et les anomalies clinicopathologiques sont caractéristiques et s’accordent bien avec l’historique et les commémoratifs du chien. Il peut donc sembler étrange qu’un gastroentérologue doive envisager cette affection quand il examine un animal. Pourtant, le tableau clinique des chiens affectés peut être peu spécifique (surtout s’ils présentent un hypocorticisme atypique spontané), et inclure des signes gastro-intestinaux chroniques évoluant de manière irrégulière. Ces signes peuvent être déclenchés ou exacerbés par des épisodes de stress, et répondent souvent à la fluidothérapie et au traitement symptomatique. L’hypocorticisme, en particulier dans sa forme atypique, peut donc être confondu avec une affection gastro-intestinale primaire et il ne doit pas être oublié dans la liste des diagnostics différentiels chez les chiens présentant des signes gastro-intestinaux vagues et non spécifiques.
Quelques rappels de base
Terminologie
L’hypocorticisme, ou maladie d’Addison, se développe lorsque le cortex surrénalien est incapable de produire et de sécréter des quantités suffisantes de glucocorticoïdes endogènes ; dans sa forme typique, une insuffisance de sécrétion en minéralocorticoïdes est également présente (Figure 1) [1]. Si l’hypocorticisme typique s’accompagne de critères cliniques et clinicopathologiques caractéristiques (liés à la carence simultanée en glucocorticoïdes et en minéralocorticoïdes), les cas d’hypocorticisme atypique sont en revanche plus difficiles à diagnostiquer chez le chien. Cette forme particulière d’insuffisance surrénalienne est non seulement moins fréquente mais son tableau clinique est également plus discret et moins spécifique [1],[2]. Un hypocorticisme atypique peut évoluer vers une forme typique, c’est pourquoi les cas atypiques doivent être régulièrement suivis [2]. Chez les chiens présentant une forme typique assez évoluée, la décompensation clinique peut provoquer une déshydratation et un choc hypovolémique (crise addisonienne). L’analyse rétrospective des cas de crises addisoniennes montre souvent une évolution initiale lente avec des signes cliniques non spécifique ayant conduit à une période d’errance. Chez ces cas, un déficit en glucocorticoïdes initial peut être suspecté mais cette évolution est difficile à prouver au moment de la découverte d’un cas typique d’hypocorticisme. Des prédispositions raciales sont signalées chez le Caniche standard, le Chien d’Eau Portugais, le Retriever de Nouvelle-Écosse, le Soft-Coated Wheaten Terrier et le Bearded Collie, mais des chiens de toute race et de tout âge peuvent être atteints par l’une ou l’autre forme de cette affection [2],[3],[4],[5]. Les chiens atteints d’hypocorticisme atypique ont tendance à être plus âgés que ceux présentant une forme typique.

Étiologie
Toute affection qui diminue la production et la libération d’hormones par le cortex surrénal peut entraîner un hypocorticisme. Le plus souvent, c’est un processus à médiation immunitaire qui est à l’origine de la destruction de la partie endocrine de la glande corticosurrénale, en particulier la partie médiane à interne qui produit des glucocorticoïdes (zona fasciculata) [5],[6],[7]. Les causes moins fréquentes voire rares d’hypocorticisme primaire sont les maladies granulomateuses (les maladies fongiques par exemple), les causes vasculaires (exemples : hémorragie, ischémie), les dépôts amyloïdes (en particulier dans les races prédisposées à développer une amyloïdose), la nécrose ou les tumeurs métastasées [8],[9],[10]. Un hypocorticisme secondaire (central) peut apparaître lorsque la production et la libération de l’hormone corticotrope (CRH) par l’hypothalamus ou de l’hormone adrénocorticotrope (ACTH) par l’hypophyse diminuent, notamment à cause d’un processus inflammatoire, infectieux, traumatique ou tumoral [1],[11].
Physiopathologie
Dans la forme typique de l’hypocorticisme, le déficit non compensé en glucocorticoïdes et en minéralocorticoïdes entraîne des anomalies caractéristiques des électrolytes plasmatiques (hyperkaliémie, hyponatrémie) [1]. Dans la forme atypique en revanche, on observe soit un déficit isolé en glucocorticoïdes, soit un déficit mixte en glucocorticoïdes et en minéralocorticoïdes mais sans évolution des concentrations en électrolytes, grâce à des mécanismes compensateurs indépendants de l’aldostérone (compensation rénale par exemple) [1],[2].
Détecter l’hypocorticisme : le grand prétendant
Signes cliniques
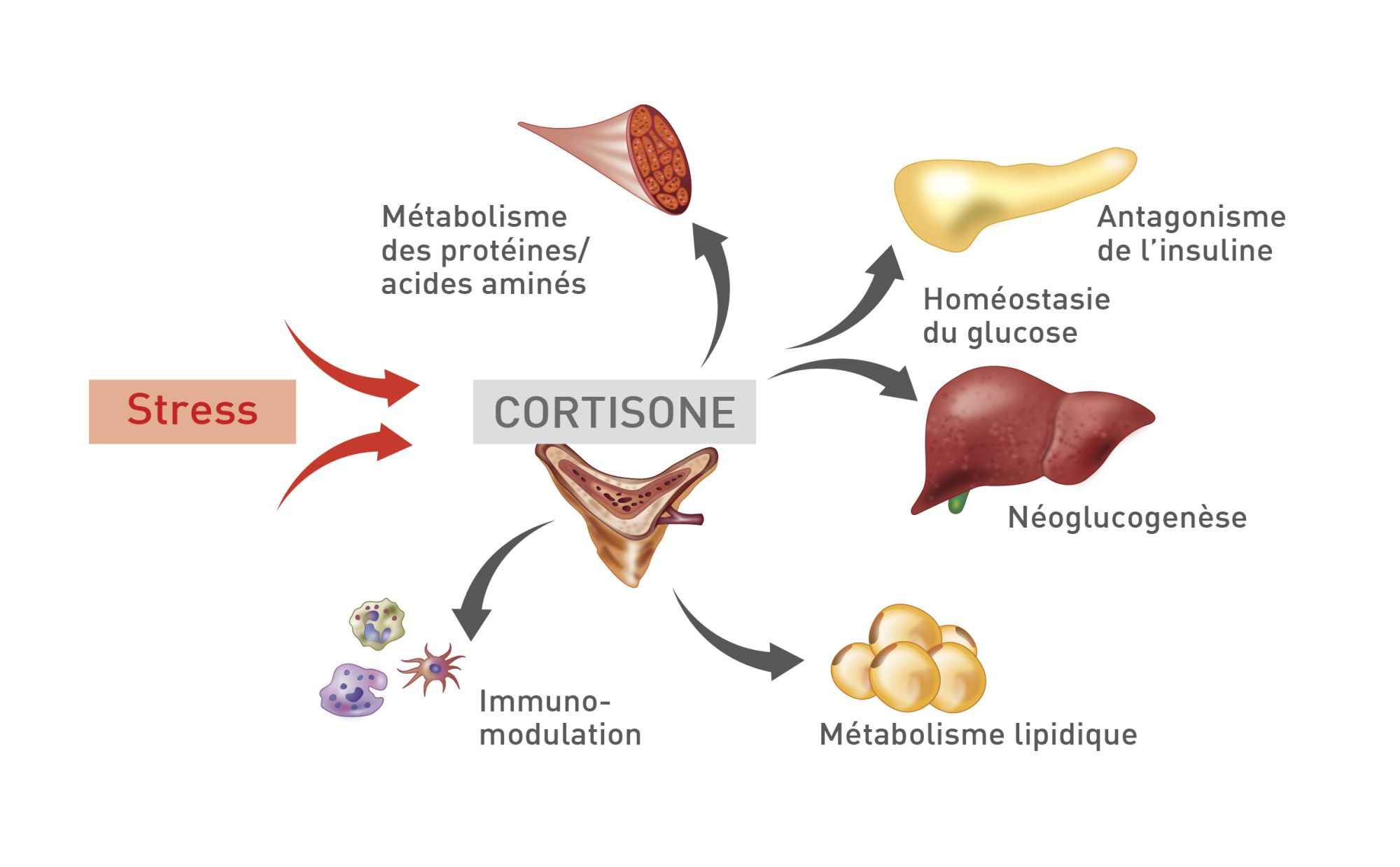
Compte tenu des rôles multiples que jouent les glucocorticoïdes endogènes dans l’organisme (Figure 2), y compris au niveau cardiaque et gastro-intestinal [12],[13], les chiens atteints d’hypocorticisme atypique présentent généralement des signes vagues et non spécifiques, qui évoluent par crises : baisse des performances (pendant les concours d’agility par exemple), léthargie, faiblesse, manque d’appétit, perte de poids voire émaciation (Figure 3), vomissements (avec ou sans hématémèse) ou régurgitations, diarrhée (pouvant être hémorragique), douleurs abdominales et incontinence [1],[2],[13],[14].

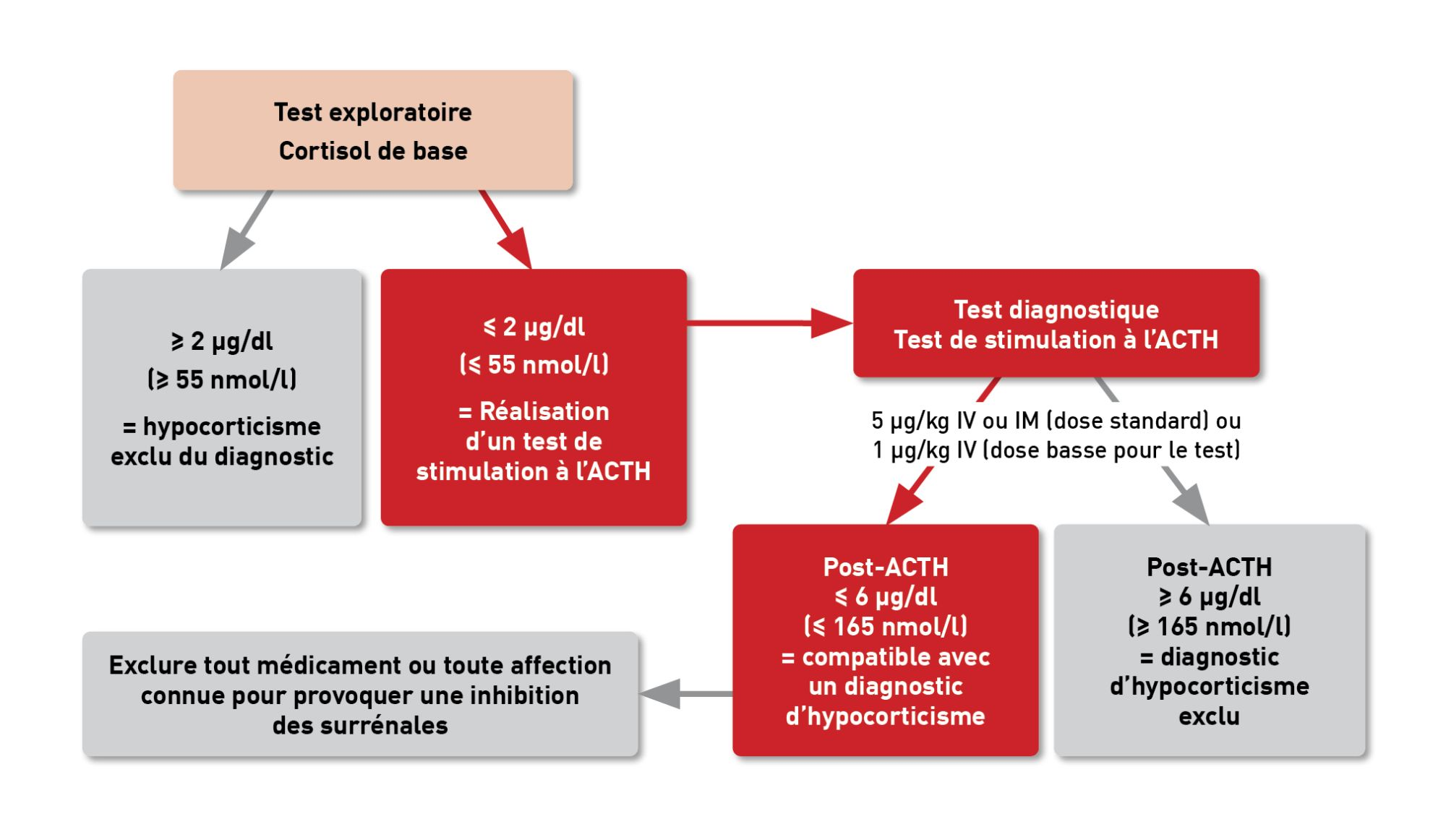
Le rapport cortisol/créatinine urinaire (RCCU) a récemment fait l’objet d’une attention particulière dans le cadre du diagnostic de l’hypocorticisme chez le chien. Un RCCU faible (≤ 2 lors du dosage radio-immunologique ou ≤ 10 avec un dosage immunologique en chimioluminescence) s’avère un critère très sensible et spécifique pour distinguer les chiens atteints de ceux présentant une maladie ressemblant à l’hypocorticisme [20].
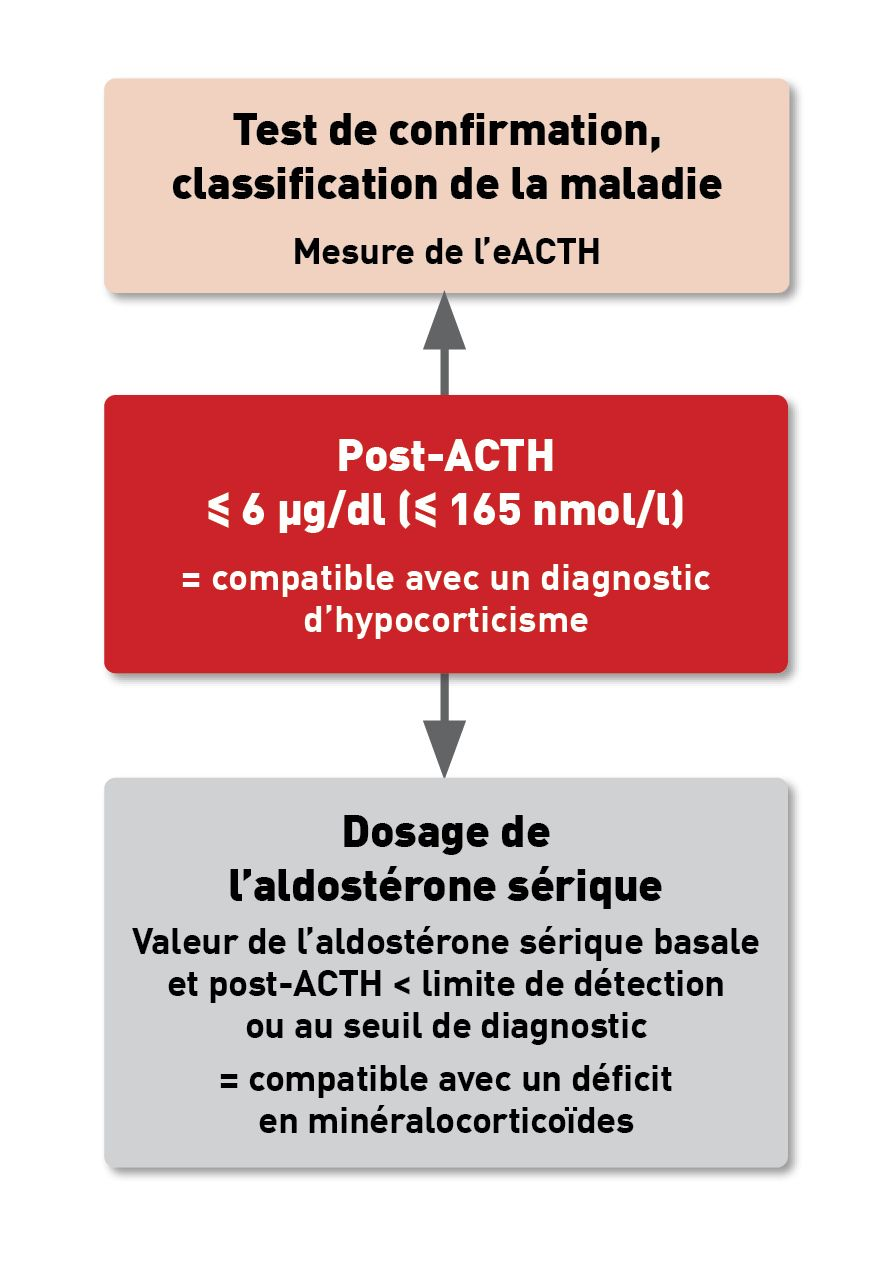
Le déficit en minéralocorticoïdes sans hyperkaliémie ou hyponatrémie, qui est théoriquement surtout compensé par des mécanismes rénaux, peut être détecté en mesurant l’aldostérone sérique avant et après stimulation par l’ACTH (Encadré 6). Ce test peut uniquement aider à distinguer les cas d’hypocorticisme atypique avec déficit en glucocorticoïdes des cas où il existe un déficit en minéralo- et glucocorticoïdes mais sans modifications électrolytiques [21]. Les dosages d’hormones thyroïdiennes des chiens atteints d’hypocorticisme peuvent révéler une augmentation du taux sérique de TSH et, dans certains cas, une diminution du taux de thyroxine (Encadré 3). Ces résultats ne sont pas le reflet d’une véritable hypothyroïdie car les taux se normalisent dans les semaines (jusqu’à 4 mois) qui suivent le début du traitement de l’hypocorticisme [22].
Encadré 6. Concentrations de cortisol et d’aldostérone sériques avant et après stimulation par l’ACTH chez le chien Boxer de la Figure 3. Ni la concentration sérique de cortisol ni celle d’aldostérone n’ont augmenté après la stimulation avec l’ACTH, ce qui confirme un déficit en glucocorticoïdes et en minéralocorticoïdes (compensé) chez ce chien.
| Paramètre | Résultat | Unité | Intervalle de référence |
|---|---|---|---|
| Test de stimulation à l’ACTH (cortisol sérique) | |||
| Cortisol (valeur basale) | < 2,8 | nmol/l | 25-125 |
| Cortisol (post-ACTH) |
< 2,8
|
nmol/l |
> 165
|
| Test de stimulation à l’ACTH (aldostérone sérique) | |||
| Aldostérone (valeur basale) | < 20 | pmol/l | 0-393 |
| Aldostérone (post-ACTH) | < 20 | pmol/l | 82-859 |
Imagerie diagnostique
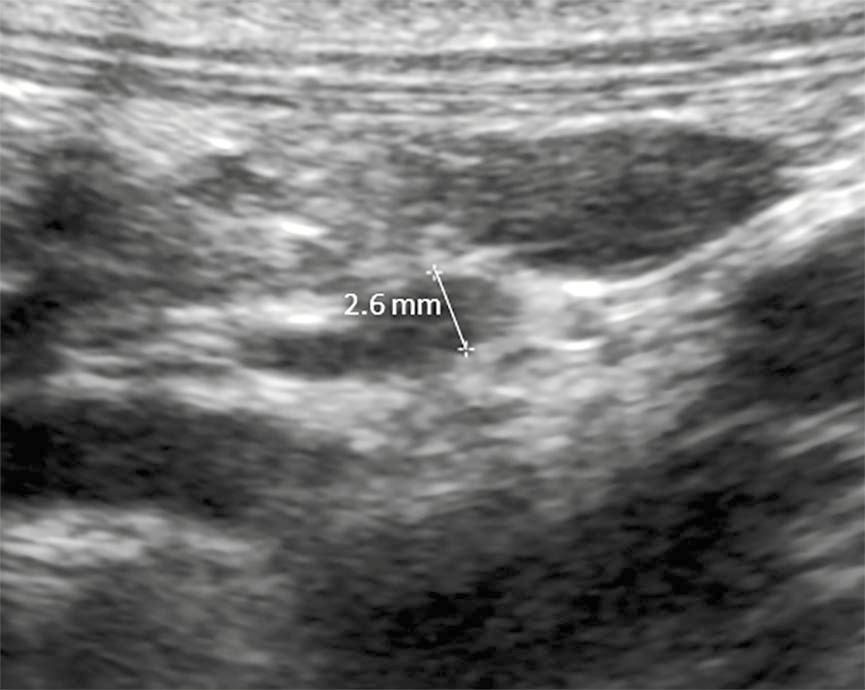
Les radiographies thoraciques et abdominales sont généralement sans intérêt chez les chiens atteints d’hypocorticisme, sauf pour évaluer la présence d’un mégaœsophage associé à l’hypocorticisme, mais elles peuvent servir à écarter d’autres hypothèses diagnostiques. L’échographie abdominale, incluant une évaluation approfondie des deux glandes surrénales, ne montre généralement rien de particulier mais un hypocorticisme peut être suspecté si le diamètre des glandes surrénales est faible (Figure 4). Dans les cas suspects, l’échographie est également recommandée pour diagnostiquer ou exclure une tumeur, une hémorragie ou un infarctus surrénaliens [1].
Traitement de l’hypocorticisme atypique
Initiation du traitement
Les chiens atteints d’hypocorticisme atypique sont généralement cliniquement stables et peuvent être traités en ambulatoire. Cependant, si une déshydratation est mise en évidence lors de l’examen clinique, une courte période d’hospitalisation sera justifiée pour administrer un soluté électrolytique équilibré. Un traitement symptomatique (des médicaments antiémétiques et gastroprotecteurs par exemple,) peut aussi être indiqué. L’hypoglycémie sera corrigée en administrant du glucose par voie IV (solution de dextrose) et la glycémie sera surveillée.
La prednisolone (ou prednisone) est le médicament de choix pour compenser le déficit en glucocorticoïdes endogènes [1],[2],[3]. Les glucocorticoïdes à action rapide (c’est-à-dire la dexaméthasone, l’hydrocortisone) sont plus couramment utilisés pour pallier la déficience aigüe en glucocorticoïdes chez les chiens présentant une crise addisonienne. La predniso(lo)ne est initialement administrée pendant quelques jours à une dose anti-inflammatoire faible (0,3-0,5 mg/kg PO q12-24h) [1],[2]. Après cette courte phase d’induction, la dose sera progressivement réduite jusqu’à atteindre le seuil (physiologique) le plus bas possible, qui compense encore efficacement la carence en glucocorticoïdes endogènes sans provoquer d’effets indésirables manifestes, et le traitement d’entretien sera poursuivi. Trouver la dose optimale pour un chien donné demande du temps (et de la patience de la part du propriétaire) mais, en fonction de la taille et de l’âge du chien, elle se situe généralement entre 0,05 et 0,2 mg/kg PO q24h (Encadré 7). Selon le caractère et le tempérament du chien, une augmentation à court terme de la dose d’entretien de predniso(lo)ne pourra être envisagée si une période de stress est à prévoir [1],[2].
Encadré 7. Recommandations pour adapter la dose de glucocorticoïdes à l’évolution des signes cliniques et à une suspicion de sous- ou de surdosage.
|
• Effets indésirables notables des glucocorticoïdes → réduction de la dose (d’environ 10 à 25 %) • Réapparition de signes cliniques (léthargie, anorexie, diarrhée) → augmentation de la dose (d’environ 50 %) |
|
• Stress important prévu (exemples : concours d’agility, feux d’artifice pendant les vacances, chirurgie planifiée)
→ envisager d’augmenter brièvement la dose (d’environ 100 à 200 %) chez certains chiens |
Un traitement de substitution des minéralocorticoïdes est indiqué dans les cas typiques d’hypocorticisme (c’est-à-dire chez les chiens présentant des modifications électrolytiques reflétant une carence concomitante en minéralocorticoïdes) mais chez les chiens présentant un hypocorticisme atypique, sa mise en œuvre dépend du statut minéralocorticoïde endogène. Si les concentrations sériques d’aldostérone sont faibles ou indétectables, les concentrations sériques en électrolytes seront étroitement surveillées. Une supplémentation en minéralocorticoïdes à faible dose (pivalate de désoxycorticostérone à la dose initiale de 1,5 mg/kg SC q25-28 j) [23] peut également être envisagée. En théorie, cela peut permettre d’alléger les mécanismes compensateurs mais un traitement substitutif à long terme avec des minéralocorticoïdes implique également une surveillance attentive du chien (électrolytes sériques, pression sanguine systémique) et peut comporter le risque d’effets indésirables [24]. Chez les chiens présentant un hypocorticisme atypique mais dont la concentration basale en aldostérone (ou la concentration sérique après stimulation à l’ACTH) est normale, seul un traitement de substitution avec des glucocorticoïdes est nécessaire, tout en surveillant régulièrement les concentrations en électrolytes sériques.
Surveillance du traitement
Les effets secondaires des glucocorticoïdes (exemples : polyurie-polydipsie, polyphagie, prise de poids, fonte musculaire, halètement, modifications de la peau et du pelage, troubles du comportement) peuvent apparaître même avec des doses très faibles de predniso(lo)ne et nécessitent de réduire la dose de 10 à 15 % environ (Encadré 7). La question de savoir si l’hydrocortisone est une bonne alternative pour compenser la carence en glucocorticoïdes chez certains chiens doit être étudiée plus avant. Chez les chiens traités pour un hypocorticisme, des signes de léthargie, de faiblesse, d’hyporexie ou d’anorexie, des vomissements et de la diarrhée peuvent indiquer que le traitement substitutif est insuffisant : la dose de glucocorticoïdes sera alors augmentée d’environ 50 % [1],[2],[3].
L’état des chiens atteints d’hypocorticisme atypique qui reçoivent un traitement substitutif à base de minéralocorticoïdes doit être initialement contrôlé toutes les 2 à 4 semaines (habituellement 10 à 14 jours puis 25 à 28 jours après le début de la supplémentation en pivalate de désoxycorticostérone) [23]. Si les concentrations sériques en électrolytes (sodium et potassium) se situent dans les fourchettes de référence, que la pression artérielle systémique est normale et que la dose de désoxycorticostérone n’a pas été récemment modifiée, la surveillance du traitement sera poursuivie tous les 1 à 3 mois (selon que le propriétaire peut ou non faire lui-même les injections de minéralocorticoïdes). Chez les chiens bien suivis, un contrôle sera effectué tous les 3 à 6 mois, sauf si l’injection mensuelle de désoxycorticostérone doit être effectuée à la clinique vétérinaire. Si une hypokaliémie, une hypernatrémie ou une hypertension systémique (pression artérielle systolique > 140 mmHg) sont détectées, la dose de pivalate de désoxycorticostérone sera diminuée de 10 à 20 % environ, ou le traitement sera arrêté temporairement [23]. Tout effet indésirable doit être attentivement évalué chez un chien présentant un hypocorticisme. La polyurie et la polydipsie sont généralement interprétées comme des effets secondaires de la (sur)supplémentation en predniso(lo)ne mais elles peuvent aussi refléter un surdosage en minéralocorticoïdes (c’est-à-dire en désoxycorticostérone) [1],[23].
Chez les chiens atteint d’hypocorticisme mais dont la concentration basale en aldostérone (ou la concentration sérique après stimulation à l’ACTH) est normale, seul un traitement de substitution avec des glucocorticoïdes est nécessaire, associé à la surveillance régulière des concentrations sériques en électrolytes.
Pronostic des cas d’hypocorticisme
Grâce à une supplémentation adéquate en glucocorticoïdes (et éventuellement en minéralocorticoïdes si cela s’impose), et un suivi du chien à intervalles réguliers, le pronostic à long terme de l’hypocorticisme atypique est généralement très bon (Figure 5) [1],[2],[25]. Lors du suivi à long terme des chiens atteints d’hypocorticisme atypique qui reçoivent seulement des glucocorticoïdes, il est indispensable de repérer une éventuelle évolution vers un hypocorticisme typique (c’est-à-dire le développement d’une hyperkaliémie ou d’une hyponatrémie) [2],[21]. Chez ces chiens, l’auteure recommande des doser les électrolytes sériques tous les 3 à 6 mois mais des recommandations concernant le rythme de surveillance des électrolytes sériques font actuellement défaut. Il en est de même pour déterminer le moment idéal pour initier la supplémentation en minéralocorticoïdes lors de déficit en aldostérone sans aucun changement électrolytique.

Conclusion
Quand l’état et la qualité de vie du chien s’améliorent rapidement en réponse au traitement, les propriétaires réalisent souvent rétrospectivement que les modifications cliniques liées à l’hypocorticisme de leur animal évoluaient lentement depuis longtemps. La maladie nécessite un traitement et une surveillance à vie mais cela renforce souvent le lien entre l’animal et l’Homme. Certains propriétaires craignent pourtant le développement d’une crise addisonienne et hésitent à laisser leur chien sans surveillance. La plupart des propriétaires sont cependant très à l’aise pour traiter à domicile un chien qui présente un hypocorticisme spontané : ils savent ou apprennent vite à repérer les changements de comportement de leur chien qui motivent une consultation vétérinaire.
| Nous remercions les Dr Juan Hernandez et Tristan Méric pour la relecture attentive de la version française de cet article. |
Romy M. Heilmann
DMV, DACVIM (SAIM), DECVIM-CA, MANZCVS (Médecine pour animaux de compagnie), PhD, Département des animaux de compagnie, Hôpital d’enseignement vétérinaire, collège de médecine vétérinaire, Université de Leipzig, Allemagne
La professeure Heilmann est spécialiste de médecine interne pour animaux de compagnie, diplômée de l’ACVIM et de l’ECVIM, et elle s’intéresse particulièrement à la gastro-entérologie, l’hépatologie, l’immunologie clinique, la radiologie interventionnelle et l’endoscopie. Après l’obtention de son doctorat vétérinaire en 2005, elle a travaillé en clientèle pour animaux de compagnie en Allemagne puis est retournée à l’université pour passer un doctorat de troisième cycle. Elle a ensuite effectué un internat en animaux de compagnie en Suisse avant de partir à l’Université A&M du Texas afin de suivre un programme combiné de spécialisation en médecine interne pour petits animaux (ACVIM-SAIM) et de doctorat. Elle est revenue en Europe en 2015, en tant que chef des internes dans une structure vétérinaire de référés en Suisse, avant d’accéder en 2016 à son poste actuel de professeure et de chef de service en médecine interne pour animaux de compagnie à l’Université de Leipzig. Ses recherches portent sur de nouvelles pistes pour diagnostiquer et traiter les gastro-entéropathies chroniques du chien et du chat, ainsi que d’autres troubles inflammatoires primaires.
Références
- Kalenyak K, Heilmann RM. Canine hypoadrenocorticism an update on pathogenesis, diagnosis and treatment. Tierarztl Prax. Ausg. K. Kleintiere Heimtiere 2018;46(3):163-175.
- Thompson AL, Scott-Moncrieff JC, Anderson JD. Comparison of classic hypoadrenocorticism with glucocorticoid-deficient hypoadrenocorticism in dogs: 46 cases (1985-2005). J. Am. Vet. Med. Assoc. 2007;230:1190-1194.
- Schofield I, Woolhead V, Johnson A, et al. Hypoadrenocorticism in dogs under UK primary veterinary care: frequency, clinical approaches and risk factors. J. Small Anim. Pract. 2021;62(5):343-350.
- Gershony LC, Belanger JM, Hytönen MK, et al. Genetic characterization of Addison’s disease in Bearded Collies. BMC Genomics 2020;21(1):833.
- Treeful AE, Rendahl AK, Friedenberg SG. DLA class II haplotypes show sex-specific associations with primary hypoadrenocorticism in Standard Poodle dogs. Immunogenetics 2019;71(5-6):373-382.
- Boag AM, Short A, Kennedy LJ, et al. Polymorphisms in the CTLA4 promotor sequence are associated with canine hypoadrenocorticism. Canine Med. Genet. 2020;7:2.
- Boag AM, Christie MR, McLaughlin KA, et al. Autoantibodies against cytochrome P450 side-chain cleavage enzyme in dogs (Canis lupus familiaris) affected with hypoadrenocorticism (Addison’s disease). PLoS One 2015;10(11):e0143458.
- Labelle P, DeCock HEV. Metastatic tumors to the adrenal glands in domestic animals. Vet. Pathol. 2005;42:52-58.s
- Buckley ME, Chapman PS, Walsh A. Glucocorticoid-deficient hypoadrenocorticism secondary to intravascular lymphoma in the adrenal glands of a dog. Aust. Vet. J. 2017;95(3):64-67.
- Lee N, Choi J, Yoon J. Presumptive nontraumatic adrenal hemorrhage preceding hypoadrenocorticism in a dog. J. Vet. Intern. Med. 2022;DOI: 10.1111/jvim.16531.
- Polledo L, Oliveira M, Adamany J, et al. Hypophysitis, panhypopituitarism, and hypothalamitis in a Scottish Terrier dog. J. Vet. Intern. Med. 2017;31(5):1527-1532.
- Gunasekaran T, Sanders RA. Ventricular systolic dysfunction in dogs diagnosed with hypoadrenocorticism. J. Vet. Cardiol. 2022;41:231-235.
- Hauck C, Schmitz SS, Burgener IA, et al. Prevalence and characterization of hypoadrenocorticism in dogs with signs of chronic gastrointestinal disease: a multicenter study. J. Vet. Intern. Med. 2020;34(4):1399-1405.
- Gallego AF, Gow AG, Boag AM. Evaluation of resting cortisol concentration testing in dogs with chronic gastrointestinal signs. J. Vet. Intern. Med. 2022;36(2):525-531.
- Zeugswetter FK, Schwendenwein I. Diagnostic efficacy of the leukogram and the chemiluminometric ACTH measurement to diagnose canine hypoadrenocorticism. Tierarztl. Prax. Ausg. K. Kleintiere Heimtiere 2014;42(2):223-230.
- Reagan KL, Reagan BA, Gilor C. Machine learning algorithm as a diagnostic tool for hypoadrenocorticism in dogs. Domest. Anim. Endocrinol. 2020;72:106396.
- Lennon EM, Boyle TE, Hutchins RG, et al. Use of basal serum or plasma cortisol concentrations to rule out a diagnosis of hypoadrenocorticism in dogs: 123 cases (2000-2005). J. Am. Vet. Med. Assoc. 2007;231(3):413-416.
- Bovens C, Tennant K, Reeve J, et al. Basal serum cortisol concentration as a screening test for hypoadrenocorticism in dogs. J. Vet. Intern. Med. 2014;28(5):1541-1545.
- Botsford A, Behrend EN, Kemppainen RJ, et al. Low-dose ACTH stimulation testing in dogs suspected of hypoadrenocorticism. J. Vet. Intern. Med. 2018;32(6):1886-1890.
- Moya MV, Refsal KR, Langlois DK. Investigation of the urine cortisol to creatinine ratio for the diagnosis of hypoadrenocorticism in dogs. J. Am. Vet. Med. Assoc. 2022;260(9):1041-1047.
- Baumstark ME, Sieber-Ruckstuhl NS, Müller C, et al. Evaluation of aldosterone concentrations in dogs with hypoadrenocorticism. J. Vet. Intern. Med. 2014;28(1):154-159.
- Reusch CE, Fracassi F, Sieber-Ruckstuhl NS, et al. Altered serum thyrotropin concentrations in dogs with primary hypoadrenocorticism before and during treatment. J. Vet. Intern. Med. 2017;31(6):1643-1648.
- Sieber-Ruckstuhl NS, Reusch CE, Hofer-Inteeworn N, et al. Evaluation of a low-dose desoxycorticosterone pivalate treatment protocol for long-term management of dogs with primary hypoadrenocorticism. J. Vet. Intern. Med. 2019;33(3):1266-1271.
- Casado Diaz JI, Sieber-Ruckstuhl NS, Boretti FS, et al. Evaluation of symmetric dimethylarginine and creatinine in dogs with primary hypoadrenocorticism receiving long-term mineralocorticoid replacement therapy. Vet. Rec. 2022;190(1):e242.
- Hupfeld J, Dölle M, Volk H, et al. Effect of long-term management of hypoadrenocorticism on the quality of life of affected dogs and their owners. Vet. Rec. 2022;8:e1977.
Autres articles de ce numéro
Partager sur les réseaux sociaux