Comment je traite… Le chylothorax félin
Ecrit par Elizabeth Rozanski
Le chylothorax est à inclure dans le diagnostic différentiel chez tout chat présentant un épanchement pleural. Elizabeth Rozanski décrit ici l’approche qu’elle privilégie dans de tels cas.
Article
Introduction
Le chylothorax se développe lorsque du chyle s’accumule dans le thorax [1],[2],[3],[4]. Le chyle est un liquide riche en lymphocytes qui s’écoule avec les chylomicrons après la digestion intestinale. Le chyle passe généralement dans la circulation sanguine, ce qui favorise la santé du système immunitaire et prévient la malnutrition, mais si le drainage normal du canal thoracique est altéré, un épanchement chyleux se développe. Les chats présentant un chylothorax sont plutôt d’âge moyen, et le premier signe clinique est généralement une tachypnée ou une respiration difficile.
Le chylothorax peut être une maladie extrêmement frustrante à la fois pour les propriétaires et les cliniciens et, comme cette affection est assez rare, les études sont peu nombreuses. Il est donc difficile d’évaluer avec précision la meilleure approche thérapeutique, et les propriétaires de chats atteints de chylothorax doivent être informés dès le départ que cette maladie peut être très difficile à traiter.
Anatomie et physiologie
Afin de mieux comprendre le chylothorax et les raisons de son développement, il est utile de revoir ses bases anatomiques et physiologiques. En résumé, les lipides (chylomicrons) et les protéines plasmatiques passent de l’intestin aux canaux lymphatiques [1],[5]. Ces canaux se rejoignent au niveau de la citerne du chyle et sont rejoints par des canaux lymphatiques provenant de la cavité abdominale et des membres pelviens ; ils forment ensuite le canal thoracique qui traverse le diaphragme pour rejoindre le système circulatoire à la jonction entre la veine jugulaire caudale et la veine cave crâniale. Cette jonction est dotée d’une valve à sens unique, de sorte que le chyle peut rejoindre la circulation veineuse, mais le sang ne peut pas circuler dans le sens rétrograde. Pour qu’un épanchement chyleux apparaisse, il faut une obstruction au drainage, un traumatisme du canal thoracique, ou une malformation/dilatation des canaux lymphatiques (lymphangiectasie) [1],[2],[3],[4].
Diagnostic
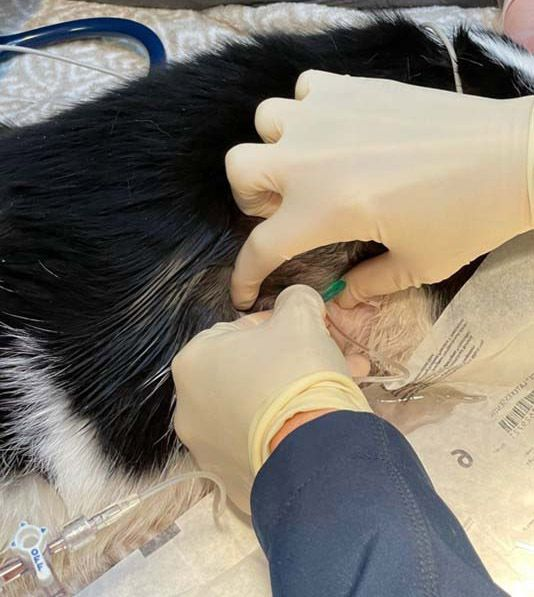
Lorsqu’un épanchement pleural est identifié, que ce soit à la suite d’un examen clinique, d’une radiographie ou d’une échographie, une thoracocentèse doit être réalisée afin d’éliminer le plus de liquide possible ; cette intervention est à la fois diagnostique et thérapeutique (Figure 1). Lors de la thoracocentèse, un échantillon de liquide sera conservé à des fins d’analyse si la cause sous-jacente n’est pas connue, si le liquide a changé d’aspect par rapport aux prélèvements précédents, ou si le statut clinique du chat a évolué.
Le diagnostic de chylothorax repose sur l’analyse du liquide : l’épanchement pleural contient de petits lymphocytes et nettement plus de triglycérides que de cholestérol [1]. Le plus souvent, l’épanchement a un aspect laiteux (Figure 2) mais, en cas d’anorexie prolongée, il peut être clair ou seulement légèrement trouble. Un autre type de liquide, appelé épanchement pseudo-chyleux, est rarement observé. Il s’agit d’un liquide qui semble trouble mais qui présente un faible taux de triglycérides mais souvent un taux élevé de cholestérol. Lorsqu’un épanchement chyleux est observé, il faut rechercher la cause sous-jacente ; la plupart des cas sont probablement idiopathiques, mais une cause spécifique peut être découverte dans certains cas et permet alors de traiter de manière ciblée [1].

Le chylothorax peut être une maladie extrêmement frustrante pour les propriétaires et les cliniciens et, comme cette affection est assez rare, les études sont peu nombreuses. Il est donc difficile d’évaluer avec précision la meilleure approche thérapeutique, et les propriétaires de chats atteints de chylothorax doivent être informés dès le départ que cette maladie peut être très difficile à traiter.
Approche clinique
Après identification du chylothorax, et si le propriétaire accepte de poursuivre le traitement, les examens suivants seront envisagés et proposés si nécessaire.
Commémoratifs et examen clinique
Bien que le traumatisme ait historiquement été considéré comme une cause potentielle de chylothorax, les données actuelles suggèrent qu’une lésion du canal thoracique (par exemple, si un traumatisme est survenu accidentellement pendant une intervention chirurgicale) guérit habituellement en une à deux semaines. L’éventualité d’un événement traumatique (par exemple, une chute ou un accident sur la voie publique) peut cependant avoir de l’importance, et toute intervention chirurgicale thoracique récente doit clairement être considérée comme un facteur de risque [6]. Il faut aussi savoir si l’animal a des antécédents de troubles cardiaques, quel est son statut vis-à-vis de la leucose féline, et s’il vit dans une région où la dirofilariose cardiaque est endémique. À l’examen, il convient d’être particulièrement attentif aux signes suivants : souffle cardiaque, rythme de galop, hypertrophie de la thyroïde, diminution de la compliance thoracique (par exemple, si une masse médiastinale est suspectée), fonte musculaire, ascite ou autres signes de maladie chronique. Un épanchement chyleux qui dure depuis longtemps (> 3 mois) peut entraîner une malnutrition, notamment une carence en vitamines liposolubles [7]. La pose d’un pacemaker transveineux chez le chat a toujours été associée à un chylothorax, c’est pourquoi ces pacemakers ne sont désormais que rarement (voire plus du tout) utilisés dans cette espèce. Chez le chien, les cathéters de dialyse, les pacemakers transveineux ou les cathéters centraux de longue durée ont également été associés au développement d’un épanchement chyleux, à cause d’une thrombose ou d’une obstruction de la veine cave crâniale.
Radiographies thoraciques
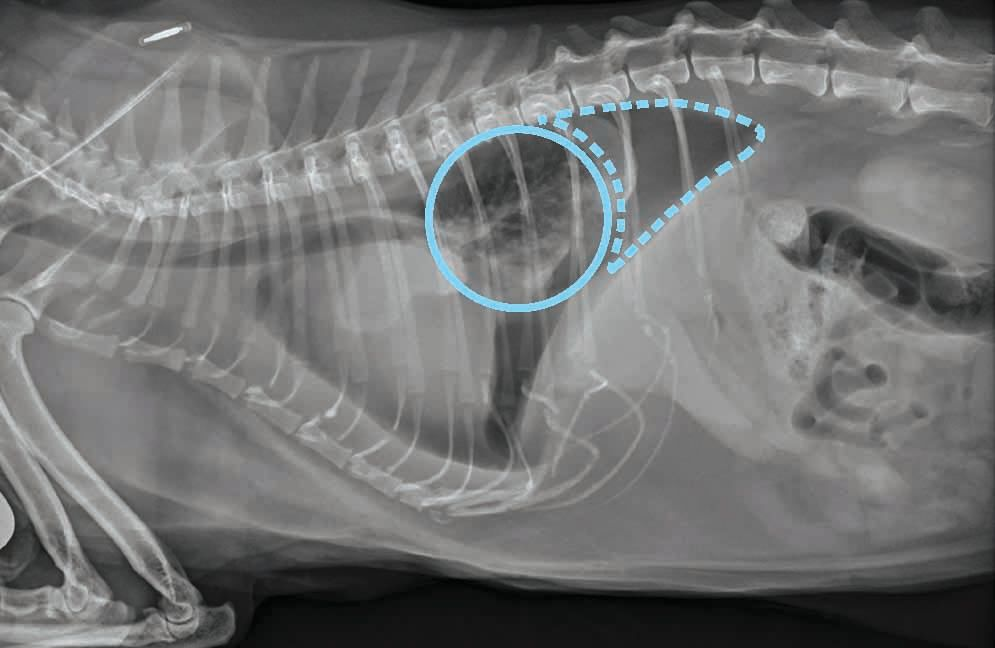
Après identification et retrait d’un épanchement pleural, les radiographies permettent d’évaluer s’il existe ou non une pleurite restrictive, et de rechercher la présence d’une cardiomégalie ou de masses intrathoraciques. Les radiographies réalisées avant le retrait de l’épanchement pleural sont rarement utiles pour déterminer l’étiologie. Un épanchement pleural restrictif peut être suspecté lorsque les champs pulmonaires apparaissent arrondis à la radiographie (Figure 3) ; s’il est présent, il est important de l’identifier, car les chats affectés risquent particulièrement de développer un pneumothorax post-thoracocentèse. Deux hypothèses peuvent l’expliquer :
- Risque de lacération directe d’un lobe pulmonaire pendant la thoracocentèse. Les tissus pulmonaires normaux et sains guérissent rapidement après une petite lacération ou une blessure par piqûre d’aiguille ; en revanche, si les poumons ont été entourés de chyle, la plèvre sera fibrotique et épaissie, elle cicatrisera lentement, permettant à l’air de s’échapper du site de thoracocentèse dans l’espace pleural.
- Présence de lobes pulmonaires « piégés ». Il s’agit essentiellement de petits poumons fibrotiques qui sont peu élastiques, de sorte que l’aspiration d’un grand volume d’épanchement pleural peut faire nettement baisser la pression intrathoracique, ce qui peut entraîner la déchirure d’un lobe pulmonaire pour remplir l’espace [8].
Échocardiographie
L’échocardiographie est extrêmement utile pour identifier et confirmer qu’une maladie cardiaque est une cause sous-jacente d’épanchement chyleux. L’insuffisance cardiaque droite ou biventriculaire a été associée au développement d’un épanchement chyleux, en raison de l’augmentation de la pression veineuse qui empêche le canal thoracique de se drainer dans la circulation veineuse [4]. Le traitement de la maladie cardiaque sous-jacente permettra de réduire l’épanchement chyleux. L’échocardiographie peut également faciliter la mise en évidence d’une dirofilariose cardiaque, ainsi que d’une masse ou d’un thrombus dans la veine cave crâniale. Le cas d’un chat présentant une endocardite aortique associée à un épanchement chyleux, identifiés par échocardiographie, a ainsi été rapporté [9].
Examens de laboratoire
Une analyse du liquide est nécessaire pour diagnostiquer un chylothorax mais, comme chez tout chat malade, des examens de routine sont également indiqués, notamment une numération globulaire complète, un profil biochimique et une analyse d’urine. Les tests antigéniques et la recherche d’anticorps contre les filaires cardiaques, ainsi que l’exploration du statut vis-à-vis des rétrovirus (FeLV et FIV) doivent également être envisagés ; chez les chats de plus de 5 ans, une exploration thyroïdienne est recommandée [10]. Lorsque l’échocardiographie n’est pas disponible, un test NT-proBNP (pouvant être effectué sur l’épanchement pleural) peut aider à dépister une maladie cardiaque.
Imagerie avancée
Après une thoracocentèse, les radiographies thoraciques sont utiles pour documenter tout signe de pleurite restrictive et pour mettre en évidence une tumeur ; si l’on suspecte une masse médiastinale, une échographie thoracique sera également pratiquée [11]. Cependant, le scanner, idéalement accompagné d’une lymphangiographie, est considéré comme la meilleure technique d’imagerie pour mettre en évidence des anomalies des canaux thoraciques (lymphangiectasie) ou des masses (Figure 4). Le scanner et la lymphangiographie seront réalisés après injection d’un produit de contraste dans le coussinet métatarsien [12]. Des thrombi ou des masses dans la veine cave crâniale peuvent également être vus au scanner.


Figure 4. Deux images au scanner d’un chat avec un épanchement chyleux qui a évolué vers une pleurite restrictive sur une période d’environ deux ans. Noter l’épaississement de la plèvre et l’aspect arrondi des poumons sur la dernière image.
© Elizabeth Rozanski
Traitement du chylothorax
Traitement chirurgical
Dans les cas de chylothorax sans cause sous-jacente apparente, la ligature du canal thoracique (LCT), seule ou associée à d’autres procédures, est couramment recommandée [1],[2],[13],[14]. L’objectif d’une LCT est d’empêcher le chyle de pénétrer dans le thorax. Des anastomoses lymphatico-veineuses se forment ensuite dans l’abdomen, permettant au chyle de réintégrer la circulation par cette voie [14]. Une LCT est évidemment dangereuse en cas d’épanchement chyleux abdominal concomitant, et l’intervention nécessite d’être attentif à tous les détails. Contrairement à de nombreuses procédures chirurgicales, le taux de réussite est faible : il oscille entre 50 et 75 %, les pourcentages les plus élevés n’étant obtenus que par les chirurgiens les plus méticuleux et les plus expérimentés. Généralement, une thoracotomie latérale est effectuée, bien que l’approche thoracoscopique puisse être occasionnellement préférée pour améliorer la visualisation souvent réduite à cause de la petite taille du chat [15]. Normalement, il n’existe qu’un grand canal, mais il n’est pas rare de voir plusieurs petits canaux qui se sont développés ou étendus après la ligature du premier. Ces canaux supplémentaires peuvent expliquer le taux d’échec chirurgical élevé. La visualisation des canaux sera améliorée en administrant un repas riche en matières grasses (par exemple, de la crème ou un aliment pour chaton) 2 à 3 heures avant l’opération, ou en utilisant un nouveau colorant au bleu de méthylène. Des lymphangiographies peropératoires peuvent également permettre d’évaluer les résultats en temps réel.
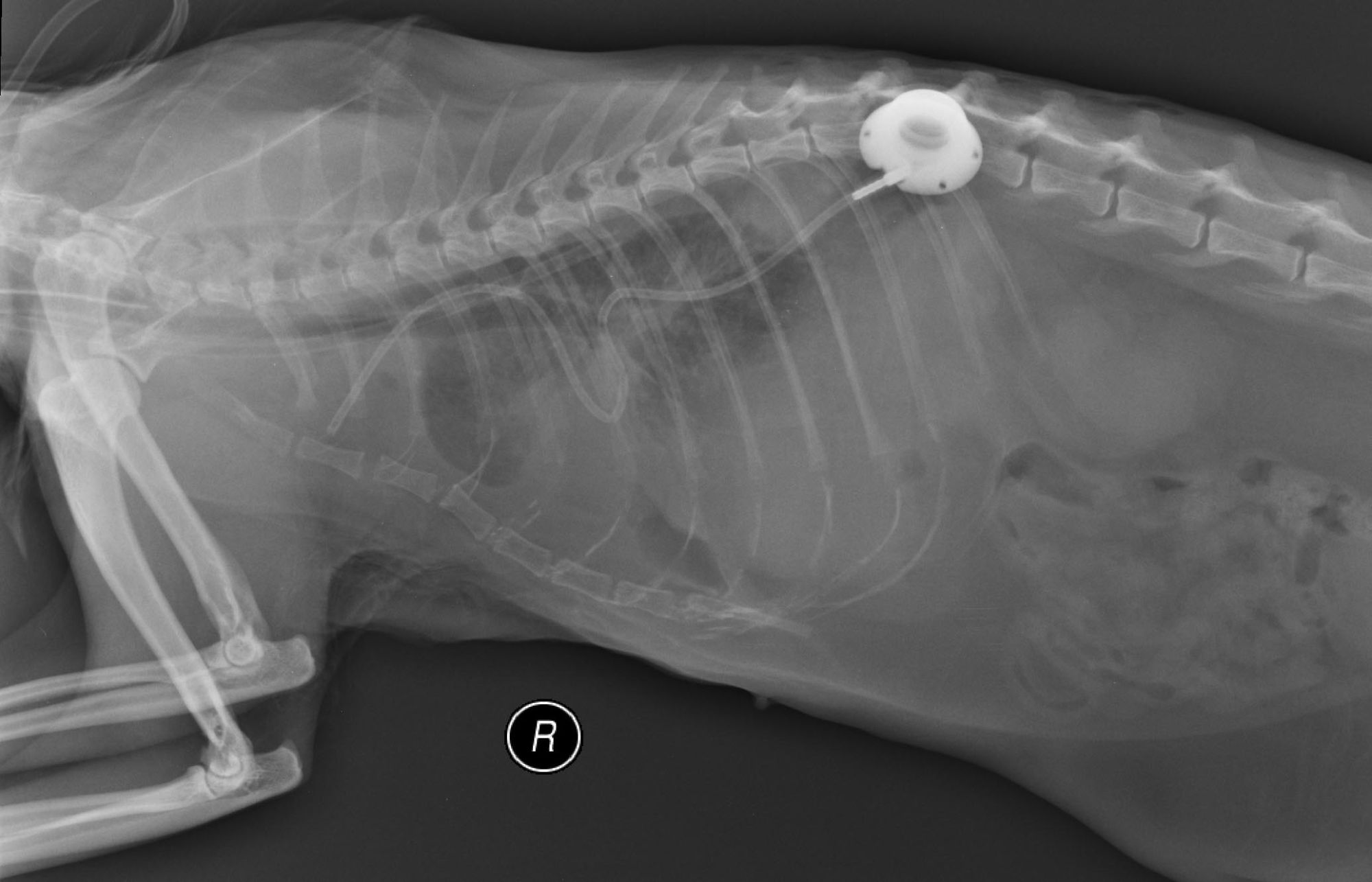
La LCT est généralement associée à une péricardiectomie sous-phrénique ; une petite étude chez le chat n’a pas montré d’intérêt à faire également l’ablation de la citerne de chyle [2]. Un port pleural est généralement placé au moment de l’opération, qui peut aider au drainage thoracique à domicile si le propriétaire et le chat le tolèrent (Figure 5). Les orifices peuvent cependant se boucher ou devenir non fonctionnels, et un pyothorax est également possible si l’asepsie n’est pas respectée.
Chez le chien, une thérapie interventionnelle par collage du canal thoracique a été décrite ; le but de cette procédure est d’occlure efficacement toutes les branches du canal [16]. À la connaissance de l’auteure, cela n’a pas été tenté chez le chat mais mériterait sans doute d’être exploré.


Figure 5. Un port pleural, comme on le voit sur ces radiographies post-chirurgicales, peut être placé pour permettre une thoracocentèse à domicile, ou pour réduire le risque de traumatisme lié au fait de devoir insérer régulièrement une aiguille pour drainer un épanchement récidivant.
© Elizabeth Rozanski
Traitement médical
Le traitement médical n’est indiqué que si une maladie sous-jacente, telle une insuffisance cardiaque congestive (ICC), est détectée. Des publications anciennes évoquaient l’intérêt potentiel d’un nutraceutique, la rutine, mais rien ne prouve actuellement qu’elle soit utile. De même, les triglycérides à chaîne moyenne (TCM) étaient auparavant préconisés, car on pensait que les TCM étaient absorbés dans les canaux lymphatiques. Cette approche ne s’est pas révélée bénéfique non plus et n’est plus d’actualité. Un régime pauvre en matières grasses peut être envisagé s’il est toléré, mais les preuves de son utilité font défaut.
En médecine humaine, le traitement non chirurgical du chylothorax s’est appuyé sur l’octréotide, avec un succès modéré chez les nourrissons [17]. Théoriquement, l’octréotide diminuerait les sécrétions dans le tube digestif, mais son mécanisme d’action exact est inconnu. Ce médicament n’a pas été formellement évalué chez le chat à chylothorax, mais une publication datant d’une vingtaine d’années mentionne un certain succès chez un petit groupe de chats [18].
Complications du chylothorax
La présence de chyle est très irritante pour les surfaces pleurales et, comme indiqué ci-dessus, une épaisse couche de tissu cicatriciel fibrotique peut se former à la surface de la plèvre viscérale. Cette évolution est particulièrement inquiétante car elle est associée au développement de deux complications potentielles : la pleurite restrictive et le pneumothorax iatrogène consécutif à la thoracocentèse. La pleurite restrictive est généralement associée à un épanchement chronique ; elle se traduit par une petite taille des poumons et une perturbation des échanges gazeux. Une pleurite restrictive sévère était historiquement considérée comme mortelle, mais un cas publié récemment a décrit la réussite du traitement chirurgical [19]. Les autres complications du chylothorax incluent la malnutrition et la perte de vitamines liposolubles (comme la vitamine K), associée à la perte de chyle ; si des thoracocentèses doivent être effectuées souvent (soit toutes les semaines ou toutes les 2 semaines), une supplémentation en vitamines liposolubles peut donc être envisagée. Un risque d’immunodéficience existe aussi lorsque la thoracocentèse a entraîné la perte récurrente d’un grand volume de chyle [7]. L’absence de résolution de l’épanchement constitue cependant le problème le plus courant et implique des visites vétérinaires régulières, qui peuvent être coûteuses pour le propriétaire et stressantes pour le chat.
Conclusion
Le chylothorax est une affection frustrante pour le clinicien mais, en respectant scrupuleusement la démarche diagnostique et en choisissant la bonne stratégie de traitement, les efforts peuvent être récompensés. Cependant, des essais cliniques sont absolument nécessaires pour obtenir des données probantes à propos des options chirurgicales et non chirurgicales pour traiter un épanchement idiopathique. Lorsqu’un épanchement chyleux est identifié chez un chat, la thoracocentèse devra rapidement être suivie de l’exploration des causes sous-jacentes et d’une intervention chirurgicale précoce pour que le pronostic soit le meilleur possible.
Elizabeth Rozanski
Dr vétérinaire, Dip. ACVIM (SAIM), Dip. ACVECCÉtats-Unis
Diplômée de l’Université de l’Illinois depuis 1992, la Dre Rozanski a effectué un internat à l’Université du Minnesota avant de faire son résidanat à l’Université de Pennsylvanie. Depuis 1996, elle enseigne au sein de l’Université Tufts, où elle travaille au service des urgences et soins intensifs. Spécialiste en médecine interne et en soins intensifs, la Dre Rozanski s’intéresse aux maladies respiratoires, en particulier à l’asthme félin et canin, et à la fibrose pulmonaire chez le West Highland White Terrier. Auteure de nombreux articles sur les soins intensifs et les maladies respiratoires, elle donne également des conférences au niveau national et international.
Références
- Reeves LA, Anderson KM, Luther JK, et al. Treatment of idiopathic chylothorax in dogs and cats: a systematic review. Vet. Surg. 2020;49(1):70-79.
- Stockdale SL, Gazzola KM, Strouse JB, et al. Comparison of thoracic duct ligation plus subphrenic pericardiectomy with or without cisterna chyli ablation for treatment of idiopathic chylothorax in cats. J. Am. Vet. Med. Assoc. 2018;252(8):976-981.
- Fossum TW, Evering WN, Miller MW, et al. Severe bilateral fibrosing pleuritis associated with chronic chylothorax in five cats and two dogs. J. Am. Vet. Med. Assoc. 1992;201(2):317-324.
- Fossum TW, Miller MW, Rogers KS, et al. Chylothorax associated with right-sided heart failure in five cats. J. Am. Vet. Med. Assoc. 1994;204(1):84-89.
- Alexander JS, Ganta VC, Jordan PA, et al. Gastrointestinal lymphatics in health and disease. Pathophysiology 2010;17(4):315-335.
- Greenberg MJ, Weisse CW. Spontaneous resolution of iatrogenic chylothorax in a cat. J. Am. Vet. Med. Assoc. 2005;226(10):1667-1670, 1659.
- Hoskote AU, Ramaiah RN, Cale CM, et al. Role of immunoglobulin supplementation for secondary immunodeficiency associated with chylothorax after pediatric cardiothoracic surgery. Pediatr. Crit. Care Med. 2012;13(5):535-541.
- Khan H, Fernandez-Perez ER, Caples SM. Post-thoracentesis trapped lung. J. Postgrad. Med. 2007;53(2):119-120.
- Dixon-Jimenez A, Margiocco ML. Infectious endocarditis and chylothorax in a cat. J. Am. Anim. Hosp. Assoc. 2011;47(6):e121-126.
- Hayes G. Chylothorax and fibrosing pleuritis secondary to thyrotoxic cardiomyopathy. J. Small Anim. Pract. 2005;46(4):203-205.
- Meadows RL, MacWilliams PS, Dzata G, et al. Chylothorax associated with cryptococcal mediastinal granuloma in a cat. Vet. Clin. Pathol. 1993;22(4):109-116.
- Chiang C, Chen KS, Chiu HC, et al. Computed tomography lymphangiography via intrametatarsal pad injection is feasible in cats with chylothorax. Am. J. Vet. Res. 2022;1:1-7.
- Lafond E, Weirich WE, Salisbury SK. Omentalization of the thorax for treatment of idiopathic chylothorax with constrictive pleuritis in a cat. J. Am. Anim. Hosp. Assoc. 2002;38(1):74-78.
- Dickerson VM, Grimes JA, Secrest SA, et al. Abdominal lymphatic drainage after thoracic duct ligation and cisterna chyli ablation in clinically normal cats. Am. J. Vet. Res. 2019;80(9):885-890.
- Radlinsky M. Thoracoscopy in the cat: an up-and-coming diagnostic and therapeutic procedure. J. Feline Med. Surg. 2014;16(1):27-33.
- Clendaniel DC, Weisse C, Culp WT, et al. Salvage cisterna chyli and thoracic duct glue embolization in 2 dogs with recurrent idiopathic chylothorax. J. Vet. Intern. Med. 2014;28(2):672-677.
- Bellini C, Cabano R, de Angelis LC, et al. Octreotide for congenital and acquired chylothorax in newborns: a systematic review. J. Paediatr. Child Health. 2018;54(8):840-847.
- Hardie RJ, Hayashi K, DaCosta Gomez T, et al. The use of the somastostating analogue (octreotide) for the treatment of idiopathic chylothorax in dogs and cats. In; Proceedings, 13th:sup Annual ACVS Symposium, Washington DC, 2003.
- Sack D, Hyndman P, Milligan M, et al. Decortication, thoracic omentalization, and pericardiectomy for treatment of severe fibrosing pleuritis in a cat. J. Am. Vet. Med. Assoc. 2022;1:1-6.
Autres articles de ce numéro
Partager sur les réseaux sociaux