กลูเตนในสุขภาพของมนุษย์และสุนัข
เขียนโดย Chih-Fan Chiang
อาหารที่ปราศจากกลูเตนกำลังได้รับความนิยมทั้งในมนุษย์และสุนัข แต่จริงๆ แล้วโรคที่เกี่ยวข้องกับกลูเตน (gluten-related disorders) นั้นสามารถเกิดขึ้นได้บ่อยแค่ไหน? บทความนี้จะเปรียบเทียบและแสดงให้เห็นถึงความแตกต่างของโรคเหล่านี้ในทั้งสองสปีชีส์
ประเด็นสำคัญ
Article

ประเด็นสำคัญ
กลูเตนเป็นคำที่ใช้เรียกโปรตีนบางชนิดที่พบในธัญพืช ซึ่งช่วยให้ขนมอบมีลักษณะ “เคี้ยวหนึบ (chewy)” เมื่อรับประทาน
อาหารที่ปราศจากกลูเตนอาจเหมาะสมสำหรับโรคในสุนัขบางโรค โดยเฉพาะอย่างยิ่งโรคระบบทางเดินอาหาร (enteropathies) ในสุนัขพันธุ์ไอริชเซ็ตเตอร์ (Irish Setters) และความผิดปกติของการเคลื่อนไหวที่ไม่สามารถควบคุมได้ซึ่งเกิดเป็นพักๆ (paroxysmal dyskinesia) ในสุนัขพันธุ์บอร์เดอร์เทอเรีย (Border Terriers)
อาหารสูตรรักษาโรค (therapeutic diet) ในสัตว์เลี้ยงที่ประกอบด้วยส่วนผสมที่ปราศจากกลูเตน (gluten-free ingredients) ในปริมาณจำกัดนั้นสามารถพิจารณาเพื่อใช้ในการลองควบคุมอาหาร (elimination diet trial) ในกรณีที่สงสัยว่าเกี่ยวข้องกับกลูเตนได้
อาหารที่ปราศจากกลูเตนยังเหมาะสมสำหรับสุนัขสุขภาพดีที่อาศัยอยู่กับคนที่เป็นโรคที่เกี่ยวข้องกับกลูเตน (gluten-related disorder) อีกด้วย
บทนำ
กลูเตนเป็นคำที่ใช้เรียกโปรตีนจากพืช (plant proteins) ที่พบในเอนโดสเปิร์ม (endosperm) ของธัญพืช (cereal grains) ซึ่งมีบทบาทในการสนับสนุนความต้องการทางโภชนาการสำหรับการงอกและการเจริญเติบโตของเมล็ดพืช นักวิทยาศาสตร์ได้ให้ความสนใจกับกลูเตนมาอย่างยาวนาน โดยมีการวิเคราะห์ที่ช่วยให้สามารถจำแนกองค์ประกอบของกลูเตนและจำแนกโปรตีนจากธัญพืชต่างๆได้เป็น 4 กลุ่ม ได้แก่ อัลบูมิน (albumin), โกลบูลิน (globulin), โพรลามิน (prolamin) และกลูเตลิน (glutelin) 1. อัลบูมินและโกลบูลินนั้นสามารถละลายน้ำได้ (water-soluble) ขณะที่โพรลามินสามารถสร้างได้จากกระบวนการผลิตแอลกอฮอล์ (alcohol process) และกลูเตลินสามารถสกัดได้ด้วยตัวทำละลายด่าง (alkaline solvent) ทั้งนี้โพรลามินได้ชื่อมาจากการที่มันมีโพรลีน (proline) และ กลูตามีน (glutamine) ในปริมาณสูง และยังเป็นที่รู้จักกันในชื่อ เกลียดิน (gliadin) ฮอร์ดีอิน (hordein) ซีคาลิน (secalin) อเวนิน (avenin) และซีอิน (zein) ในเมล็ดธัญพืช (grains) ที่ได้จากข้าวสาลี ข้าวบาร์เลย์ ข้าวไรย์ ข้าวโอ๊ต และข้าวโพดตามลำดับ กลูเตลินเป็นโปรตีนที่รวมถึงเอนไซม์และผนังเซลล์ (cell walls) นอกจากนี้ยังรู้จักกันในชื่อ กลูเตนิน (glutenin) ในธัญพืชที่ได้จากข้าวสาลี นักเขียนบางคนแนะนำว่า คำว่า "กลูเตน" ควรใช้เฉพาะสำหรับเกลียดินและกลูเตนินที่เป็นโปรตีนจากข้าวสาลีที่ไม่ละลายน้ำ (water-insoluble wheat grain proteins) เท่านั้น
นอกจากบทบาทในการสนับสนุนการงอกของเมล็ดพืชแล้ว กลูเตนยังมีความสำคัญในวิศวกรรมอาหาร (food engineering ) ด้วย พันธะไดซัลไฟด์ (disulfide bonds) ระหว่างกรดอะมิโนในกลูเตนทำหน้าที่เป็นตัวรับผิดชอบคุณสมบัติหยุ่นหนืด (viscoelastic) และยึดเกาะ (adhesive) ของแป้งที่ผ่านการหมัก อีกทั้งยังมีส่วนช่วยในการสร้างโครงสร้างภายในของขนมปังที่มีลักษณะเหนียวนุ่ม การเพิ่มกลูเตนในแป้งเป็นอีกหนึ่งวิธีที่มีประสิทธิภาพและคุ้มค่าในการปรับปรุงเนื้อสัมผัสและรสชาติของขนมอบ แต่อย่างไรก็ตามกลูเตนยังมีส่วนทำให้เกิดโรคต่างๆ เช่น โรคซีลีแอค (celiac disease) ในมนุษย์ โดยที่เป็นที่ทราบกันดีว่าการบริโภคธัญพืชที่ได้จากพืชในวงศ์ Triticeae เช่น ข้าวสาลี ข้าวบาร์เลย์ และข้าวไรย์ นั้นสามารถกระตุ้นอาการแสดงทางคลินิกในบุคคลที่มีความไวรับต่อการเกิดโรค (susceptible individual) ได้ อาการแสดงทางคลินิกที่คล้ายกันนี้ยังสามารถเกิดขึ้นได้จากการบริโภคข้าวโอ๊ตบางชนิดและเมล็ดข้าวโอ๊ตที่ผ่านการแปรรูปในโรงงานที่ใช้สำหรับแปรรูปข้าวสาลี ข้าวบาร์เลย์ และข้าวไรย์ 2. ถึงแม้ว่าโดยทั่วไปคำว่า "กลูเตน" จะใช้เพื่อหมายถึงโปรตีนจากธัญพืชทั้งหมด แต่กลูเตนที่ได้จากข้าวโพดและข้าวนั้นไม่ได้เชื่อมโยงกับโรคที่เกี่ยวข้องกับกลูเตนในมนุษย์ เพราะฉะนั้นบทความนี้จะใช้คำนี้เพื่อหมายถึงโปรตีนที่ได้จากข้าวบาร์เลย์ ข้าวไรย์ ข้าวโอ๊ต และข้าวสาลีเท่านั้น
โรคที่เกี่ยวข้องกับกลูเตนในมนุษย์
"โรคที่เกี่ยวข้องกับกลูเตน (gluten-related disorders)" เป็นคำรวมๆที่ใช้เพื่ออธิบายอาการแสดงทางคลินิกที่เกิดจากการรับสัมผัสกลูเตน (gluten exposure) โดยเนื่องจากพยาธิกำเนิด (pathogenesis) และสาเหตุ (etiology) ที่แตกต่างกัน ทำให้โรคเหล่านี้สามารถแบ่งออกได้เป็น 3 กลุ่มหลัก ได้แก่ 3. อาการแพ้ (allergic reactions) อาการแพ้กลูเตน (allergic reactions to gluten) อาจเป็นภาวะภูมิไวเกินชนิดที่ 1 หรือชนิดที่ 4 (hypersensitivity type I or type IV) และอาจเกิดขึ้นได้ทั้งภายหลัง (delayed) หรือทันที (immediate) เมื่อรับสัมผัสกลูเตนในบุคคลหรือสัตว์ที่มีความไวรับต่อการเกิดโรค โดยหากมีส่วนเกี่ยวข้องกับอิมมูโนโกลบูลินอี (immunoglobulin E; IgE) ความเชื่อมโยงระหว่าง IgE และกลูเตนจะกระตุ้นกระบวนการตอบสนองภายในเซลล์ (cellular cascades) ในแมสต์เซลล์ (mast cell) และเบโซฟิล (basophils) ซึ่งส่งผลให้เกิดการแตกตัวของแกรนูล (degranulation) และปล่อยไซโตไคน์ (cytokines) รวมถึงสารก่อการอักเสบ (inflammatory mediators) เช่น ฮีสตามีน (histamine) ออกมาซึ่งจะกระตุ้นให้เกิดอาการแสดงทางคลินิกที่อาจแตกต่างกันไปตามตำแหน่งที่ร่างกายมีการตอบสนอง ซึ่งอาการเหล่านี้รวมถึง อาการอาเจียน ท้องเสีย คัน มีผื่นแพ้ ภาวะหอบหืด (asthma) และโรคจมูกอักเสบ (rhinitis) โรคที่เกี่ยวข้องกับกลูเตนที่เกิดร่วมกับอาการแพ้จะเรียกรวมๆ ว่า "โรคภูมิแพ้ข้าวสาลี (wheat allergy)" ซึ่งเป็นหนึ่งในโรคภูมิแพ้อาหาร (food allergies) ที่พบได้บ่อยที่สุดทั่วโลกปฏิกิริยาแพ้ภูมิตัวเอง (autoimmune reactions)
ตัวอย่างที่คลาสสิกในกลุ่มนี้คือโรคซีลีแอค (celiac disease) โดยเมื่อบุคคลที่มีความไวรับบริโภคผลิตภัณฑ์ที่มีข้าวสาลี การมีเกลียดินในทางเดินอาหารจะทำให้ความสมบูรณ์ของผนังเซลล์ที่เชื่อมต่อระหว่างเซลล์เยื่อบุลำไส้ (enterocyte tight junctions) ถูกทำลายลงและเปลี่ยนแปลงการซึมผ่านของลำไส้ (intestinal permeability) 4. เกลียดินที่รั่วไหลออกมาจากลำไส้จะกระตุ้นการตอบสนองทางภูมิคุ้มกันในร่างกายและนำไปสู่การผลิตแอนติบอดีต่อต้านเกลียดิน (anti-gliadin (AG) antibodies) ทั้งนี้นอกจากการซึมผ่านของลำไส้ที่เพิ่มขึ้น การย่อยและดูดซึมกลูเตน (gluten assimilation) ยังก่อให้เกิดปฏิกิริยาแพ้ภูมิตัวเองต่อต้านเอนไซม์ทรานส์กลูตาไมเนสในเนื้อเยื่อ (tissue transglutaminase; tTG) 5. ซึ่งเอนไซม์นี้เป็นเอนไซม์ที่มีหน้าที่หลากหลายซึ่งพบได้ทั่วไปในร่างกายมนุษย์ และมีหน้าที่ในการเอาหมู่อะมิโนออก (deamidation) รวมถึงย้ายหมู่อะมิโน (transamidation) ของกลูตามีนในทางเดินอาหาร ซึ่งเนื่องจากเกลียดินมีกลูตามีนสูง tTG จึงทำการสร้างพันธะที่แน่นหนากับเกลียดินและสร้างเอพิโทปของแอนติเจน (antigenic epitopes) ใหม่ขึ้นมา ทำให้เกิดการพัฒนาออโตแอนติบอดีต่อต้าน tTG (autoantibodies against tTG) นอกจากผลกระทบโดยตรงของกลูเตนแล้ว ความเสี่ยงทางพันธุกรรม (genetic predisposition) ในผู้ป่วยโรคซีลีแอคถือเป็นปัจจัยสำคัญที่ทำให้พวกเขามีความเสี่ยงสูงมากขึ้น โดยผู้ป่วยส่วนใหญ่จะมีรูปแบบยีนของแอนติเจนบนเม็ดเลือดขาวมนุษย์ (human leukocyte antigen (HLA) genes) ที่จำเพาะ จึงทำให้เกิดการตอบสนองทางภูมิคุ้มกัน (immune reaction) ที่รุนแรงขึ้นจากการกระตุ้นการทำงานของลิมโฟไซต์ (lymphocyte activation) 3. โรคซีลีแอคเกี่ยวข้องกับระบบร่างกายหลายระบบ อีกทั้งยังมีออโตแอนติบอดีที่ทำให้ปฏิกิริยาแพ้ภูมิตัวเอง (autoimmune reactions) ต่อต้านกลูเตนนั้นแตกต่างกันออกไป โดยทั่วไปแล้วผู้ป่วยโรคซีลีแอคจะมีการดูดซึมสารอาหารผิดปกติ (malabsorption) และอาการของระบบทางเดินอาหารอื่นๆ อันเป็นผลสืบเนื่องจากความเสียหายที่เกิดกับเซลล์เยื่อบุลำไส้และการฝ่อของวิลลัส (villous atrophy) ที่เกิดขึ้นหลังจากการรับสัมผัสกลูเตน (รูปภาพที่ 1)นักวิทยาศาสตร์เชื่อว่าแอนติบอดีต่อต้าน tTG (anti-tTG) มีส่วนช่วยในการพัฒนาให้เกิดภาวะภูมิคุ้มกันทำลายตนเองบนผิวหนัง (dermatitis herpetiformis) (รูปภาพที่ 2) และภาวะกล้ามเนื้อสูญเสียการประสานสัมพันธ์กันจากกลูเตน (gluten ataxia) ซึ่งเป็นอีกสองรูปแบบของปฏิกิริยาแพ้ภูมิตัวเองที่เกี่ยวข้องกับกลูเตน 6. สิ่งที่น่าสังเกตก็คือแม้ว่าสัญญาณของกระบวนการเกิดโรคเหล่านี้อาจทับซ้อนกัน แต่อาการแสดงทางคลินิกที่เด่นชัดมักจะเกิดที่อวัยวะหรือเนื้อเยื่อที่เกี่ยวข้องเป็นหลัก ยกตัวอย่างเช่น เนื่องจากมีการเกี่ยวข้องกับเซลล์เพอร์คินจี (purkinje cells) และสมองส่วนซีรีเบลลัม (cerebellum) ผู้ป่วยที่มีภาวะกล้ามเนื้อสูญเสียการประสานสัมพันธ์กันจากกลูเตนมักจะมีการเคลื่อนไหวที่ผิดปกติ (movement disorders) เช่น อาการเดินเซ (ataxia) อาการสั่น (tremor) และอาการกล้ามเนื้อกระตุกรัว (myoclonus) 6. การวิเคราะห์ระดับแอนติบอดีต่อต้าน tTG และแอนติบอดีต่อต้านเกลียดินในซีรั่ม (serum anti-tTG and AG antibodies) จึงเป็นเครื่องมือที่มีประโยชน์อย่งยิ่งในการช่วยวินิจฉัยกรณีที่สงสัยว่าเกิดจากปฏิกิริยาแพ้ภูมิตัวเองต่อกลูเตน (autoimmune reactions to gluten)
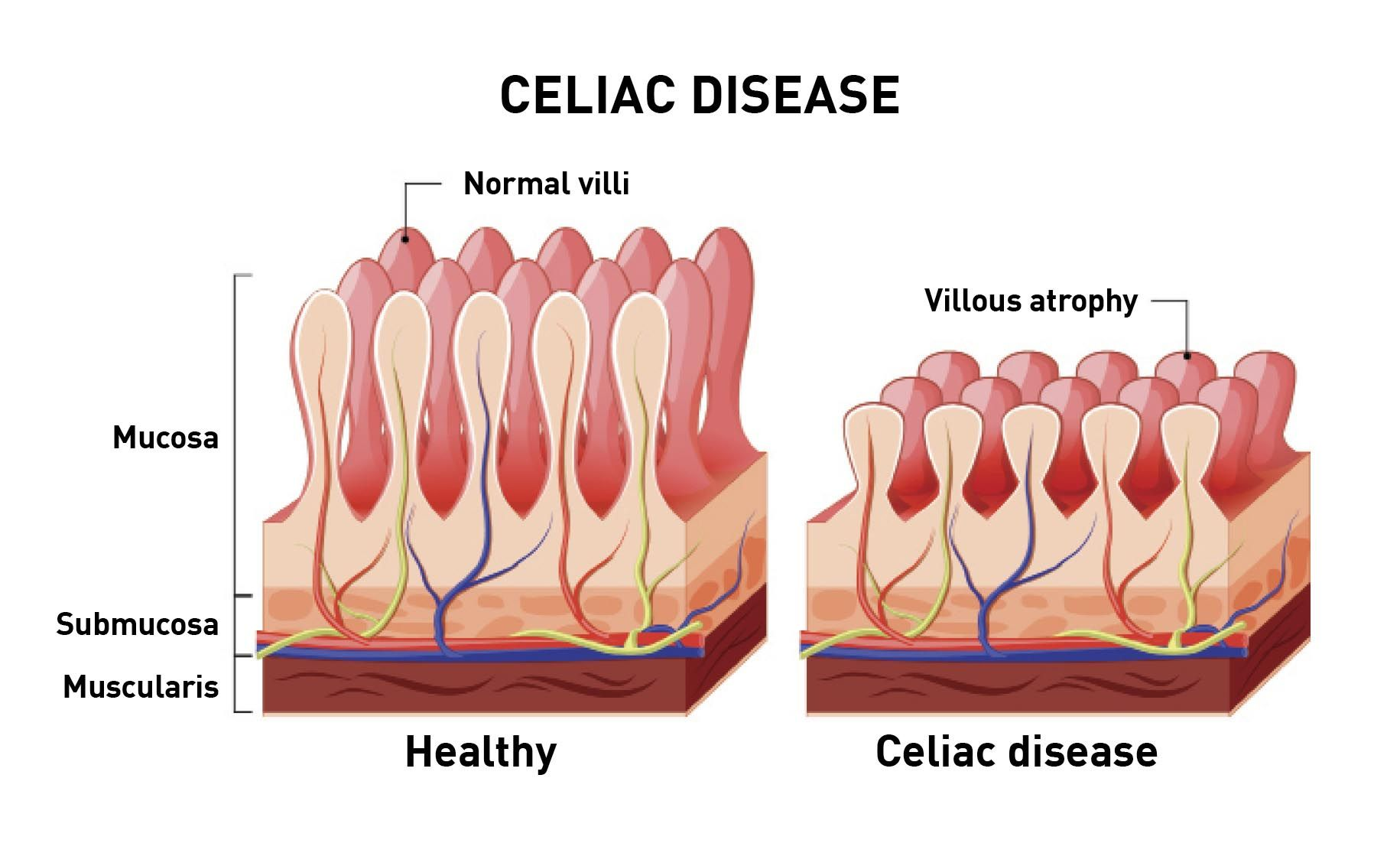
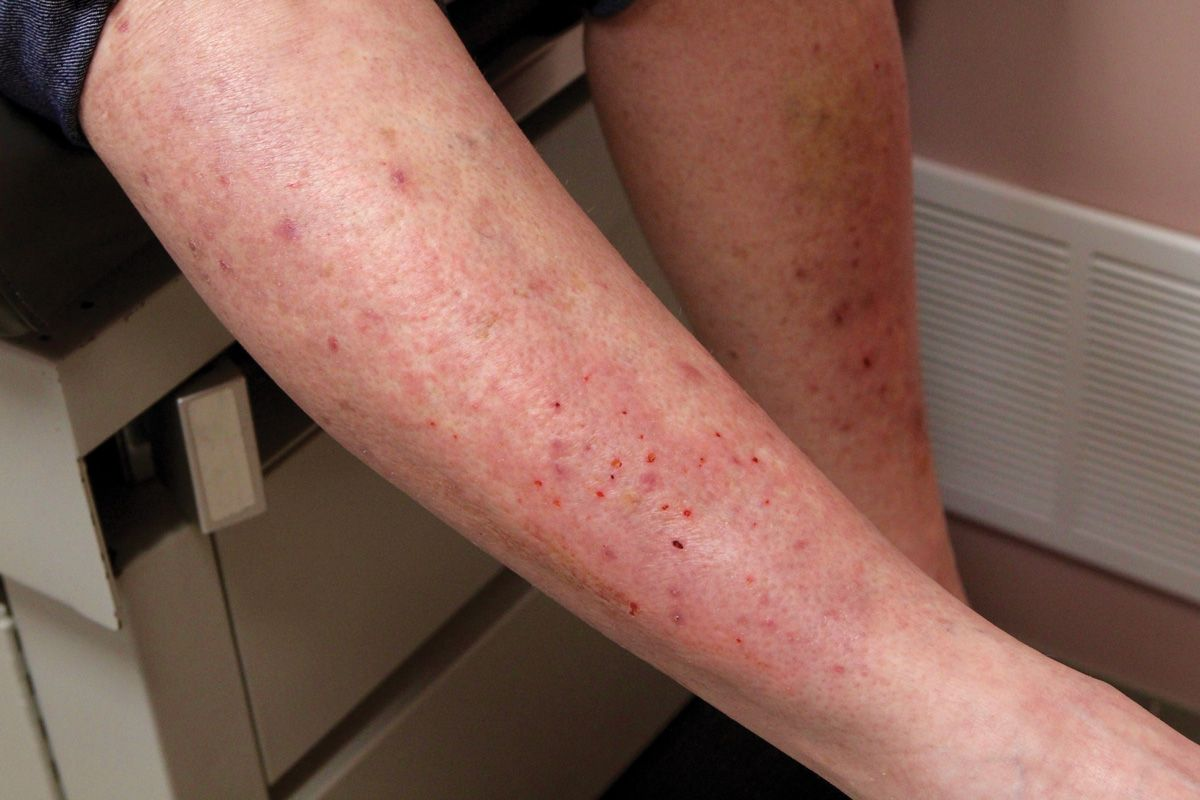
ปฏิกิริยาอื่นๆที่เกี่ยวข้องกับกลูเตน
ผู้ป่วยบางคนอาจมีปฏิกิริยาหลังจากการบริโภคกลูเตนโดยที่ไม่สามารถระบุได้ว่าเป็นกลไกการแพ้หรือกลไกการแพ้ภูมิตัวเอง (allergic nor autoimmune mechanisms) โดยอาการแสดงทางคลินิกจะคล้ายคลึงกับที่พบในบุคคลที่มีปฏิกิริยาการแพ้หรือปฏิกิรยาแพ้ภูมิตัวเองต่อกลูเตน แต่การตรวจทางจุลพยาธิวิทยา (histopathological examination) ของชิ้นเนื้อลำไส้ (intestinal biopsies) นั้นจะไม่พบความผิดปกติ และแม้ว่าในบางครั้งอาจพบระดับแอนติบอดีต่อต้านเกลียดินในซีรั่มที่สูงขึ้น แต่ก็มักจะไม่พบแอนติบอดีต่อต้าน tTG ในซีรั่มอย่างชัดเจน 3. อาการแสดงทางคลินิกที่คล้ายกันทำให้การวินิจฉัย "ปฏิกิริยาที่ไม่ใช่การแพ้หรือการแพ้ภูมิตัวเอง" สามารถทำได้โดยการคัดออก (exclusion) เท่านั้น ดังนั้นกลุ่มนี้จึงมักเรียกว่าภาวะไวต่อกลูเตนที่ไม่ใช่โรคซีลีแอคหรือ non-celiac gluten sensitivity 3. ทั้งนี้แม้ว่าจะมีการจัดกลุ่มอย่างชัดเจน แต่ความชุกที่แท้จริง (true prevalence) ของโรคที่เกี่ยวข้องกับกลูเตนในมนุษย์นั้นก็ยังไม่ชัดเจน เนื่องจากบุคคลที่มีอาการแสดงทางคลินิกที่เกี่ยวข้องส่วนใหญ่มักจะพยายามปรับเปลี่ยนอาหาร (diet modification) ด้วยตนเองโดยไม่ได้รับคำแนะนำจากแพทย์ รวมถึงในกรณีที่สงสัยว่าจะเป็นโรคที่เกี่ยวข้องกับกลูเตน การใช้เครื่องมือวินิจฉัย เช่น การตรวจระดับแอนติบอดีในซีรั่ม (serum antibody profile) การตรวจยีน (genetic typing) และการตรวจชิ้นเนื้อลำไส้ (intestinal biopsies) จะช่วยในการตรวจสอบให้ง่ายขึ้น แม้ว่าความสัมพันธ์เชิงสาเหตุ (causal relationship) ระหว่างส่วนประกอบในอาหาร (dietary component) และโรคนั้นจะพิสูจน์ได้ค่อนข้างยาก แต่การลองควบคุมอาหาร (elimination diet test) ตามด้วยการทดสอบด้วยการบริโภค (provocation tests) กลูเตนบริสุทธิ์ (pure gluten) หรืออาหารที่มีกลูเตน (gluten-containing foods) อาจช่วยในการเชื่อมโยงการรับสัมผัสกลูเตนกับอาการแสดงทางคลินิก อย่างไรก็ตามสิ่งที่น่าสังเกตคือการหยุดรับประทานกลูเตนในอาหารอาจทำให้การทดสอบได้ผลลบลวง (false negative tests) ซึ่งรวมไปถึงการไม่พบความผิดปกติของระดับแอนติบอดีในซีรั่มและไม่พบการเปลี่ยนแปลงทางจุลพยาธิวิทยาจากชิ้นเนื้อลำไส้ของผู้ป่วยโรคซีลีแอค 7.โรคที่เกี่ยวข้องกับกลูเตนในสุนัข
อาการแสดงทางคลินิกที่เกี่ยวข้องกับกลูเตนในอาหารได้รับการรายงานในสุนัขบางสายพันธุ์ในช่วงไม่กี่ทศวรรษที่ผ่านมา การเชื่อมโยงระหว่างกลูเตนและโรคระบบทางเดินอาหาร (enteropathy) ที่พบในสุนัขพันธุ์ไอริชเซ็ตเตอร์นั้นได้รับการศึกษาตั้งแต่ปลายศตวรรษที่ 20 โดยมีการศึกษาหนึ่งที่พยายามจำแนกลักษณะของโรคนี้และประเมินความแตกต่างระหว่างโรคนี้กับโรคซีลีแอคในมนุษย์ 7. การศึกษานี้ได้ทำการประเมินสุนัขพันธุ์ไอริชเซ็ตเตอร์ที่มีปัญหาในการรักษาน้ำหนักตัว (maintaining body weight) และถูกส่งตัวมาเพื่อทำการวินิจฉัย (รูปภาพที่ 3) สุนัขที่เข้าร่วมการศึกษามีผลการตรวจอุจจาระที่ปกติ ความเข้มข้นของโคบาลามินในซีรั่มที่ปกติ (serum cobalamin concentrations) และการทำงานของตับอ่อนในการผลิตเอนไซม์ย่อยอาหาร (exocrine pancreatic function) ปกติ แต่การตรวจทางจุลพยาธิวิทยาของชิ้นเนื้อลำไส้เล็กเผยให้เห็นการฝ่อของวิลลัสในระดับความรุนแรงต่างๆ ซึ่งอาจส่งผลให้การดูดซึมสารอาหารผิดปกติและทำให้มีปัญหาในการรักษาน้ำหนักตัว อย่างไรก็ตามการศึกษานี้ไม่ได้ประเมินประวัติการให้อาหาร (dietary history) ของสุนัขเหล่านี้อย่างละเอียด และไม่สามารถสรุปความสัมพันธ์เชิงสาเหตุระหว่างกลูเตนและโรคระบบทางเดินอาหารได้อย่างชัดเจน
แม้ว่าความสัมพันธ์เชิงสาเหตุที่เป็นไปได้จะถูกแนะนำไว้ในการศึกษาเหล่านี้ แต่การศึกษากลับไม่พบความแตกต่างอย่างมีนัยสำคัญ (significant differences) ในระดับความเข้มข้นของแอนติบอดีต่อต้านเกลียดินในซีรั่ม (serum AG antibody concentration) ระหว่างสุนัขพันธุ์ไอริชเซ็ตเตอร์ที่มีความไวรับต่อโรคและถูกเลี้ยงด้วยอาหารที่มีข้าวสาลีเป็นส่วนประกอบหรืออาหารที่ปราศจากธัญพืช อีกทั้งระดับความเข้มข้นของออโตแอนติบอดีในซีรั่ม (concentrations of serum autoantibody) และอิมมูโนโกลบูลิน (immunoglobulins) อื่นๆก็ไม่ได้มีความแตกต่างกันอย่างมีนัยสำคัญระหว่างสองกลุ่ม 9. โดยเมื่อพิจารณาจากการไม่มีส่วนร่วมของระบบภูมิคุ้มกันและออโตอิมมูน โรคระบบทางเดินอาหารที่รายงานในสุนัขสายพันธุ์นี้จึงดูเหมือนจะแตกต่างจากโรคซีลีแอคที่ถูกกำหนดไว้โดยทั่วไป และแม้ว่าพยาธิกำเนิดและความเสี่ยงทางพันธุกรรม (genetic predisposition) ของโรคระบบทางเดินอาหารในสุนัขพันธุ์ไอริชเซ็ตเตอร์ยังคงต้องได้รับการศึกษาต่อไป แต่สุนัขเหล่านี้ก็ดูเหมือนจะได้รับประโยชน์จากการให้อาหารที่ปราศจากกลูเตน การประเมินผลการศึกษานี้พร้อมกับพิจารณาแนวโน้มล่าสุดในด้านโภชนาการของมนุษย์จึงทำให้กลูเตนในอาหารเป็นหัวข้อที่ได้รับความสนใจอย่างมากในการพูดคุยระหว่างเจ้าของสัตว์เลี้ยงและสัตวแพทย์
นอกจากนี้กลูเตนยังได้รับการรายงานว่าเกี่ยวข้องกับความผิดปกติของการเคลื่อนไหวที่ไม่สามารถควบคุมได้ซึ่งเกิดเป็นพักๆ (paroxysmal dyskinesia หรือ PD) ในสุนัขพันธุ์บอร์เดอร์เทอเรีย (รูปภาพที่ 4) paroxysmal dyskinesia เป็นคำที่ใช้เรียกกลุ่มของภาวะที่มีอาการเคลื่อนไหวผิดปกติที่เกิดเป็นพักๆ ซึ่งรวมถึงภาวะกล้ามเนื้อบีบเกร็ง (dystonia) และอาการสั่น (tremor) โดยสามารถถูกกระตุ้นได้จากการกระตุ้นต่างๆ เช่น ความตื่นเต้น การออกกำลังกาย หรือความเครียด 10. อาการเหล่านี้มักพบในสุนัขอายุน้อย (young) และวัยกลางคน (middle-aged dogs) บางสายพันธุ์ เช่น บอร์เดอร์เทอเรีย (Border Terriers) คาวาเลียร์คิงชาร์ลส์สแปนเนียล (Cavalier King Charles Spaniels) ชิโนคส์ (Chinooks) นอร์วิชเทอเรีย (Norwich Terriers) และซอฟท์โคทเต็ดวีเทนเทอเรีย (Soft Coated Wheaten Terriers) 11 นอกจากนี้ถึงแม้จะมีการเคลื่อนไหวนอกอำนาจจิตใจที่ผิดปกติ (abnormal involuntary movements) ซึ่งอาจใช้เวลานานตั้งแต่หลายนาทีจนถึงหลายชั่วโมง แต่ผู้ป่วยก็ยังดูเหมือนมีสติอยู่ตลอดระยะเวลาของอาการเหล่านี้ และ (แตกต่างจากความผิดปกติทางระบบประสาท (neurological deficits) บางอย่างที่มักพบหลังจากการชัก (epileptic seizure) ที่ยาวนาน) การฟื้นตัวจากอาการที่หายได้เอง (self-limiting episodes) เหล่านี้มักไม่มีปัญหา โดยสุนัขจะกลับมาพฤติกรรมปกติระหว่างช่วงอาการ 12.

แม้ว่าพยาธิกำเนิดของโรคจะยังไม่เข้าใจอย่างสมบูรณ์ แต่มีการพูดถึงการกลายพันธุ์ของยีน (gene mutations) ว่าอาจเป็นสาเหตุของความผิดปกติของการเคลื่อนไหวที่ไม่สามารถควบคุมได้ซึ่งเกิดเป็นพักๆ (PD) ในสุนัขได้ มีการศึกษาฉบับหนึ่งรายงานการหายไปของยีน BCAN (BCAN gene) ในสุนัขพันธุ์คาวาเลียร์คิงชาร์ลส์สแปนเนียล . ซึ่งยีนนี้จะถอดรหัส (encodes) ได้เป็นโปรติโอไกลแคน (proteoglycan) ที่ชื่อว่า brevican ซึ่งเป็นส่วนหนึ่งของสารเคลือบเซลล์ (extracellular matrix) ในสมองและมีหน้าที่ในการรักษาเสถียรภาพของการถ่ายทอดกระแสประสาท synaptic stability) การกลายพันธุ์ของ BCAN นั้นถือว่ามีความสัมพันธ์อย่างมากกับกลุ่มอาการล้มไม่มีแรงเคลื่อนไหวแบบเป็นๆหายๆ (episodic falling syndrome) ซึ่งเป็นความผิดปกติของการเคลื่อนไหวที่ไม่สามารถควบคุมได้ซึ่งเกิดเป็นพักๆที่พบในสุนัขพันธุ์คาวาเลียร์คิงชาร์ลส์สแปนเนียล 11
ในทางตรงกันข้าม ส่วนประกอบในอาหารดูเหมือนจะมีบทบาทสำคัญในความผิดปกติของการเคลื่อนไหวที่ไม่สามารถควบคุมได้ซึ่งเกิดเป็นพักๆ (paroxysmal dyskinesia หรือ PD) ในสุนัขพันธุ์บอร์เดอร์เทอเรีย (ซึ่งเคยรู้จักในชื่อ canine epileptoid cramping syndrome หรือ Spike’s disease) มีการศึกษาหนึ่งพยายามที่จะจำแนกประเภทของ PD ในสุนัขพันธุ์นี้ โดยได้รวมสุนัขที่มีคุณสมบัติตามการสังเกตจากเจ้าของ การบันทึกวิดีโอ และประวัติการรักษา 12. เป็นที่น่าสนใจว่าในการศึกษานี้พบว่าอาการทางผิวหนัง (เช่น การคันบ่อย) และอาการระบบทางเดินอาหารที่รุนแรงเล็กน้อย (เช่น อาเจียนและท้องเสีย) พบได้ถึงร้อยละ 50 ของสุนัขที่ได้รับการประเมิน นอกจากนี้สุนัขจำนวนมากที่ได้เปลี่ยนอาหาร (เป็นอาหารสูตรที่ "ไม่ก่อให้เกิดอาการแพ้ (hypoallergenic)" หรืออาหารที่มีแหล่งโปรตีนและคาร์โบไฮเดรตเพียงชนิดเดียว) ก็พบว่ามีความถี่ของการเกิด PD ลดลง ซึ่งแสดงให้เห็นว่าอาจมีการแพ้อาหาร (food allergy) หรือแพ้อาหารแฝง (food intolerance) เป็นสาเหตุพื้นเดิม (underlying cause) ผลการศึกษานี้ยังได้ระบุว่านักเพาะพันธุ์สัตว์ (breeders) และเจ้าของสุนัขพันธุ์บอร์เดอร์เทอเรียที่มีอาการเหล่านี้ได้กล่าวว่าพวกเขาพบอาการผิดปกติในการเคลื่อนไหวลดลงหลังจากที่ได้เปลี่ยนให้สุนัขที่มีอาการแสดงทางคลินิกไปกินอาหารที่ปราศจากกลูเตน
ต่อมามีการศึกษาขนาดเล็ก ได้ทำการคัดเลือกสุนัขพันธุ์บอร์เดอร์เทอเรียที่เป็น PD จำนวน 6 ตัว และทำการลองควบคุมอาหารอย่างเข้มงวดเป็นเวลา 9 เดือนโดยใช้อาหารสูตรรักษาโรคที่ประกอบไปด้วยส่วนผสมที่จำกัดจำนวนไฮโดรไลเสตทำให้ดูเหมือนจะปราศจากกลูเตน ผลการทดลองพบว่าความถี่ของการเกิด PD ในสุนัขที่เจ้าของปฏิบัติตามการรักษาลดลงอย่างมีนัยสำคัญ และระดับความเข้มข้นของแอนติบอดี AG และแอนติบอดีต่อต้าน tTG ในซีรั่มของสุนัขเหล่านี้ลดลงด้วย 13. ทั้งนี้แม้จะเป็นกลุ่มตัวอย่างที่ขนาดเล็ก แต่การศึกษานี้ก็ได้แสดงให้เห็นถึงการตอบสนองที่ดีต่ออาหารที่ปราศจากกลูเตนในสุนัขที่ได้รับผลกระทบ
ในการศึกษาผลการรักษา (follow-up study) นักวิจัยได้จัดกลุ่มสุนัขพันธุ์บอร์เดอร์เทอเรียที่เข้าร่วมการศึกษาออกเป็น 4 กลุ่มตามการวินิจฉัยทางคลินิกเพื่อพยายามจำแนกผลการตรวจปริมาณแอนติบอดี (serological profile) ของสุนัขที่มีความผิดปกติของการเคลื่อนไหวที่ไม่สามารถควบคุมได้ซึ่งเกิดเป็นพักๆ 14. โดยนอกจากกลุ่มสุนัขที่สุขภาพดี กลุ่มสุนัขที่สันนิษฐานว่าเป็น PD และกลุ่มสุนัขที่สันนิษฐานว่าเป็นโรคลมชักชนิดไม่ทราบสาเหตุ (idiopathic epilepsy) สุนัขตัวอื่นๆที่เข้าร่วมการศึกษาจะได้รับการจัดกลุ่มเป็นกลุ่มที่ 4 (สัตว์ที่มีการวินิจฉัยทางคลินิกที่คลุมเครือหรือมีภาวะที่ไม่เกี่ยวข้องกับระบบประสาท (non-neurological conditions)) โดยในกลุ่มนี้ไม่มีสุนัขที่ได้รับการให้อาหารที่ปราศจากกลูเตนเลย นักวิจัยไม่พบการเพิ่มสูงขึ้นของระดับความเข้มข้นของแอนติบอดี (serological markers) เช่น แอนติบอดีต่อต้าน tTG และแอนติบอดีต่อต้านเกลียดินในสุนัขพันธุ์บอร์เดอร์เทอเรียทั้งหมดที่สันนิษฐานว่าเป็น PD นอกจากนี้ระดับความเข้มข้นของแอนติบอดีก็ไม่ได้พบเป็นลักษณะเฉพาะในสุนัขที่มีอาการแสดงทางคลินิกที่สอดคล้องกับ PD ทั้งนี้เช่นเดียวกับมนุษย์ที่มีโรคที่เกี่ยวข้องกับกลูเตน สุนัขพันธุ์บอร์เดอร์เทอเรียที่มีระดับความเข้มข้นของแอนติบอดีสูงดูเหมือนจะมีอาการแสดงทางคลินิกที่ค่อนข้างหลากหลาย แต่อย่างไรก็ตามการตรวจระดับความเข้มข้นของแอนติบอดีนี้ดูเหมือนจะมีความจำเพาะสูงสำหรับการวินิจฉัยความผิดปกติของการเคลื่อนไหวที่ไม่สามารถควบคุมได้ซึ่งเกิดเป็นพักๆและไวต่อกลูเตน (paroxysmal gluten-sensitive dyskinesia) ในสุนัขสายพันธุ์นี้ 15. ถึงแม้ว่าค่าวินิจฉัย (diagnostic value) จะลดลงเมื่อสุนัขที่ได้รับผลกระทบได้รับการเปลี่ยนเป็นอาหารที่ปราศจากกลูเตนแล้ว การผสมผสานระหว่างการตรวจปริมาณแอนติบอดี ประวัติการกินอาหารที่ครบถ้วน และเครื่องมือวินิจฉัย (diagnostic tools) เพื่อตัดสาเหตุที่เกี่ยวข้องกับสมองภายนอกและภายใน (extra- and intra-cranial causes) ออก จะช่วยให้สัตวแพทย์สามารถศึกษาวิจัย PD ในสุนัขพันธุ์บอร์เดอร์เทอเรียได้
โดยเมื่อพิจารณาจากการไม่มีส่วนร่วมของระบบภูมิคุ้มกันและออโตอิมมูน โรคระบบทางเดินอาหารที่รายงานในสุนัขสายพันธุ์นี้จึงดูเหมือนจะแตกต่างจากโรคซีลีแอคที่ถูกกำหนดไว้โดยทั่วไป
ในปัจจุบันข้อมูลด้านระบาดวิทยา (epidemiology data) ที่เกี่ยวกับโรคที่เกี่ยวข้องกับกลูเตนในประชากรสุนัขทั่วไปนั้นยังคงต้องการการศึกษาวิจัยเพิ่มเติม นอกจากนี้ยังต้องมีการศึกษาค้นคว้าเพิ่มเติมเพื่อทำความเข้าใจเกี่ยวกับการระบุลักษณะ (phenotyping) และพยาธิกำเนิด (pathogenesis) ของโรคเหล่านี้ให้ดีขึ้น โดยถึงแม้จะยังมีช่องว่างในความรู้ต่างๆเหล่านี้ แต่สุนัขบางสายพันธุ์ที่มีอาการแสดงทางคลินิกและมีประวัติการกินอาหารที่สอดคล้องกับโรคที่เกี่ยวข้องกับกลูเตนก็สามารถได้รับประโยชน์จากการปรับเปลี่ยนอาหารตามข้อมูลที่มีอยู่
เมื่อสงสัยว่าสุนัขเป็นโรคที่เกี่ยวข้องกับกลูเตน เป้าหมายของสัตวแพทย์คือการให้โภชนาการที่ครบถ้วนและสมดุลโดยใช้ส่วนผสมที่ปราศจากกลูเตนที่เหมาะสมกับช่วงชีวิตของสุนัข เพื่อช่วยบรรเทาอาการแสดงทางคลินิกและให้พลังงานอย่างเพียงพอเพื่อส่งเสริมหรือรักษาภาวะร่างกายอย่างที่ควรจะเป็น (ideal body condition) องค์การอาหารและยา (FDA) ของประเทศสหรัฐอเมริกาได้กำหนดข้อกำหนดสำหรับการระบุฉลาก “ปราศจากกลูเตน” บนผลิตภัณฑ์อาหาร ซึ่งจะช่วยให้ผู้ที่เป็นโรคที่เกี่ยวข้องกับกลูเตนสามารถเลือกผลิตภัณฑ์ที่เหมาะสมเพื่อรักษาโภชนาการที่ดีได้ 16. ทั้งนี้แม้ว่าจะสะดวกสบาย แต่สิ่งที่ต้องระวังก็คือการตัดส่วนผสมในอาหารบางส่วนอาจทำให้เกิดภาวะขาดสารอาหาร (nutritional deficiencies) ได้ เช่น ใยอาหารและสังกะสี (zinc) ดังนั้นจึงควรได้รับคำแนะนำจากผู้เชี่ยวชาญเพื่อให้แน่ใจว่าได้รับโภชนาการที่ครบถ้วนและสมดุล 17. ในทางสัตวแพทย์ยังมีรายงานการขาดสารหารที่เกิดจากอาหารที่ทำเองที่บ้าน (home-cooked diet) ซึ่งไม่ได้วางแผนอย่างมืออาชีพ 18. นอกจากนี้แม้ว่าจะสามารถจัดเตรียมอาหารทำเองที่บ้านที่มีสารอาหารครบถ้วนและสมดุลโดยนักโภชนาการสัตวแพทย์ที่ได้รับการรับรอง (board-certified veterinary nutritionist) ได้ แต่การให้อาหารประเภทนี้อาจไม่สะดวกเสมอไป เนื่องจากความยุ่งยากในการเตรียมอาหารและทรัพยากรที่ต้องใช้ 19. ซึ่งโชคดีที่ตอนนี้มีอาหารสุนัขเชิงพาณิชย์ (commercial dog foods) หลายตัวที่ได้รับการพัฒนาเพื่อรองรับความต้องการทางโภชนาการของสุนัขในทุกช่วงชีวิต วิถีการดำเนินชีวิต (lifestyles) และกระบวนการของโรค โดยเจ้าของสัตว์สามารถเลือกอาหารที่เหมาะสมที่สุดสำหรับสุนัขของตนภายใต้การแนะนำจากสัตวแพทย์ (รูปภาพที่ 5) อาหารที่ปราศจากกลูเตนที่ผลิตจากบริษัทที่มีชื่อเสียงนั้นสามารถพิจารณาใช้ได้และการใช้ WSAVA checklist ยังช่วยในการประเมินอาหารสัตว์และบริษัทผู้ผลิตอาหารสัตว์ด้วย 20.

เนื่องจากยังไม่มีการข้อกำหนดที่ชัดเจนเกี่ยวกับการอ้างสิทธิ์ว่าเป็นอาหารที่ปราศจากกลูเตนจากหน่วยงานที่เกี่ยวข้อง เช่น สมาคมควบคุมอาหารสัตว์แห่งอเมริกา (AAFCO) การตรวจสอบว่าอาหารสัตว์เชิงพาณิชย์นั้นเป็นอาหารที่ปราศจากกลูเตนหรือไม่จำเป็นต้องประเมินรายการส่วนผสมบนบรรจุภัณฑ์อย่างละเอียด ซึ่งบางครั้งอาจต้องใช้การคาดเดาจากความรู้เนื่องจากการควบคุมคุณภาพของบริษัทผู้ผลิตอาหารสัตว์นั้นอาจมีความแตกต่างกัน<sup>20.</sup>. มีการศึกษาหนึ่งรายงานว่าอาหารเชิงพาณิชย์ “ส่วนผสมจำกัด (limited-ingredient)” บางตัวที่วางขายในร้านค้ามีโปรตีนจากสัตว์ที่ไม่ได้ระบุไว้ในฉลากบนบรรจุภัณฑ์ <sup>22.</sup> แม้ว่าจะมีข้อจำกัดในงานวิจัยนี้ เช่น ความแปรปรวนของรอบการผลิต (batch variation) และผลบวกลวง (false positive) ของการทดสอบที่มีความละเอียดอ่อน ผลลัพธ์เหล่านี้ชี้ให้เห็นถึงความเป็นไปได้ในการปนเปื้อนข้ามระหว่างกระบวนการผลิตซึ่งอาจทำให้อาหารสัตว์เชิงพาณิชย์ที่มีส่วนผสมจำกัดนั้นไม่เหมาะสมเมื่อจำเป็นต้องทำการลองควบคุมอาหาร (elimination diet) ในความเห็นของผู้เขียน อาหารสัตว์สูตรรักษาโรค (veterinary therapeutic diet) ที่ได้รับการออกแบบโดยใช้ส่วนผสมที่ปราศจากกลูเตนในจำนวนที่จำกัดและผลิตโดยผู้ผลิตที่มีประสบการณ์พร้อมกับการควบคุมคุณภาพที่ดีก็ถือเป็นตัวเลือกที่ดีเมื่อทำการทดลองดังกล่าว ตัวเลือกที่เป็นไปได้ซึ่งรวมถึงอาหารหลายสูตรที่ถูกออกแบบมาเพื่อรักษาอาการที่ไม่พึงประสงค์จากอาหาร (adverse food reactions) หรืออาหารสูตร hypoallergenic diets ที่ถูกออกแบบมาเพื่อใช้สำหรับโรคภูมิแพ้อาหารที่เกี่ยวข้องกับโรคผิวหนัง (dermatology-related food allergies)
เราควรทราบว่าอาหารเชิงพาณิชย์มีความแตกต่างกันอย่างมากในหลายๆด้าน รวมถึงวิธีการผลิตและคุณค่าทางโภชนาการ ดังนั้นชื่อของผู้ผลิตและผลิตภัณฑ์ ประเภทของอาหาร (อาหารแห้งหรือเปียก) และปริมาณอาหารที่ควรให้ในแต่ละวันจะต้องให้แจ้งแก่ลูกค้าเมื่อแนะนำอาหารเพื่อหลีกเลี่ยงความเข้าใจผิด ทั้งนี้ขึ้นอยู่กับอาการแสดงทางคลินิก ระบบร่างกายที่เกี่ยวข้อง และการตอบสนองของสัตว์ป่วย การลองควบคุมอาหาร (elimination diet trial) อาจใช้เวลา 1-2 สัปดาห์สำหรับอาการทางระบบทางเดินอาหาร และอาจใช้เวลานานถึง 12 สัปดาห์สำหรับอาการที่เกี่ยวข้องกับโรคผิวหนัง ซึ่งโดยปกติแล้วการทดลองนี้ควรตามด้วยการทดสอบด้วยการบริโภค (provocation testing) เพื่อประเมินการตอบสนองของสัตว์ป่วยต่ออาหารที่สงสัยว่าจะเกี่ยวข้องกับอาการแสดงทางคลินิก การทดสอบเหล่านี้จะช่วยยืนยันการวินิจฉัยโรคที่เกี่ยวข้องกับกลูเตนและระบุความจำเป็นในการเริ่มแผนการติดตามและการให้อาหารที่ปราศจากกลูเตนตลอดชีวิตสำหรับสุนัขที่ได้รับผลกระทบ
สุดท้ายนี้แม้ว่าจนถึงปัจจุบันจะมีการบันทึกอาการแสดงทางคลินิกของโรคที่เกี่ยวข้องกับกลูเตนในสุนัขพันธุ์บอร์เดอร์เทอเรีย (Border Terriers) และพันธุ์ไอริชเซ็ตเตอร์ (Irish Setters) เท่านั้น แต่บางครั้งเจ้าของสัตว์ก็อาจจะขออาหารที่ปราศจากกลูเตนเนื่องจากอาการแพ้กลูเตนของตนเองซึ่งอาจเป็นอันตรายถึงชีวิตในบุคคลที่มีความเสี่ยง เพราะฉะนั้นคำขอในกรณีนี้ควรได้รับการพิจารณาอย่างจริงจังและสัตวแพทย์ต้องให้ความสำคัญในการวางแผนการกินอาหารที่เหมาะสมสำหรับสุนัข
สรุป
โรคที่เกี่ยวข้องกับกลูเตนนั้นได้รับการรายงานทั้งในมนุษย์และสุนัข แต่สามารถจัดการได้ด้วยการหลีกเลี่ยงกลูเตนในอาหารอย่างระมัดระวัง ทั้งนี้แม้ว่าความชุกและพยาธิกำเนิดของโรคที่เกี่ยวข้องกับกลูเตนในสุนัขยังคงต้องการการศึกษาเพิ่มเติม แต่การตอบสนองในเชิงบวกที่เห็นได้ในสุนัขที่ได้รับผลกระทบนั้นก็ทำให้ทราบว่าการแทรกแซงทางโภชนาการในเวลาที่เหมาะสมถือเป็นสิ่งสำคัญ เมื่อกลูเตนเป็นหัวข้อหลักในการโภชนาการทั้งในมนุษย์และสุนัข การมีพื้นฐานความรู้ที่ดีดจะช่วยให้สัตวแพทย์สามารถให้คำแนะนำที่ดีที่สุดแก่เจ้าของสัตว์เลี้ยงได้ว่าเมื่อใดที่ควรปรับเปลี่ยนอาหารของสุนัข
Chih-Fan Chiang
DVM, MPVM, Dip. ACVIM (Nutrition), Good Nutrition DVM Consulting Services, Taiwan
Taiwan
Chih-Fan Chiang obtained his veterinary degree from the School of Veterinary Medicine at the National University of Taiwan. He then pursued residency training at the Veterinary Medical Teaching Hospital at the University of California, Davis, and achieved board certification in clinical nutrition with the American College of Veterinary Internal Medicine in 2021. Since then Dr. Chiang has been sharing his experience in clinical nutrition to optimize patient care and to promote veterinary education, and is currently the board-certified veterinary nutritionist at a private consultancy in Taiwan.
References
- Osborne TB. The vegetable proteins. 2nd ed. London (UK): Longmans, Green and Co, 1924.
- <div>Biesiekierski JR. What is gluten? J. Gastroenterol. Hepatol. 2017;32:78-81.</div>
- <div>Sapone A, Bai JC, Ciacci C, et al. Spectrum of gluten-related disorders: consensus on new nomenclature and classification. BMC Med. 2012;10:13.</div>
- <div>Lammers KM, Lu R, Brownley J, et al. Gliadin induces an increase in intestinal permeability and zonulin release by binding to the chemokine receptor CXCR3. Gastroenterol. 2008;135:194-204.</div>
- <div>Dieterich W, Ehnis T, Bauer M, et al. Identification of tissue transglutaminase as the autoantigen of celiac disease. Nat. Med. 1997;3:797-801.</div>
- <div>Taraghikhah N, Ashtari S, Asri N, et al. An updated overview of spectrum of gluten-related disorders: clinical and diagnostic aspects. BMC Gastroenterol. 2020;20:258.</div>
- <div>Batt RM, Carter MW, McLean L. Morphological and biochemical studies of a naturally occurring enteropathy in the Irish setter dog: a comparison with celiac disease in man. Res. Vet. Sci. 1984;37:339-346.</div>
- <div>Hall EJ, Batt RM. Dietary modulation of gluten sensitivity in a naturally occurring enteropathy of Irish setter dogs. Gut. 1992;33:198-205.</div>
- <div>Hall EJ, Carter SD, Barnes A, et al. Immune responses to dietary antigens in gluten-sensitive enteropathy of Irish setters. Res. Vet. Sci. 1992;53:293-299.</div>
- <div>Lowrie M, Garosi L. Classification of involuntary movements in dogs: paroxysmal dyskinesias. Vet. J. 2017;220:65-71.</div>
- <div>Gill JL, Tsai KL, Krey C, et al. A canine BCAN microdeletion associated with episodic falling syndrome. Neurobiol. Dis. 2012;45:130-136.</div>
- <div>Black V, Garosi L, Lowrie M, et al. Phenotypic characterization of canine epileptoid cramping syndrome in the Border terrier. J. Small Anim. Pract. 2014;55:102-107.</div>
- <div>Lowrie M, Garden OA, Hadjivassiliou M, et al. The clinical and serological effect of a gluten-free diet in Border terriers with epileptoid cramping syndrome. J. Vet. Intern. Med. 2015;29:1564-1568.</div>
- <div>Lowrie M, Garden OA, Hadjivassiliou M, et al. Characterization of paroxysmal gluten-sensitive dyskinesia in Border terriers using serological markers. J. Vet. Intern. Med. 2018;32:775-781.</div>
- <div>US Food & Drug Administration. Gluten and food labeling. Available at: https://www.fda.gov/food/nutrition-education-resources-materials/gluten-and-food-labeling. Accessed August 8, 2022.</div><div><li class="rc-list__item reference-list-item" data-gtm-vis-has-fired37450158_104="1" style="box-sizing: inherit; line-height: 1.5; position: relative; margin-bottom: 0.5rem;"></li></div>
- <div>Vici G, Belli L, Biondi M, et al. Gluten free diet and nutrient deficiencies: a review. Clin. Nutr. 2016;35:1236-1241.</div>
- <div>Stockman J, Fascetti AJ, Kass PH, et al. Evaluation of recipes of home-prepared maintenance diets for dogs. J. Am. Vet. Med. Assoc. 2013;242:1500-1505.</div>
- <div>Johnson LN, Linder DE, Heinze CR, et al. Evaluation of owner experiences and adherence to home-cooked diet recipes for dogs. J. Small Anim. Pract. 2016;57:23-27.</div>
- <div>WSAVA Global Nutrition Committee: guidelines on selecting pet foods. Available at: https://wsava.org/wp-content/uploads/2021/04/Selecting-a-pet-food-for-your-pet-updated-2021_WSAVA-Global-Nutrition-Toolkit.pdf. Accessed July 8, 2022.</div><div><li class="rc-list__item reference-list-item" data-gtm-vis-has-fired37450158_104="1" style="box-sizing: inherit; line-height: 1.5; position: relative; margin-bottom: 0.5rem;"></li></div>
- <div>Olivry T, Mueller RS. Critically appraised topic on adverse food reactions of companion animals (5): discrepancies between ingredients and labeling in commercial pet foods. BMC Vet. Res. 2018;14:24.</div>
- <div>Fossati LA, Larsen JA, Villaverde C, et al. Determination of mammalian DNA in commercial canine diets with uncommon and limited ingredients. Vet. Med. Sci. 2019;5:30-38.</div>
Other articles in this issue
แบ่งปันบนโซเชียลมีเดีย