Canines Parvovirus
Geschrieben von Nicola Decaro
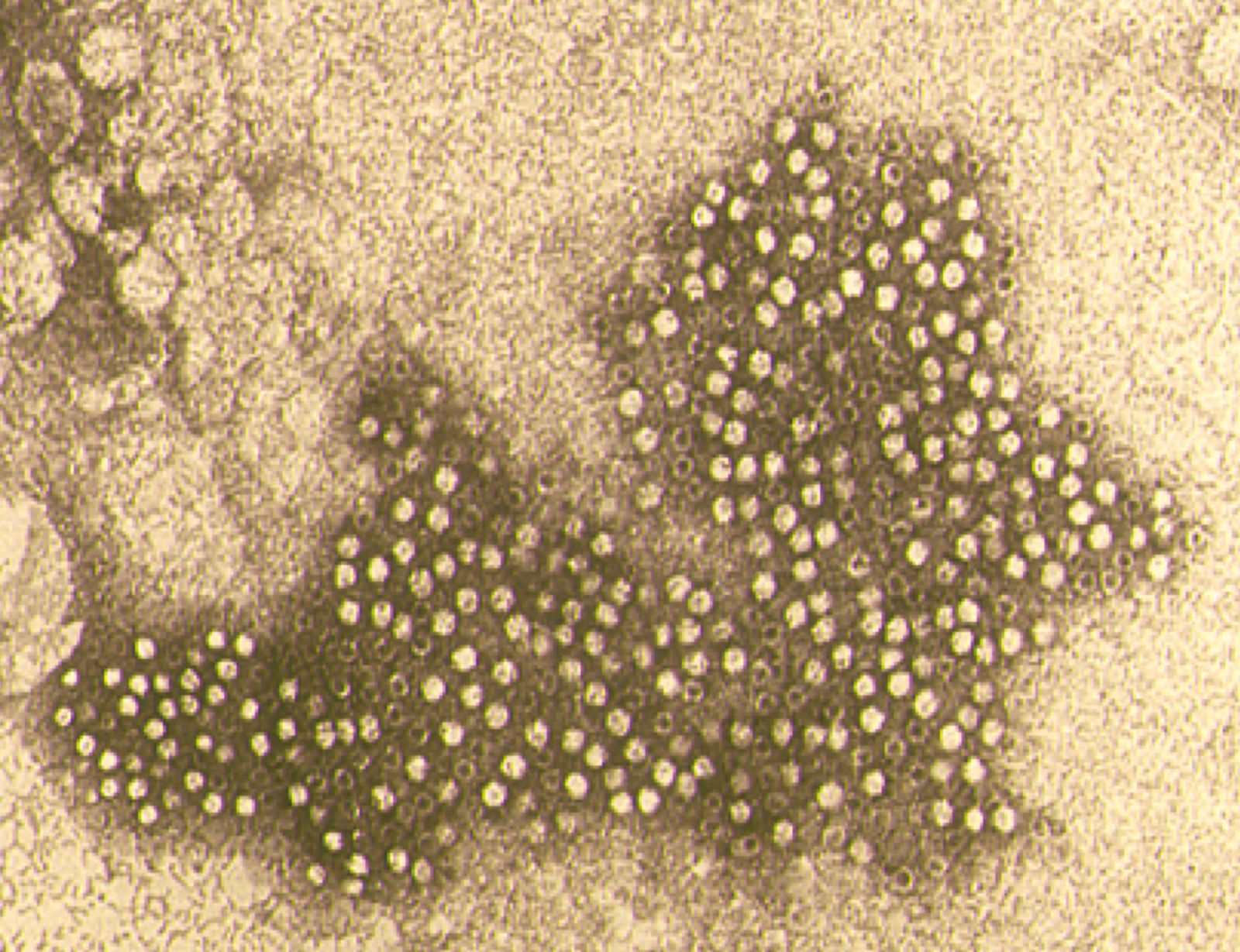
Das canine Parvovirus (CPV) ist ein kleines, unbehülltes Virus mit einem sphärischen Kapsid (zusammengesetzt aus den drei Proteinen VP1, VP2 und VP3). Das Kapsid enthält ein lineares Einzelstrang-DNA-Molekül, das für zwei nicht-strukturelle (NS1 und NS2) und zwei strukturelle (VP1 und VP2) Proteine kodiert.
Kernaussagen
Das canine Parvovirus ist der Haupterreger der akuten Gastroenteritis bei jungen Hundewelpen und kommt weltweit vor.
Drei antigene Varianten mit unterschiedlicher geographischer Verbreitung haben den ursprünglichen Stamm heute vollständig ersetzt.
Typische klinische Symptome sind Erbrechen, hämorrhagische Diarrhoe und Leukopenie. Die Mortalitätsraten erreichen bis zu 60-70 % in infizierten Zwingern und Tierheimen.
Diagnostische Assays für die Praxis haben eine geringe Sensitivität. Zur Bestätigung der Diagnose können zusätzliche Tests auf PCR-Basis erforderlich sein.
Die Behandlung besteht in erster Linie aus unterstützenden Therapiemaßnahmen, getestet werden aber auch verschiedene antivirale Wirkstoffe.
Die Impfung der Welpen ist nach wie vor die wirksamste Strategie zur Infektionskontrolle, trotz möglicher Interferenzen maternaler Antikörper und potenzieller Nichtübereinstimmungen („Mismatch“) zwischen Impfviren und Feldstämmen.
Einleitung
Das canine Parvovirus (CPV) ist ein kleines, unbehülltes Virus (Abbildung 1) mit einem sphärischen Kapsid (zusammengesetzt aus den drei Proteinen VP1, VP2 und VP3). Das Kapsid enthält ein lineares Einzelstrang-DNA-Molekül, das für zwei nicht-strukturelle (NS1 und NS2) und zwei strukturelle (VP1 und VP2) Proteine kodiert. VP2 ist das Hauptkapsidprotein und verantwortlich für die virale Antigenität [1] [2]. Erst vor kurzem wurde die Nomenklatur der Familie der Parvoviridae revidiert, wobei das CPV jetzt der Spezies „carnivores Protoparvovirus 1“ zugeordnet wird, ebenso wie das feline Panleukopenievirus (FPV) und andere verwandte carnivore Parvoviren [3].
Das CPV ist der Haupterreger der akuten Gastroenteritis bei Hundewelpen im Alter zwischen einem und sechs Monaten. Das Virus ist zwar schon seit den späten 1970er Jahren bekannt, aufgrund der Hochgradigkeit der klinischen Symptome und der Problematik der Interferenzen maternaler Antikörper mit der aktiven Immunisierung, die ein Impfprogramm beeinträchtigen können, stellt es aber auch heute noch eine große Bedrohung für junge Hunde dar [1] [2]. Ein weiteres Problem bei der Kontrolle dieser Erkrankung sind Feldvarianten (CPV-2a, CPV-2b, CPV-2c), deren Antigenität sich von der des ursprünglichen CPV-2-Stammes unterscheidet, der immer noch in den meisten kommerziellen Impfstoffen enthalten ist. CPV-2 und seine antigenen Varianten unterscheiden sich zwar lediglich in einigen wenigen Aminosäuren, es wird jedoch vermutet, dass die Impfung nur einen partiellen Schutz gewährt, der geimpfte Hunde nicht vor einer Infektion mit Feldstämmen zuverlässig schützt und sich gelegentlich sogar deutliche Krankheitssymptome entwickeln können [4] [5] [6]. Weitere Probleme, die in Angriff genommen werden müssen, sind das zunehmende Auftreten der klinischen Erkrankung bei adulten Hunden [4] [5] und die Fähigkeit der antigenen Varianten, auch Katzen zu infizieren, und bei diesen klinische Symptome hervorzurufen, die identisch sind mit denen der felinen Panleukopenie [7] [8]. Dieser Artikel konzentriert sich auf die klinischen, pathologischen und diagnostischen Aspekte der CPV-Infektion, ergänzt um einen kurzen Überblick über aktuelle epidemiologische Studien in verschiedenen Ländern und empfohlene Impfschemata.
Epidemiologie
Der ursprüngliche CPV-2-Stamm trat erstmals in den späten 1970er Jahren in Erscheinung. Wahrscheinlich handelte es sich um eine FPV-Wirtsvariante, die durch eine vorangegangene Adaptation in einer nicht bekannten wilden Carnivoren-spezies entstanden ist. In den frühen 1980er Jahren wurde das ursprüngliche Virus plötzlich ersetzt durch die beiden zwei allergenen Varianten CPV-2a und CPV-2b, die sich durch fünf oder sechs Aminosäuresubstitutionen im Kapsid-protein VP2 auszeichnen, und eine dritte Variante, CPV-2c, die im Jahr 2000 in Italien beschrieben wurde [9].
Der immer noch in den meisten Impfstoffen enthaltene ursprüngliche CPV-2-Stamm zirkuliert gegenwärtig nicht mehr im Feld, während die drei antigenen Varianten in unterschiedlicher Verteilung weltweit vorkommen. Im kontinentalen Europa kommen alle Varianten vor, wobei die Typen 2a und 2b in Portugal, Frankreich und Belgien überwiegen, die Typen 2a und 2c in Italien, Typ 2a in Osteuropa und Typ 2c auf der iberischen Halbinsel. In Deutschland sind alle drei Typen etwa gleich häufig verteilt. In Nordamerika kommt CPV-2b/2c sehr häufig vor und in Südamerika vorwiegend CPV-2a/2c. In Asien und auf isolierten Inseln wie Großbritannien, Australien und Japan dominieren die Typen 2a und 2b [1] [2]. Die wenigen Berichte aus Afrika weisen auf eine Co-Zirkulation der drei Stämme im Norden des Kontinentes hin und eine hohe Häufigkeit von CPV-2a und CPV-2b im Süden [10].
Das CPV ist in der Lage, domestizierte Hunde, Wölfe und andere wild lebende Carnivoren zu infizieren, bei denen häufig intermediäre Stämme zwischen CPV-2 und CPV-2a isoliert werden [11]. Der ursprüngliche CPV-2-Stamm kann feline Zellen in vitro infizieren, nicht aber in vivo. Die neuen antigenen Varianten sind dagegen in der Lage, auch Katzen in vivo zu infizieren und eine klinische Erkrankung zu induzieren, die nicht von der felinen Panleukopenie zu unterscheiden ist [7] [8]. Theoretisch gibt es gegenüber einer CPV-Infektion zwar keine besonderen rassespezifischen Empfindlichkeiten, große Rassen wie der Deutsche Schäferhund, der Labrador, der Rottweiler, der Alaskan Malamute und der Dobermann scheinen jedoch ein höheres Erkrankungsrisiko zu tragen. Eine mögliche Ursache hierfür könnte jedoch darin liegen, dass die Konzentrationen maternaler Antikörper bei Welpen schnell wachsender, großer Hunderassen schneller absinken als bei Welpen kleinerer Hunderassen [1] [2]. CPV-Infektionen und die entsprechenden klinischen Erkrankungen treten zwar überwiegend bei Welpen unter sechs Monaten auf, zunehmend häufig werden aber auch bei adulten Hunden hochgradige klinische Symptome beschrieben, die oft im Zusammenhang mit einer CPV-2c-Infektion stehen [5] [6].
Hauptquelle für die Kontamination der Umwelt mit dem caninen Parvovirus sind die Fäzes infizierter Welpen. In der Umwelt ist das Virus außergewöhnlich stabil und kann über mehrere Wochen oder sogar Monate infektiös bleiben. Immunologisch naive Welpen werden auf oronasalem Weg über direkten oder indirekten Kontakt infiziert [1] [2].
Pathogenese
Das Zielgewebe für die virale Replikation sind die intestinalen Krypten und lymphatische Organe, das Virus kann sich aber in sämtliche Gewebe ausbreiten. Nach Eintritt in den Körper des Tieres repliziert das CPV primär im lymphatischen Gewebe des Oropharynx, des Thymus, der mesenterialen Lymphknoten und der Peyer‘schen Platten. Dort verursacht es eine ausgedehnte Nekrose, bevor es hauptsächlich über infizierte Lymphozyten in den Blutkreislauf übertritt. Die Virämie hält sehr lange Zeit an (mittels Echtzeit-PCR kann das Virus bis zu 60 Tage nachgewiesen werden) und führt zu einer Besiedelung der Dünndarmkrypten, in denen die aktive Virusreplikation eine schnelle Lysis epithelialer Stammzellen induziert. Die direkte Folge ist eine Beeinträchtigung des Turnovers des Epithels der Zottenspitzen, die zur Entstehung einer Diarrhoe führt. Die Virusausscheidung über die Fäzes beginnt zwei bis drei Tage nach der Infektion und dauert bis zu 45-50 Tage an. Hohe Virustiter sind jedoch nur innerhalb der ersten sieben bis zehn Tage nachweisbar. Bei neugeborenen Welpen (2-3 Wochen alt) kann sich das CPV auch in aktiv replizierenden Herzmuskelzellen reproduzieren und eine hochgradige Myokarditis hervorrufen, wobei diese Form gegenwärtig nur sporadisch beobachtet wird [1] [2]. Im Vergleich zum ursprünglichen Typ-2 zeigen die antigenen Varianten eine höhere Pathogenität, eine kürzere Inkubationszeit (weniger als 4-5 Tage), hochgradigere klinische Symptome, eine hochgradigere und länger andauernde Virusausscheidung und eine geringere erforderliche virale Minimaldosis für eine Infektion bei Hunden [12]. Begleitende Infektionen mit caninen Coronaviren (CCoV) können die klinischen Symptome verstärken, wobei das CPV das Epithel der Darmkrypten infiziert, während das CCoV das Epithel der Zottenspitzen infiziert [1] [2].
Klinische Symptome und Pathologie
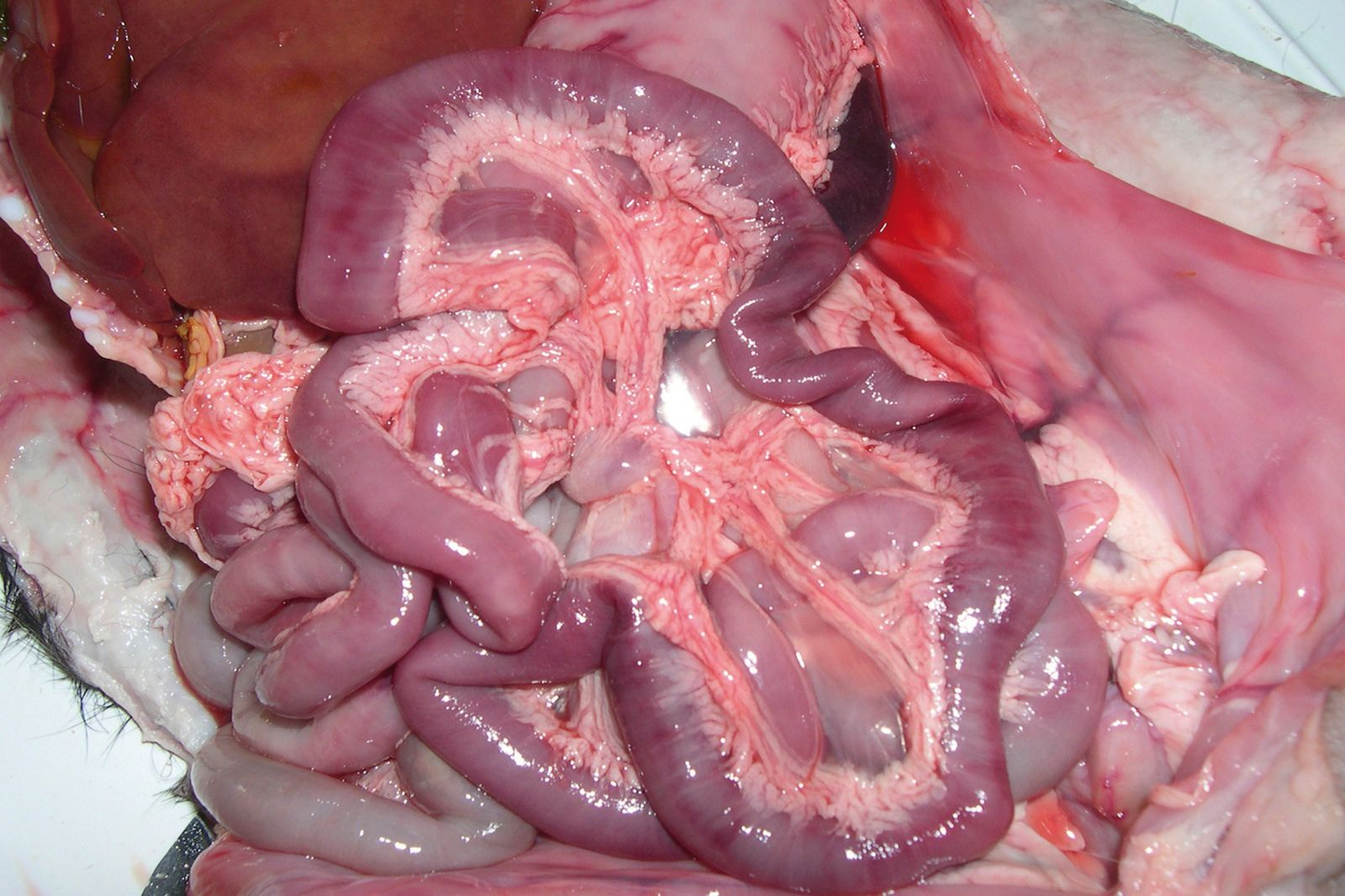
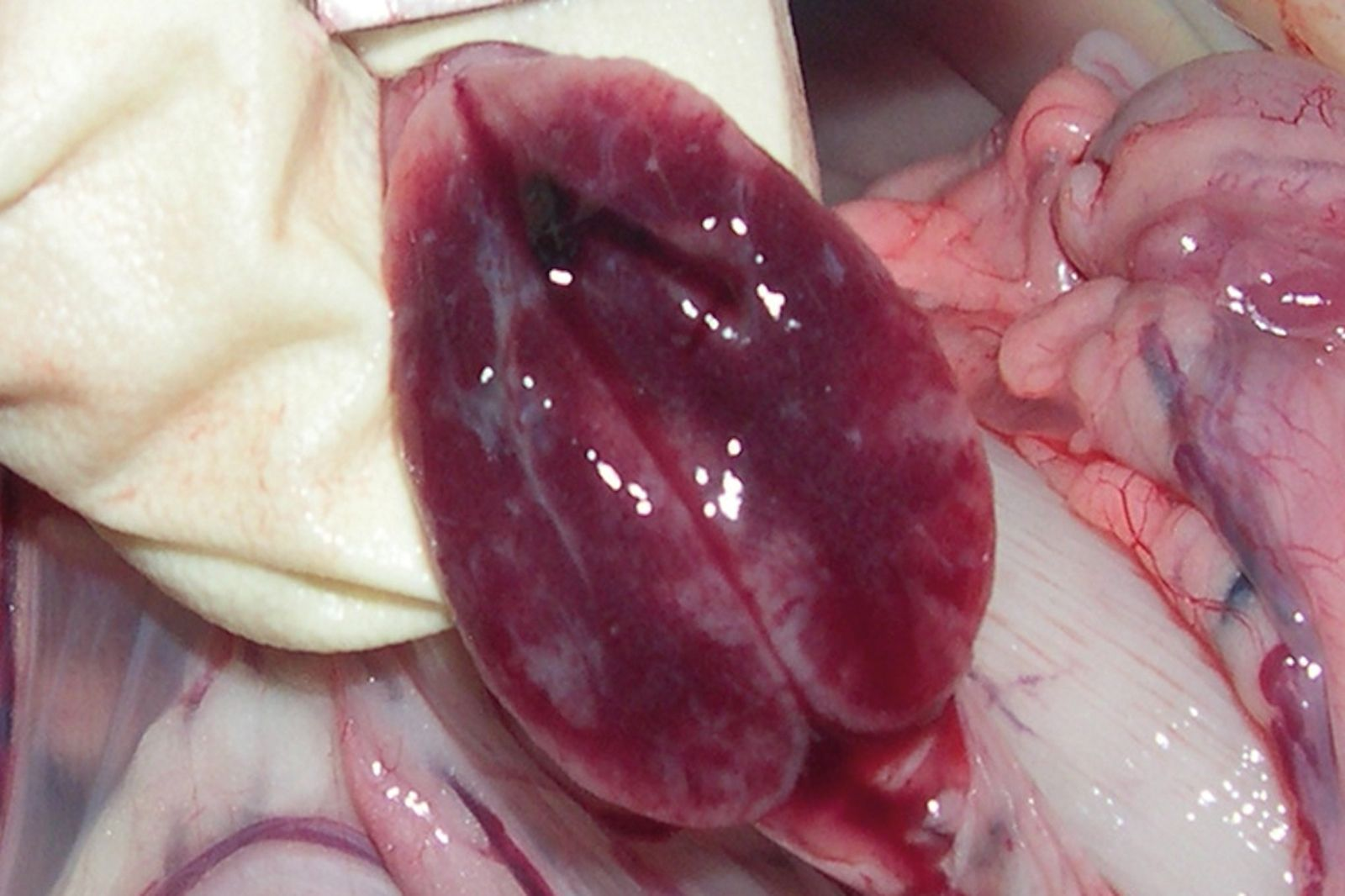
Hundewelpen, die aufgrund einer CPV-Enteritis sterben, sind in der Regel extrem dehydriert. Bei der Sektion fallen makroskopische Veränderungen im Magendarmtrakt auf, die hauptsächlich das Duodenum und an zweiter Stelle das Jejunum umfassen. Der häufigste Befund ist eine hämorrhagische Gastroenteritis (Abbildung 2). Die Darmwand ist dabei in der Regel verdickt und segmental verfärbt. Die Serosaoberfläche kann dunkelrot oder violett verfärbt und von Fibrin überzogen sein. Das Darmlumen kann vollständig leer sein oder dunkles (oft blutiges) Material oder hämorrhagische Flüssigkeit enthalten. Die mesenterialen Lymphknoten und die Peyer’schen Platten sind vergrößert und gestaut, oft mit über die Cortex und Schnittflächen verstreuten Blutungen (Abbildung 3). Histopathologisch findet man im Dünndarmgewebe eine multifokale Nekrose der Krypten und intrazelluläre Einschlusskörperchen, sowie eine ausgedehnte Lymphozytendepletion in den Peyer’schen Platten, den Lymphknoten, der Milz und im Thymus. Im Falle bakterieller Komplikationen können bei der Sektion auch ein Lungen-ödem und eine Alveolitis auffallen [1] [2].
Myokardiale Form
Akute Myokarditis war ein häufiger Befund während der ersten weltweiten epizootischen Seuchenzüge des CPV, in denen die Erkrankung auf eine immunologisch naive Hundepopulation traf. Heute wird diese Form im Feld jedoch nur noch sporadisch beobachtet. Eine CPV-induzierte Myokarditis kann in der Tat nur bei Welpen in einem Alter von unter drei bis vier Wochen auftreten, in dem sich das myokardiale Synzytium aktiv repliziert und entsprechend anfällig ist für die Virusreplikation. Da heute jedoch die Mehrzahl der Hündinnen geimpft ist (oder dem Virus ausgesetzt war) und folglich eine starke Immunantwort entwickelt hat, erhalten nahezu alle Welpen maternale Antikörper, die sie während ihrer ersten Lebenswochen vor Parvovirusinfektionen schützen.
Typisches Kennzeichen einer CPV-Myokarditis ist der plötzliche Tod infizierter Welpen. In einigen Fällen gehen dem Tod gastrointestinale Symptome und eine kurze Periode mit Dyspnoe, Schreien und Würgen voraus. Einige betroffene Tiere können klinisch gesund sein, so dass Hinweise auf eine Erkrankung des Herzens nur im EKG erkennbar sind. Diese Hunde sind prädisponiert für eine degenerative Herzerkrankung, die Wochen oder Monate später in der Entwicklung einer Herzinsuffizienz münden kann. Welpen, die sich von einer CPV-Myokarditis erholen, entwickeln in der Regel eine Myokardfibrose. Hunde, die aufgrund der myokardialen Form sterben, sind oft in gutem Allgemeinzustand, und bei der Sektion dieser Patienten ist ein Lungenödem gelegentlich der einzige makroskopisch erkennbare Befund. In anderen Fällen zeigt das Herz schlaffe Wände und erweiterte Kammern mit blassen, nekrotischen Bezirken an der Oberfläche (Abbildung 4). Histopathologisch handelt es sich um eine nichteitrige Myokarditis mit multifokaler Infiltration von Lymphozyten und Plasmazellen und intranukleären Einschlusskörperchen [1] [2].

Diagnostisches Vorgehen
Die Diagnose einer CPV-Infektion basiert häufig lediglich auf dem Nachweis einer faulig riechenden, blutigen Diarrhoe. Dabei ist jedoch zu berücksichtigen, dass ähnliche Symptome auch durch andere pathogene Erreger hervorgerufen werden können und dass CPV-assoziierte Diarrhoen in vielen Fällen auch nicht-hämorrhagischer Natur sind. Um eine CPV-Infektion endgültig zu bestätigen bzw. sicher auszuschließen, ist deshalb immer eine Labordiagnose erforderlich [1] [2].
Klinische Diagnose
Erbrechen und hämorrhagische Diarrhoe im Angesicht einer akuten Leukopenie führt zum starken Verdacht einer CPV-Infektion. Wichtige Differenzialdiagnosen sind jedoch Staupe, infektiöse canine Hepatitis, Darmparasitosen und weitere Erkrankungen des Gastrointestinaltraktes. Das canine Coronavirus (CCoV) ruft in der Regel nicht-hämorrhagische Enteritiden hervor, es kann unter bestimmten Bedingungen aber auch zu hämorrhagischer Diarrhoe führen, und hypervirulente Stämme (pantropes CCoV) können auch zu einer systemischen Erkrankung und Leukopenie führen [13].
Behandlung
Management
Impfung
Interferenz maternaler Antikörper
Das Hauptproblem bei der CPV-Impfung sind die maternalen Antikörper, die Welpen vor einer Infektion mit Feldstämmen schützen, aber mit der aktiven Immunisierung interferieren.
Der Titer maternaler Antikörper bei einem Welpen ist abhängig von den Antikörperleveln im Serum der Hündin und der Menge der vom Welpen aufgenommenen Kolostralmilch. So können Welpen derselben Hündin unterschiedliche Konzentrationen maternaler Antikörper aufweisen und daher in unterschiedlichem Alter empfänglich für eine CPV-Infektion (und eine aktive Immunisierung) sein. Werden Welpen mit hohen Titern maternaler Antikörper (HI-Titer > 1:20) geimpft, kann die Serokonversion aufgrund der Zerstörung der Impfviren durch kolostrale Antikörper ausbleiben. Da jedoch nur HI-Titer ≥ 1:80 als protektiv gegen eine Infektion durch Feldstämme gelten, entsteht eine in der Regel zwei bis drei Wochen andauernde kritische Periode – die sogenannte „Impfschutzlücke“– während der die Welpen noch nicht geimpft werden können, aber bereits anfällig sind für die Infektion und die Entwicklung der klinischen Erkrankung.
Um eine Interferenz mit der aktiven Immunisierung zu vermeiden, sollten Welpen erst nach erfolgter Abnahme der maternalen Antikörper geimpft werden [1] [2]. Zur Vermeidung von Interferenzen mit maternalen Antikörpern werden verschiedene Strategien vorgeschlagen, einschließlich der Verwendung hochtitriger Impfstoffe und intranasaler Impfungen [25]. Wiederholte intranasale Applikationen monovalenter CPV-Impfstoffe führten zu einer erfolgreichen Eradikation des Virus in infizierten Zwingern (persönliche Beobachtung).
Die Richtlinien der World Small Animal Veterinary Association [26] empfehlen, dass eine Grundimmunisierung gegen CPV nicht vor der 14.-16. Lebenswoche enden soll, um einen Impfschutz auch bei Welpen mit lang anhaltenden Titern maternaler Antikörper zu gewährleisten. Das empfohlene Impfschema umfasst drei CPV-Impfungen innerhalb des ersten Lebensjahres und eine Auffrischungsimpfung nach einem Jahr, gefolgt von weiteren Auffrischungen alle drei Jahre [1].
CPV-2-Impfstoffe und Kreuzschutz mit den antigenen Varianten
Die Hauptursache einer aktiven CPV-Zirkulation unter geimpften Tieren ist zwar die oben angesprochene Impfschutzlücke, es gibt darüber hinaus aber auch Zweifel hinsichtlich einer vollständigen Wirksamkeit von Typ-2-basierten Impfstoffen gegen die neueren antigenen Varianten [4] [5] [6]. Die meisten kommerziell erhältlichen Impfstoffe werden mit dem alten CPV-2-Stamm hergestellt, der heute im Feld nicht mehr zirkuliert. Studien zeigen das Ausbleiben einer vollständigen Neutralisation von CPV-Feldstämmen durch Antikörper, die gegen dieses Impfvirus gebildet werden. Inzwischen gibt es einige wenige zugelassene Impfstoffe mit der CPV-2b-Variante, und es wäre wünschenswert, weitere Impfstoffe mit der neuen CPV-2c-Variante zu entwickeln, auch wenn die drei antigenen Varianten in der Lage sind, eine wirksame gegenseitige Kreuzneutralisation zu induzieren [4].
Nicola Decaro
DVM, PhD
Italien
Dr. Decaro schloss sein Tiermedizinstudium an der Universität Bari in Italien ab und promovierte (PhD) an der Universität Utrecht in den Niederlanden. Zurzeit ist er Associate Professor für Infektionskrankheiten der Tiere an der veterinärmedizinischen Fakultät der Universität Bari. Dr. Decaro ist Mitherausgeber des Journal of Virological Methods, Redaktionsmitglied bei mehreren internationalen Fachzeitschriften sowie Autor und Co-Autor zahlreicher in internationalen Fachzeitschriften veröffentlichter Artikel. Sein Hauptinteresse gilt Virusinfektionen bei Carnivoren und Wiederkäuern.
[Literatur]
- Greene CE, Decaro, N. Canine viral enteritis. In: Greene CE, ed. Infectious Diseases of the Dog and Cat, 4th ed. St. Louis: Elsevier Saunders, 2012;67-80.
- Decaro N, Buonavoglia C. Canine parvovirus – A review of epidemiological and diagnostic aspects, with emphasis on type 2c. Vet Microbiol 2012;155:1-12.
- ICTV Virus Taxonomy 2015. Available at: http://ictvonline.org/virusTaxonomy.asp. Accessed Sep 11, 2015.
- Cavalli A, Martella V, Desario C, et al. Evaluation of the antigenic relationships among canine parvovirus type 2 variants. Clin Vaccine Immunol 2008;15:534-539.
- Decaro N, Desario C, Elia G, et al. Evidence for immunisation failure in vaccinated adult dogs infected with canine parvovirus type 2c. New Microbiol 2008;31:125-130.
- Decaro N, Cirone F, Desario C, et al. Severe parvovirus in a 12-year-old dog that had been repeatedly vaccinated. Vet Rec 2009;164:593-595.
- Decaro N, Buonavoglia D, Desario C, et al. Characterisation of canine parvovirus strains isolated from cats with feline panleukopenia. Res Vet Sci 2010;89:275-278.
- Decaro N, Desario C, Amorisco F, et al. Canine parvovirus type 2c infection in a kitten associated with intracranial abscess and convulsions. J Feline Med Surg 2011;13:231-236.
- Buonavoglia C, Martella V, Pratelli A, et al. Evidence for evolution of canine parvovirus type-2 in Italy. J Gen Virol 2001;82:1555-1560.
- Dogonyaro BB, Bosman AM, Sibeko KP, et al. Genetic analysis of the VP2-encoding gene of canine parvovirus strains from Africa. Vet Microbiol 2013;165:460-465.
- Allison AB, Harbison CE, Pagan I, et al. Role of multiple hosts in the cross-species transmission and emergence of a pandemic parvovirus. J Virol 2012;86:865-872.
- Decaro N, Buonavoglia C. Parvovirosi del cane. In: Bo S., ed. Manuale di Malattie Infettive del Cane e del Gatto. Milan, Abbiategrasso 2014;38-48.
- Decaro N, Buonavoglia C. Canine coronavirus: not only an enteric pathogen. Vet Clin North Am Small Anim Pract 2011;38:799-814.
- Decaro N, Martella V, Elia G, et al. Tissue distribution of the antigenic variants of canine parvovirus type 2 in dogs. Vet Microbiol 2007;121:39-44.
- Decaro N, Desario C, Beall M.J, et al. Detection of canine parvovirus type 2c by a commercially available in-house rapid test. Vet J 2010;184:373-375.
- Decaro N, Desario C, Billi M, et al. Evaluation of an in-clinic assay for the diagnosis of canine parvovirus. Vet J 2013;98:504-507.
- Desario C, Decaro N, Campolo M, et al. Canine parvovirus infection: which diagnostic test for virus? J Virol Methods 2005;121:179-185.
- Decaro N, Elia G, Martella V, et al. A real-time PCR assay for rapid detection and quantitation of canine parvovirus type 2 DNA in the feces of dogs. Vet Microbiol 2005;105:19-28.
- Decaro N, Elia G, Martella V, et al. Characterisation of the canine parvovirus type 2 variants using minor groove binder probe technology. J Virol Methods 2006;133:92-99.
- Decaro N, Elia G, Desario C, et al. A minor groove binder probe real-time PCR assay for discrimination between type 2-based vaccines and field strains of canine parvovirus. J Virol Methods 2006;136:65-70.
- Decaro N, Martella V, Elia G, et al. Diagnostic tools based on minor groove binder probe technology for rapid identification of vaccinal and field strains of canine parvovirus type 2b. J Virol Methods 2006;138:10-16.
- Decaro N, Desario C, Elia G, et al. Occurrence of severe gastroenteritis in pups after canine parvovirus vaccine administration: a clinical and laboratory diagnostic dilemma. Vaccine 2007;25:1161-1166.
- Decaro N, Crescenzo G, Desario C, et al. Long-term viremia and fecal shedding in pups after modified-live canine parvovirus vaccination. Vaccine 2014;32:3850-3853.
- Mohr AJ, Leisewitz AL, Jacobsion LS, et al. Effect of early enteral nutrition on intestinal permeability, intestinal protein loss, and outcome in dogs with severe parvoviral enteritis. J Vet Int Med 2003;17:791-798.
- Martella V, Cavalli A, Decaro N, et al. Immunogenicity of an intranasally administered modified live canine parvovirus type 2b vaccine in pups with maternally derived antibodies. Clin Diagn Lab Immunol 2005;12:1243-1245.
- Day MJ, Horzinek MC, Schultz RD. WSAVA guidelines for the vaccination of dogs and cats. J Small Anim Pract. 2010;51(6):1-32.
Andere Artikel in dieser Ausgabe
Auf sozialen Medien teilen