Toxoplasmosis felina
Escrito por Christopher Fernandez-Prada y Victoria Wagner
Actualmente se sabe que la toxoplasmosis presenta una distribución mundial y, aunque el gato es el único hospedador definitivo, se trata de un parásito que puede tener implicaciones significativas tanto para la salud humana como para la salud animal.
Article

Puntos clave
La infeccin por Toxoplasma gondii es frecuente en gatos de todo el mundo, pero la mayora permanecen asintomticos.
Las personas se pueden infectar por T. gondii mediante la ingestin de ooquistes (p. ej., alimentos, tierra y agua contaminada) o de quistes en tejidos (carne poco cocinada).
La identificacin de ooquistes de T. gondii en las heces del gato como nica prueba diagnstica no est recomendada debido al corto periodo de eliminacin y a la similitud con otros parsitos.
Los ooquistes necesitan un mnimo de 24 horas tras ser eliminados para ser infecciosos, por lo que la limpieza diaria del arenero es una estrategia eficaz para prevenir la transmisin en el hogar.
Introducción
Toxoplasma gondii es un parásito protozoario intracelular que puede infectar a la mayoría de las especies de animales vertebrados y, aunque los félidos son los únicos hospedadores definitivos, cada vez se reconoce más su importancia al suponer una amenaza para muchos ecosistemas. La ingestión del parásito, ya sea por parte del hospedador definitivo o del intermediario, suele terminar provocando una infección crónica subclínica o asintomática; sin embargo, en individuos susceptibles o no inmunocompetentes, la toxoplasmosis puede provocar abortos y fallos reproductivos, o incluso fallo orgánico y muerte [1]. Actualmente la toxoplasmosis presenta una distribución mundial; la prevalencia de eliminación de ooquistes en gatos varía entre el 0,7-41%, en función de los diferentes países. En Estados Unidos la seroprevalencia de anticuerpos frente a T. gondii en gatos oscila entre el 14-100% [2]. Aunque también hay muchas personas infectadas (p. ej., en Estados Unidos unos 40 millones), la mayoría son asintomáticas, pero algunas de ellas, especialmente las inmunodeprimidas, pueden presentar problemas oculares o neurológicos [3].
Ciclo biológico de Toxoplasma gondii
Toxoplasma gondii tiene un ciclo biológico complejo que requiere un hospedador definitivo y un hospedador intermediario para completar el ciclo sexual y el ciclo asexual respectivamente (Figura 1). Este parásito se puede presentar en tres formas diferentes: taquizoíto, bradizoíto y esporozoíto (contenidos en ooquistes) y todas ellas pueden ser infecciosas para el ser humano. Los taquizoítos son formas parasitarias del ciclo asexual que se multiplican rápidamente y se pueden encontrar en los tejidos de cualquier hospedador vertebrado. Los bradizoítos también son ubicuos y pueden encontrarse en los tejidos del hospedador, pero estas formas se multiplican lentamente y forman quistes.
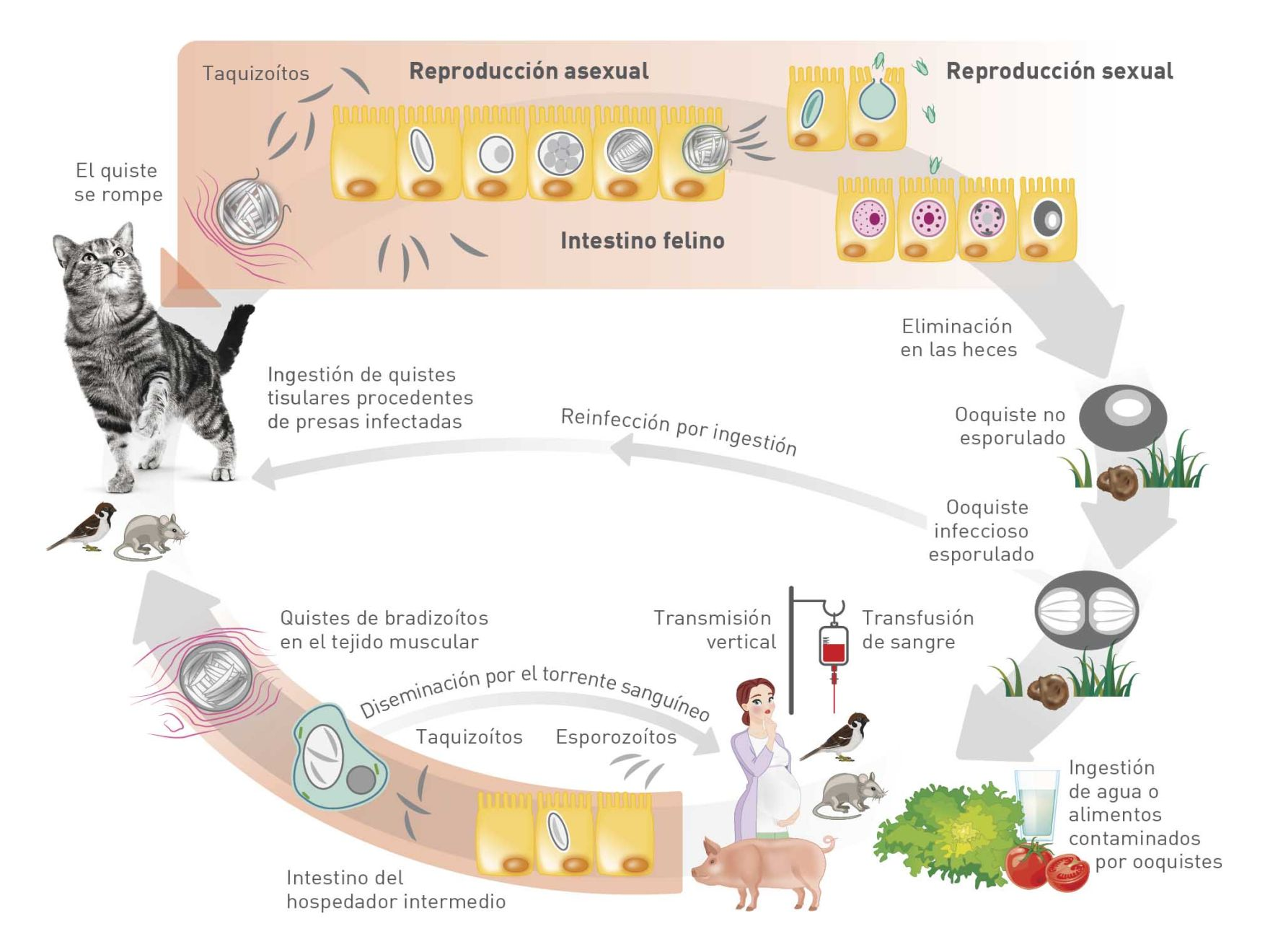
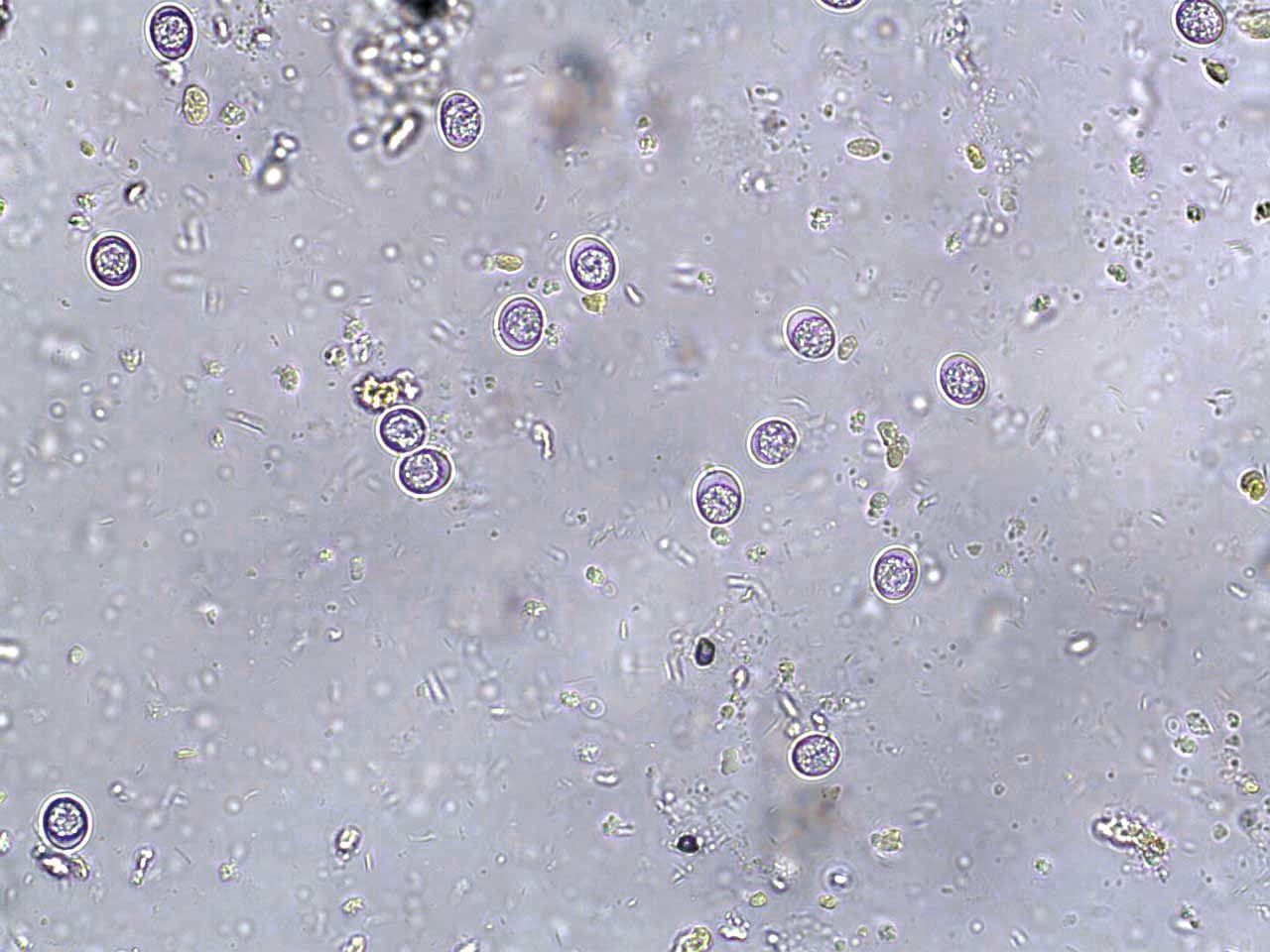
El gato, que es el hospedador definitivo de T. gondii, se infecta mediante la ingestión de quistes presentes en los tejidos (p. ej., de presas que cazan y comen) (Figura 2) o de ooquistes esporulados o infecciosos (procedentes de la tierra, agua o plantas contaminadas con heces de un gato infectado). Este parásito se puede reproducir sexualmente en el gato, de manera que una vez que se ha infectado con bradizoítos u ooquistes, empezará a eliminar ooquistes en sus heces entre 3-10 días o 19-48 días después, respectivamente, y podrá seguir eliminado ooquistes incluso 2 semanas más (Figura 3) [2],[4]. Los ooquistes esporulan y se vuelven infecciosos 1-5 días después de su eliminación y son extremadamente resistentes en el medio ambiente.

Las principales vías de infección en las personas son la ingestión de quistes presentes en la carne poco cocinada y la ingestión de ooquistes a través de la contaminación fecal de alimentos, las manos o cualquier material [4],[5].
Signos clínicos de toxoplasmosis felina
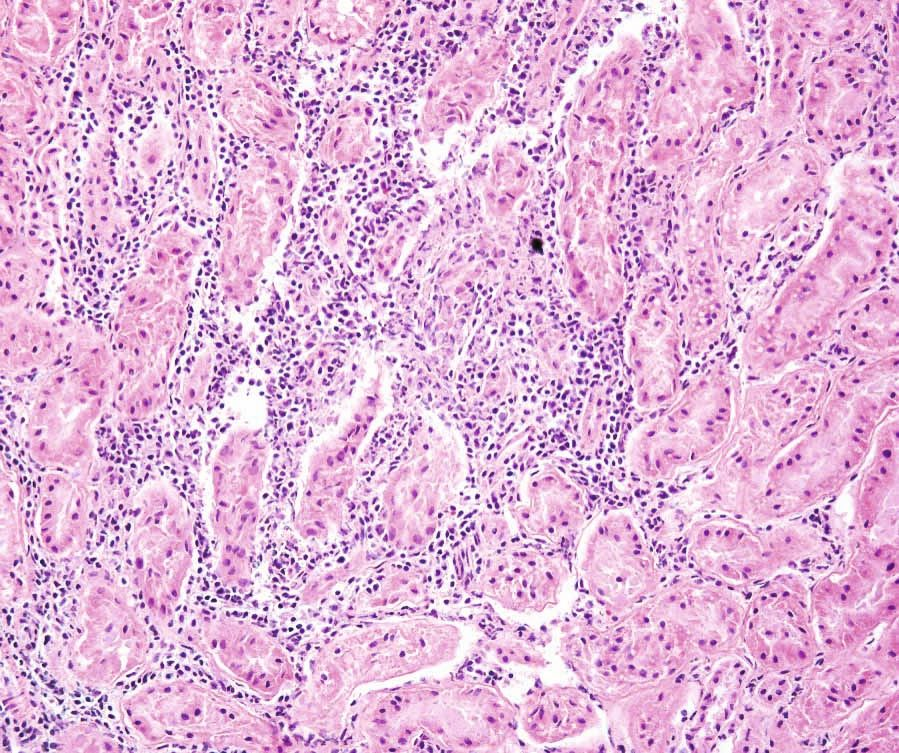
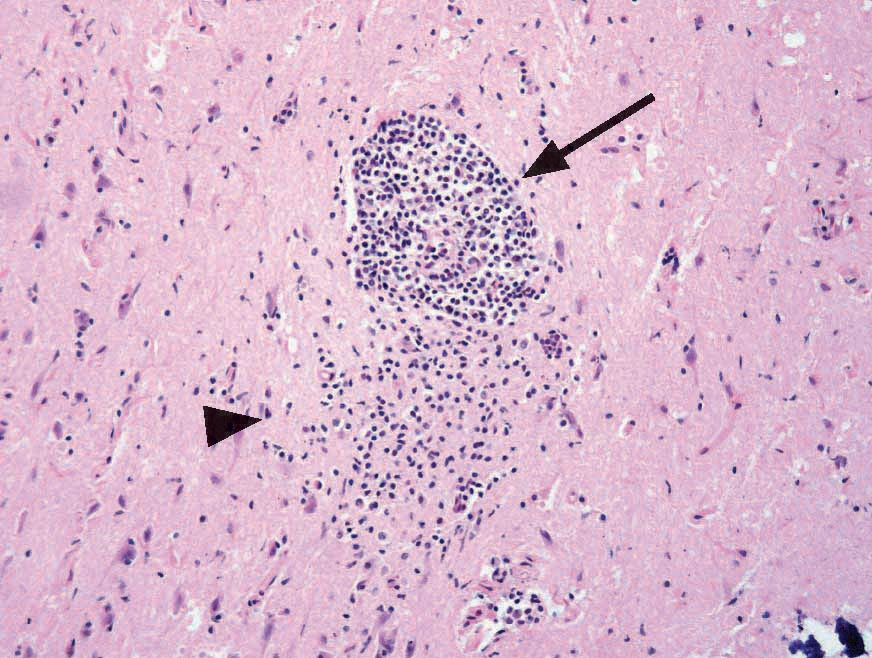
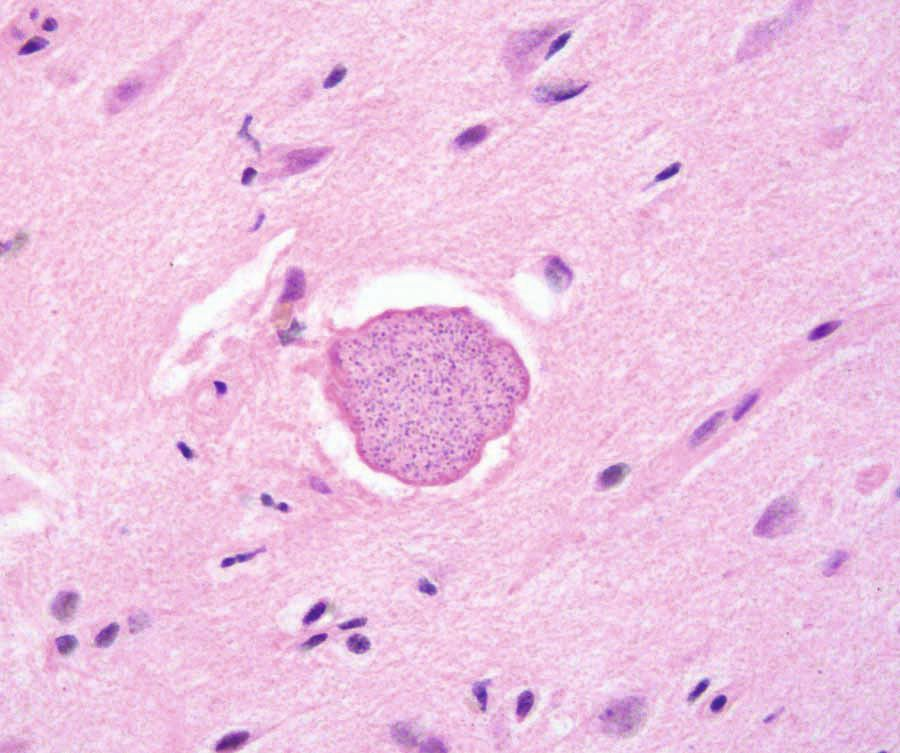
La toxoplasmosis puede ser difícil de identificar en los gatos, ya que la mayoría de las infecciones son asintomáticas. En caso de presentar signos clínicos, los más frecuentes son la fiebre, la anorexia y la letargia. El crecimiento intracelular de los taquizoítos produce efectos citopáticos directos, inflamación y necrosis celular, por lo que se pueden observar otros signos más específicos dependiendo de la localización de los taquizoítos en el organismo (Figuras 4-6); por ejemplo, signos oculares, neurológicos, neumonía e ictericia [4]. El virus de la leucemia felina, el virus de la inmunodeficiencia felina, las neoplasias y la administración de fármacos inmunosupresores (especialmente la ciclosporina) son factores de riesgo para el desarrollo de la enfermedad clínica. Las infecciones agudas, especialmente en gatitos, suelen ser mortales [6].
Diagnóstico
Obtener un diagnóstico fiable de toxoplasmosis puede resultar complicado. Las alteraciones hematológicas presentes en gatos infectados pueden incluir anemia no regenerativa, leucocitosis, linfocitosis, monocitosis y eosinofilia. En las infecciones graves también se puede observar leucopenia; particularmente, neutropenia con desviación degenerativa a la izquierda. Los hallazgos de la bioquímica sérica y análisis de orina dependen de los órganos afectados [6].
La detección de ooquistes de T. gondii en heces no está recomendada como única herramienta de diagnóstico, debido al corto periodo de eliminación de ooquistes en las heces del gato, así como a la similitud microscópica de los ooquistes de T. gondii con otros parásitos [4],[7]. Además, la identificación de ooquistes en heces no se correlaciona con el desarrollo de la enfermedad clínica en el gato [2]. En su lugar, para obtener un diagnóstico ante mortem definitivo están recomendadas las pruebas serológicas, en donde los títulos elevados de IgM (> 1:256) generalmente son compatibles con una infección reciente por T. gondii. Como alternativa, se pueden utilizar los títulos de IgG de muestras pareadas (tomadas con un intervalo de 2-4 semanas entre una uy otra), aunque la interpretación de los resultados puede ser compleja (Tabla 1) [1],[2]. Algunos gatos también pueden presentar una infección crónica por T. gondii, en la que los quistes de los tejidos se rompen y liberan bradizoítos a la circulación; estos episodios pueden o no estar asociados a la eliminación de ooquistes, dependiendo del estado inmunitario del animal a nivel individual [8].
En gatos sanos no es recomendable realizar pruebas de anticuerpos frente a T. gondii [6] ya que en esta especie, las pruebas serológicas no indican con precisión la eliminación de ooquistes y la mayoría de los gatos que eliminan activamente ooquistes en realidad son seronegativos en ese momento [2].
Tabla 1. Interpretación de los resultados de la serología IgG de T. gondii [6].
| Resultado serológico | Interpretación/análisis |
|---|---|
| Incremento del título entre muestras séricas pareadas ≥ 4 veces | Verdadero positivo (infección reciente/activa) |
| Incremento del título en muestras de suero pareadas < 4 veces | Verdadero negativo (ninguna infección reciente/activa) o falso negativo (infección recurrente) |
| Un único resultado positivo elevado (p.ej., 1:1000) | Presencia de quistes de bradizoítos en tejidos |
La toxoplasmosis es una infección que puede ser difícil de identificar en el gato, ya que en la mayoría de los casos es asintomática; los signos clínicos más frecuentes, en caso de presentarse, son fiebre, anorexia y letargia.
Tratamiento y pronóstico
No hay fármacos autorizados para el tratamiento de la toxoplasmosis felina, pero en los casos agudos o cuando la infección se ha diseminado, la clindamicina es el fármaco de elección (10-12,5 mg/kg PO cada 12h hasta 4 semanas de duración), en combinación con el tratamiento de apoyo adecuado [6]. Para disminuir la eliminación de ooquistes, se puede administrar pirimetamina (0,25-0,5 mg/kg PO cada 12h hasta 4 semanas de duración) o una sulfonamida (15-30 mg/kg PO cada 12h hasta 4 semanas de duración), lo que generalmente resulta beneficioso durante la fase aguda de la infección, aunque es raro que sean eficaces eliminando la infección. Otra opción es utilizar la combinación trimetoprim-sulfonamida (15 mg/kg PO q12h durante 4 semanas) [2] y también se puede considerar la administración de fármacos que actúan frente a coccidios (p. ej., toltrazuril, ponazuril). Cabe destacar que ningún tratamiento ha demostrado ser significativamente eficaz frente a los bradizoítos infectivos[1].
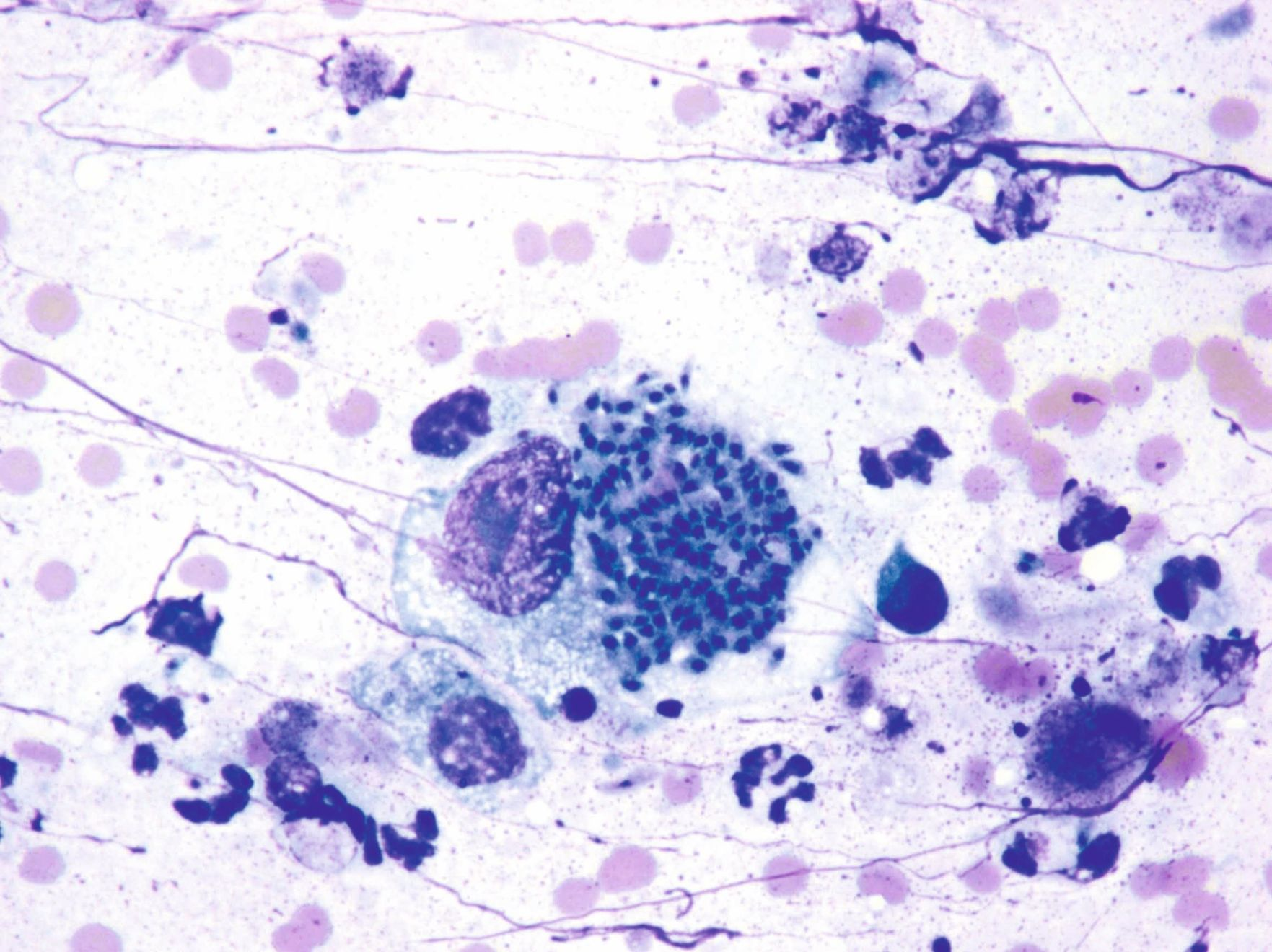
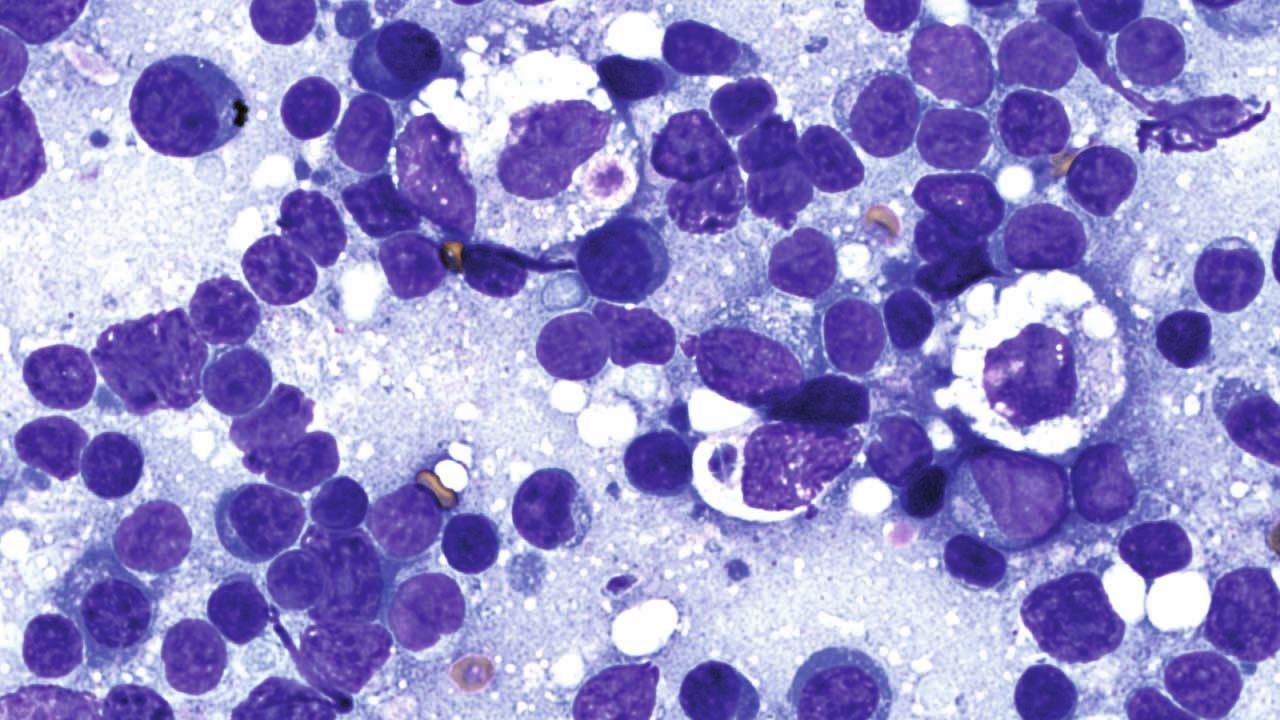
Hay varios factores que influyen en el pronóstico de los gatos con signos clínicos de toxoplasmosis; por ejemplo, los sistemas/órganos afectados (Figuras 7 y 8) y el tiempo transcurrido entre la infección y el inicio del tratamiento. Por lo general, si se observa una mejoría en los signos clínicos a los 2-3 días de iniciar el tratamiento, el pronóstico es más favorable, pero si la infección afecta a los pulmones o el hígado, el pronóstico asociado es malo [4].
Implicaciones zoonóticas
Las personas pueden adquirir la infección por T. gondii mediante la ingestión de alimentos o agua contaminados con ooquistes, quistes tisulares en carne poco cocinada y mediante transfusiones de sangre, trasplantes de órganos, aunque también puede ser congénita. La mayoría de las infecciones son asintomáticas, aunque ocasionalmente se han descrito signos como fiebre, linfadenopatía y malestar general. Sin embargo, T. gondii representa un grave riesgo para la salud del feto durante el embarazo; la toxoplasmosis congénita puede causar graves daños oculares y/o neurológicos cuando los taquizoítos migran por vía transplacentaria y alcanzan al feto [1]. Aunque generalmente los bebés no presentan ningún signo al nacer, más adelante pueden sufrir alteraciones graves de la visión, convulsiones u otros problemas nerviosos [9]. Además, las personas inmunocomprometidas de cualquier edad tienen el riesgo de desarrollar toxoplasmosis sintomática, que afecta al cerebro, los pulmones y/u otros órganos vitales [5].
En los gatos sanos no está recomendado realizar pruebas de anticuerpos frente a T. gondii; las pruebas serológicas no son precisas como indicadores de la eliminación de ooquistes, y la mayoría de los gatos son seronegativos cuando están eliminando activamente ooquistes.
Cada vez se tiene más constancia en todo el mundo de la contaminación del suelo y las aguas subterráneas con ooquistes de Toxoplasma. En una revisión de 22 estudios se concluyó que este es un motivo de gran preocupación, ya que el vertido de heces de gatos infectados que contamina masas de agua es considerable [3]. La contaminación del océano es responsable de la infección y muerte de varios mamíferos marinos, como focas, ballenas, delfines y nutrias marinas [10],[11]. El agua potable también tiene riesgo de contaminación; tirar los excrementos de gato por el inodoro ha contribuido a la aparición de varios brotes de toxoplasmosis humana en varios países [12],[13].
Los ooquistes son muy resistentes y pueden sobrevivir y permanecer infecciosos durante años, incluso en condiciones subóptimas [14]. Además, los ooquistes necesarios para infectar a una persona probablemente sean pocos; en estudios con cerdos se ha demostrado que solo un ooquiste es suficiente para inducir la infección [15]. Por ello, es esencial tomar medidas para eliminar las heces de los gatos de forma responsable.
A diferencia de la creencia popular, el contacto directo con los gatos no es un factor de riesgo significativo para la infección humana por Toxoplasma gondii [16]. Sin embargo, la limpieza diaria de la bandeja de arena es una estrategia preventiva fácil de aplicar (Figura 9) , ya que los ooquistes necesitan un mínimo de 24 horas para volverse infecciosos [4]. Mantener a los gatos en el interior del hogar (cuando sea posible) también es una medida útil. Los veterinarios deben desempeñar un papel fundamental enseñando a sus clientes las medidas que se deben tomar para limitar el riesgo de infección por T. gondii, tanto en gatos como a nivel general (Tabla 2).

Tabla 2. Estrategias para reducir el riesgo de zoonosis por infección de T. gondii [1],[2],[3],[4].
| Estrategias generales | Estrategias específicas para los gatos |
|---|---|
| Lavarse bien las manos después de manipular carne cruda, trabajar en el jardín o realizar otras actividades de riesgo (p. ej., vaciar/limpiar la bandeja de arena). | Mantener a los gatos domésticos dentro de casa |
| Lavar cuidadosamente los cuchillos de cocina y las tablas de cortar después de preparar carne cruda, frutas o verduras crudas | Alimentar a los gatos únicamente con alimentos comerciales secos, húmedos o comida cocinada |
| Cocinar bien la carne antes de consumirla | Limpiar diariamente la bandeja de arena y eliminar las heces de forma responsable (p.ej., en bolsas de basura cerradas). |
| Lavar o pelar las frutas y verduras antes de consumirlas | Evitar que las mujeres embarazadas o personas inmunodeprimidas limpien la bandeja de arena. |
| Utilizar guantes para trabajar en el jardín | Cubrir las zonas con arena o tierra suelta en las áreas de juego al aire libre para evitar que los gatos defequen en ellas. |
Conclusión
La infección por Toxoplasma gondii es frecuente en el gato y suele ser asintomática. No obstante, las infecciones agudas o diseminadas pueden afectar a órganos como los ojos, el cerebro u otros sistemas. La clindamicina es el tratamiento de elección. Para obtener un diagnóstico definitivo es necesario realizar pruebas serológicas para determinar los títulos de IgM o de IgG en muestras pareadas. La toxoplasmosis es una zoonosis por lo que es especialmente peligrosa en mujeres embarazadas o personas inmunodeprimidas. Sin embargo, el hecho de tener gatos no supone un riesgo significativo de infección en las personas; siendo más importante la ingestión de ooquistes a través de agua o alimentos contaminados o de quistes tisulares en la carne poco cocinada. La contaminación fecal del suelo y el agua también representa un grave riesgo para la salud. Con unas sencillas medidas de higiene se puede evitar la transmisión de T. gondii y, los cuidadores de gatos pueden limitar en gran medida el riesgo de zoonosis manteniendo a sus mascotas dentro de casa (si es posible) y limpiando a diario la bandeja de arena.
Christopher Fernandez-Prada
DMV, MSc, PhD, Departamento de Patología y Microbiología, Universidad de Montreal, Canadá
Canadá
El Dr. Fernández-Prada es veterinario e investigador de parasitología molecular y, en particular, de los parásitos zoonóticos. Es profesor asociado en la Facultad de Veterinaria de la Universidad de Montreal (UdeM) y director del Laboratorio de Diagnóstico de Parasitología Animal de dicha universidad, además de profesor adjunto en la Facultad de Medicina de la Universidad McGill. Sus áreas de investigación se centran en el descubrimiento de los mecanismos de resistencia a los fármacos y en el desarrollo de nuevas pruebas de diagnóstico y vacunas frente a los parásitos protozoarios.
Victoria Wagner
DMV, MSc, Departamento de Patología y Microbiología, Universidad de Montreal, Canadá
Canadá
La Dra. Wagner, tras licenciarse por la Facultad de Veterinaria de la UdeM en el 2020, realizó un Máster en Parasitología Veterinaria en dicha facultad en colaboración con el Centro de Salud de la Universidad McGill, centrándose en la leishmaniosis canina. Actualmente Victoria Wagner se dedica tanto a la clínica de pequeños animales como a la medicina veterinaria de los animales de laboratorio y tiene un especial interés por la investigación y la formación relacionada con los parásitos zoonóticos.
Referencias
- Mor GA. Toxoplasmosis in Animals. Merck Manual Veterinary Manual. 2022. https://www.msdvetmanual.com/generalized-conditions/toxoplasmosis/toxoplasmosis-in-animals accessed 17th January 2023
- Companion Animal Parasite Council (CAPC). CAPC Guidelines; Toxoplasma gondii. 2014. https://capcvet.org/guidelines/toxoplasma-gondii/ accessed 17th January 2023
- Torrey E. Sentinel seals, safe cats, and better treatments. In: Parasites, Pussycats and Psychosis. Springer, Cham. 2022;121-133.
- Cornell Feline Health Center. Toxoplasmosis in Cats. 2018 https://www.vet.cornell.edu/departments-centers-and-institutes/cornell-feline-health-center/health-information/feline-health-topics/toxoplasmosis-cats Accessed 17th January 2023
- Elmore SA, Jones JL, Conrad PA, et al. Toxoplasma gondii: epidemiology, feline clinical aspects, and prevention. Trends Parasitol. 2010;26(4):190-196.
- Barrs V. Feline Toxoplasmosis. In; Proceedings, WSAVA Congress 2013. Sydney, Australia.
- Abdul Hafeez M, Mehdi M, Aslam F, et al. Molecular characterization of Toxoplasma gondii in cats and its zoonotic potential for public health significance. Pathogens 2022;11(4):437.
- Castillo-Morales VJ, Acosta Viana KY, Guzmn-Marn EDS, et al. Prevalence and risk factors of Toxoplasma gondii infection in domestic cats from the Tropics of Mexico using serological and molecular tests. Interdiscip. Perspect. Infect. Dis. 2012;2012:529108.
- Center for Disease Control. Toxoplasmosis: An Important Message for Cat Owners. https://www.cdc.gov/parasites/toxoplasmosis/resources/printresources/catowners_2017.pdfaccessed 17th January 2023
- Iqbal A, Measures L, Lair S, et al. Toxoplasma gondii infection in stranded St. Lawrence Estuary beluga Delphinapterus leucas in Quebec, Canada. Dis. Aquat. Organ 2018;130(3):165-175.
- Miller MA, Grigg ME, Kreuder C, et al. An unusual genotype of Toxoplasma gondii is common in California sea otters (Enhydra lutris nereis) and is a cause of mortality. Int. J. Parasitol. 2004;34(3):275-284.
- Bowie, WR, King AS, Werker DH, et al. Outbreak of toxoplasmosis associated with municipal drinking water. The BC Toxoplasma Investigation Team. Lancet 1997;350(9072):173-177.
- Shapiro K, Bahia-Oliveira L, Dixon B, et al. Environmental transmission of Toxoplasma gondii: Oocysts in water, soil and food. Food Waterborne Parasitol. 2019;15;e00049.
- Yilmaz SM, Hopkins SH. Effects of different conditions on duration of infectivity of Toxoplasma gondii oocysts. J. Parasitol. 1972;58(5):938-939.
- Dubey JP, Lunney JK, Shen SK, et al. Infectivity of low numbers of Toxoplasma gondii oocysts to pigs. J. Parasitol. 1996;82(3):438-443.
- Dubey JP, Jones JL. Toxoplasma gondii infection in humans and animals in the United States. Int. J. Parasitol. 2008;38(11):1257-1278.
Otros artículos de este número
Compartir en las redes sociales