Implicazioni sistemiche della malattia periodontale
Scritto da Alessandro De Simoi
La malattia periodontale è la malattia infettiva più comune riscontrata nei piccoli animali, con una prevalenza che si avvicina all’80%. La prevalenza aumenta con l’età e diminuisce al crescere della taglia...
Article
Punti chiave
La malattia periodontale la malattia infettiva pi comune rilevata nei piccoli animali.
stato suggerito che la malattia periodontale possa essere un fattore maggiore in diverse malattie sistemiche, tra cui problemi cardiovascolari, disturbi della riproduzione, malattie del fegato e diabete.
Sono state formulate varie ipotesi sulle modalit con cui la periodontite pu influenzare la malattia sistemica, ma non esistono ancora prove definitive di un collegamento.
La malattia periodontale pu essere prevenuta con la rimozione accurata della placca batterica mediante spazzolamento dei denti e igiene orale.
Introduzione
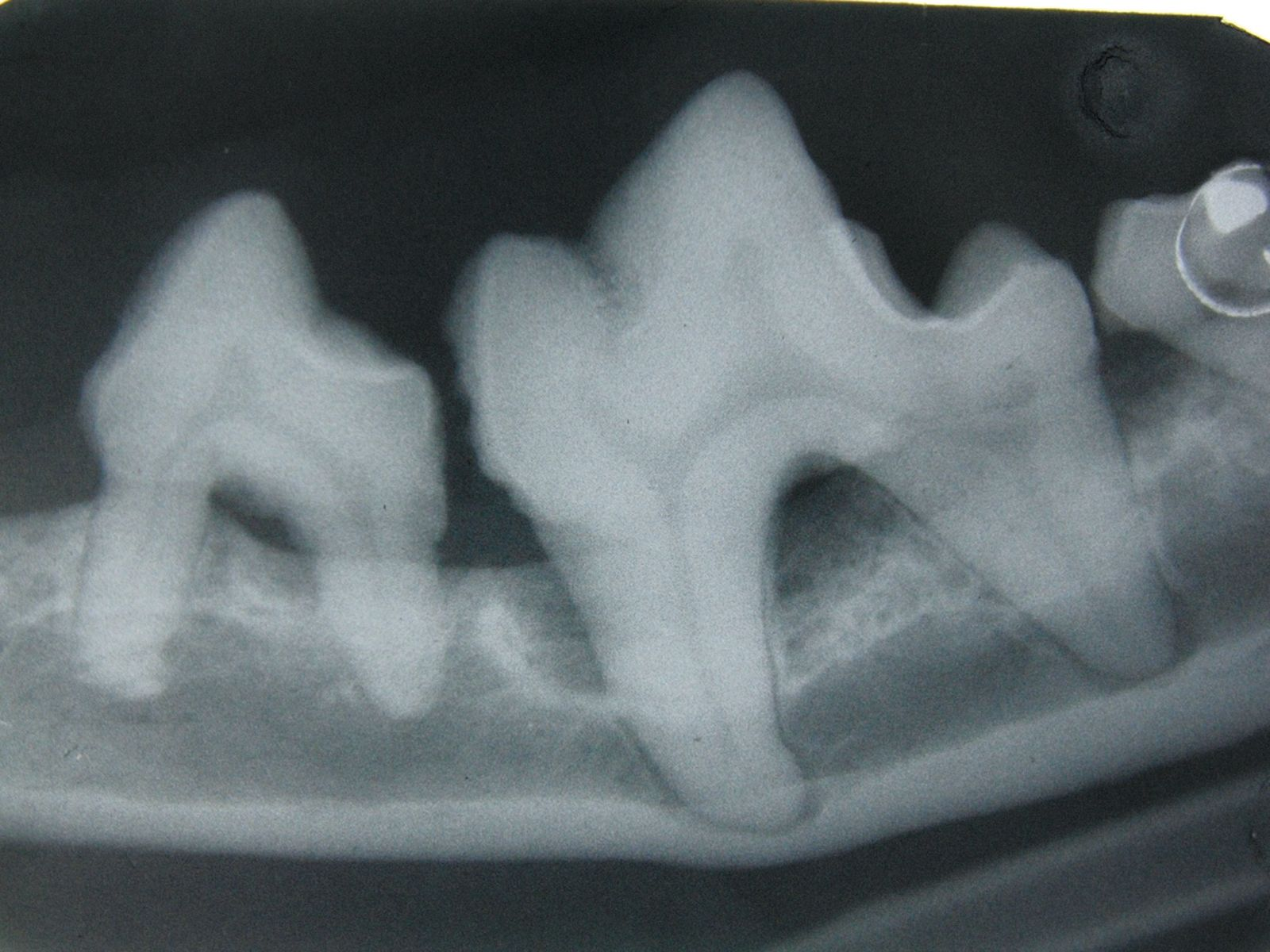
La malattia periodontale è la malattia infettiva più comune riscontrata nei piccoli animali, con una prevalenza che si avvicina all’80% [1]. La prevalenza aumenta con l’età e diminuisce al crescere della taglia: è molto più comune negli animali più piccoli rispetto a quelli di taglia media e grande [1]. Il periodonto comprende la gengiva, il cemento, il legamento alveolare dentale e l’osso alveolare, che insieme contribuiscono al sostegno del dente. La malattia periodontale è causata dalla placca batterica, e ha due componenti: gengivite e periodontite. La gengivite è un’infiammazione reversibile delle gengive, perché una volta rimossa la causa (placca batterica) l’infiammazione recede. La periodontite, invece, è una condizione infiammatoria irreversibile del tessuto non gengivale (legamento alveodentario, cemento e osso alveolare) e viene valutata misurando la perdita di fissaggio del dente. La periodontite può essere inattiva (quiescente), dove manca un’evidenza di infiammazione gengivale (e se vi è stata perdita di fissaggio dei denti, questa può essere avvenuta qualche tempo prima), oppure attiva con distruzione tissutale in corso (Figura 1). Sebbene sia riconosciuto che la periodontite è una malattia infettiva e siano state identificate più di 700 specie batteriche capaci di colonizzare il biofilm del solco sottogengivale, i postulati di Koch * non sono applicabili a questa condizione [2].
* 1. Il microrganismo responsabile deve essere rilevato in abbondanza nell’animale affetto dalla malattia, ma deve essere assente negli animali sani. 2. Il microrganismo deve essere isolato da un animale malato e messo in coltura. 3. Il microrganismo coltivato deve quindi causare la malattia quando introdotto in un animale sano. 4. Il microrganismo deve essere nuovamente isolato da questo animale infettato sperimentalmente e identificato come identico all’agente causale originale.
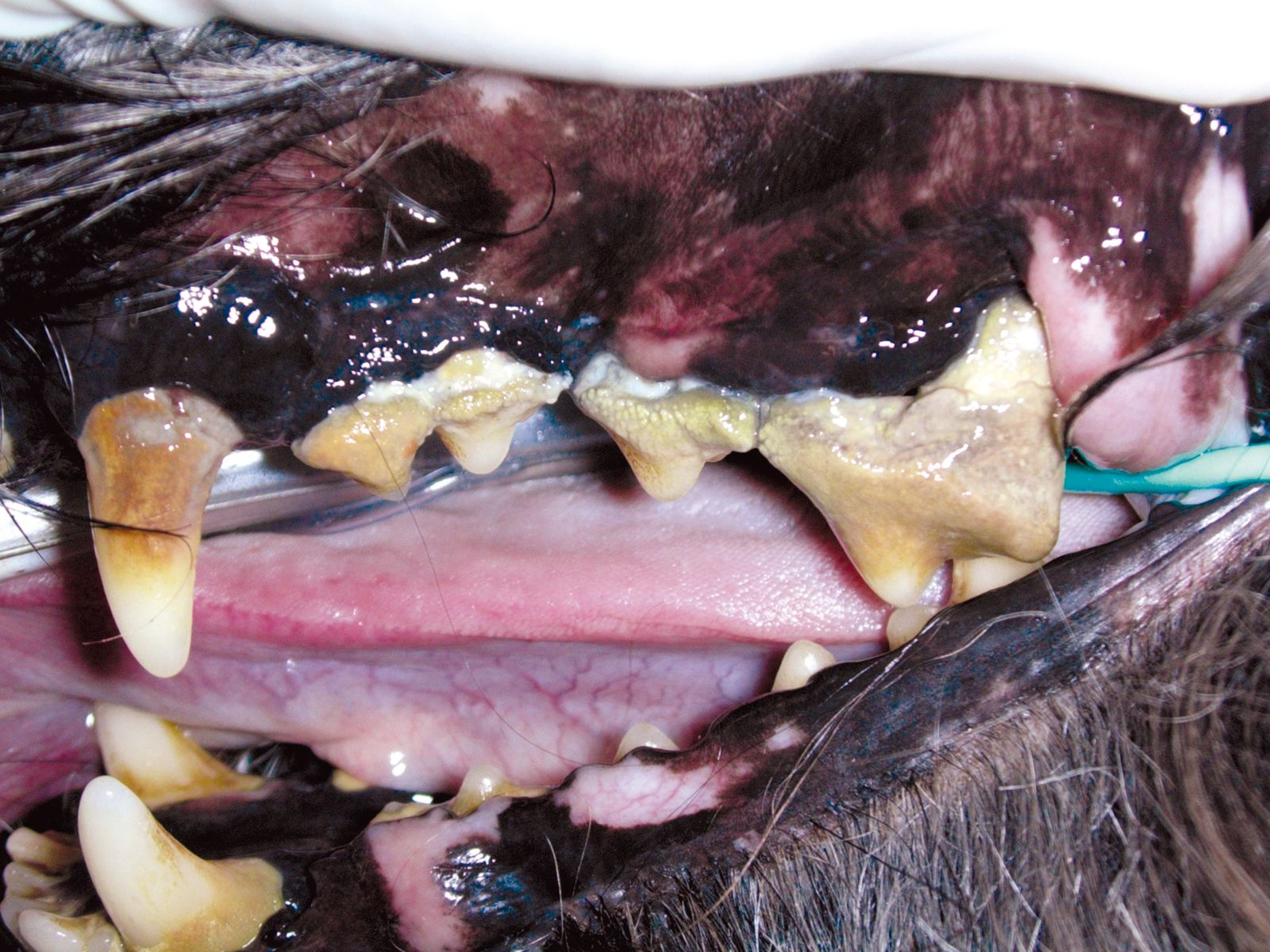
La gengivite, anche se non trattata, non esita sempre nella periodontite. Lo sviluppo della malattia periodontale è infatti determinato da uno squilibrio tra la popolazione batterica e il sistema immunitario dell’ospite. Capacità immunitaria, stress, età, stato nutrizionale e stato metabolico, razza e malattie endocrine, sono tutti fattori che possono favorire o prevenire la progressione della malattia periodontale.
Se la malattia progredisce, la distruzione ossea e la migrazione apicale del tessuto connettivo di sostegno esitano nell’allentamento e perdita finale di uno o più denti.
La malattia periodontale è un’infezione focale. Questo concetto, introdotto più di un secolo fa, descrive una malattia cronica localizzata che rappresenta una fonte di microrganismi, tossine e prodotti della degradazione batterica e tissutale, in grado di raggiungere organi e tessuti remoti [3]. La superficie corporea coinvolta nella periodontite è stata misurata in alcune razze toy colpite ed è risultata compresa tra 3,18 e 29,8 cm2 [4]. Per questa ragione, l’area tissutale interessata può rappresentare una proporzione considerevole della superficie corporea totale del cane.
Durante lo sviluppo della periodontite, i batteri presenti nelle tasche periodontali possono raggiungere il flusso ematico provocando una batteriemia, e sebbene nei soggetti sani questi vengano intercettati dal sistema reticoloendoteliale [5], l’esposizione continua e prolungata alla batteriemia può essere associata alla malattia sistemica associata a organi e sistemi remoti [6] [7]. Le implicazioni sistemiche della malattia periodontale non sono tuttavia limitate alla carica batterica. Inoltre, possono essere coinvolti mediatori chimici infiammatori, endotossine batteriche e tossine derivanti dalla degradazione tissutale, o per conseguenza di effetti dannosi diretti o perché causa di reazioni immunitarie in organi distanti dalla cavità orale.
Implicazioni cardiovascolari
Lo stesso vale in medicina veterinaria, dove vari studi hanno anche dimostrato una correlazione positiva tra malattia periodontale e alterazioni istopatologiche che interessano il cuore e altri organi interni [4] [5] [6] [7][11] [12] [13] [14]. L’opinione scientifica internazionale non è tuttavia unanime sull’importanza delle infezioni orali nella genesi della malattia sistemica, perché non esiste attualmente alcuna evidenza conclusiva per un collegamento diretto tra malattia periodontale e altre malattie [14].
Disturbi della riproduzione
È stato dimostrato che le donne gravide con periodontite hanno un rischio fino a 7,5 volte superiore di parto prematuro e basso peso alla nascita dei neonati. Questo risultato è correlato all’aumento delle citochine proinfiammatorie innescato dalle lipoproteine batteriche circolanti. In alcuni casi, sono stati rilevati batteri periodontopatogeni direttamente all’interno del fluido amniotico [15].
Diabete mellito
Epatopatia
Ipotesi eziopatogenetiche
Dato che è difficile identificare con chiarezza i meccanismi che legano la malattia orale a quella sistemica, sono state formulate diverse ipotesi per spiegare questo rapporto, e precisamente l’infezione diretta, l’infiammazione sistemica con danno endoteliale, e il mimetismo molecolare tra antigeni batterici e autoantigeni.
Ipotesi dell’infezione diretta
Ipotesi dell’infiammazione sistemica
Secondo questa ipotesi, la periodontite causa un aumento nelle citochine circolanti che può danneggiare direttamente l’endotelio dei vasi sanguigni, portando alla formazione di lesioni del cuore e di altri organi interni. È stato dimostrato che citochine proinfiammatorie come TNF e IL6 possono causare mutazioni anaboliche nei miociti attraverso l’attivazione di segnali intracellulari, esitando infine nell’ipertrofia miocardica [20]. In diversi studi sono stati osservati livelli elevati di CRP associati a periodontite cronica [21], mentre uno studio recente [22] ha dimostrato che persone sottoposte a terapia periodontale intensiva (detartrasi e levigatura radicolare) avevano sperimentato una riduzione significativa nell’elasticità dell’arteria brachiale 24 ore dopo la terapia, rispetto al gruppo di controllo. Questo risultato era correlato all’aumento di CRP e IL6 durante la terapia periodontale. Tuttavia, 60 e 180 giorni dopo la procedura odontoiatrica, l’elasticità vascolare era significativamente maggiore nel gruppo sottoposto a terapia periodontale rispetto al gruppo di controllo, e tale aumento è stato attribuito agli effetti benefici del trattamento periodontale.
Ipotesi della reattività crociata molecolare
Diagnosi della malattia periodontale
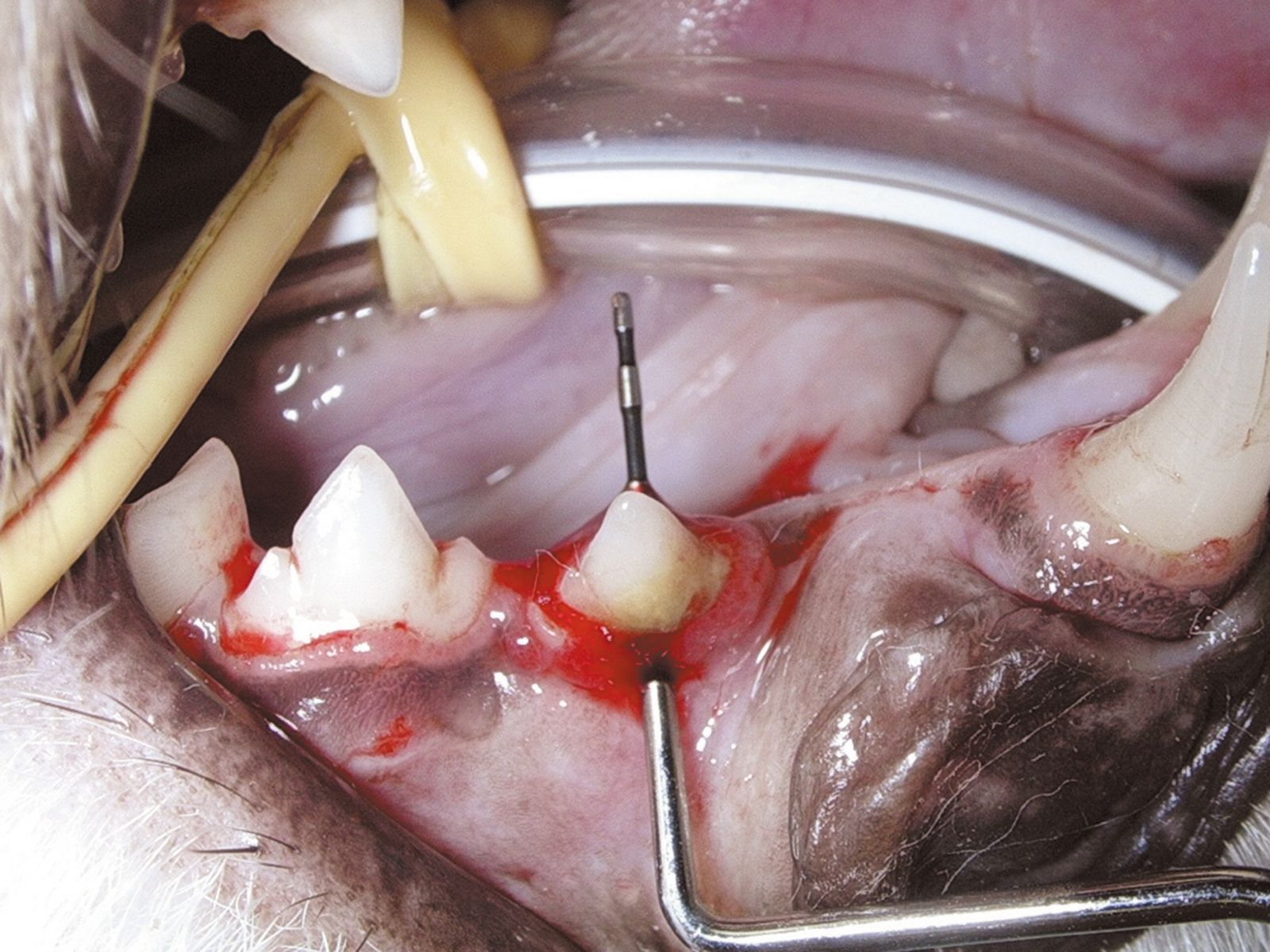
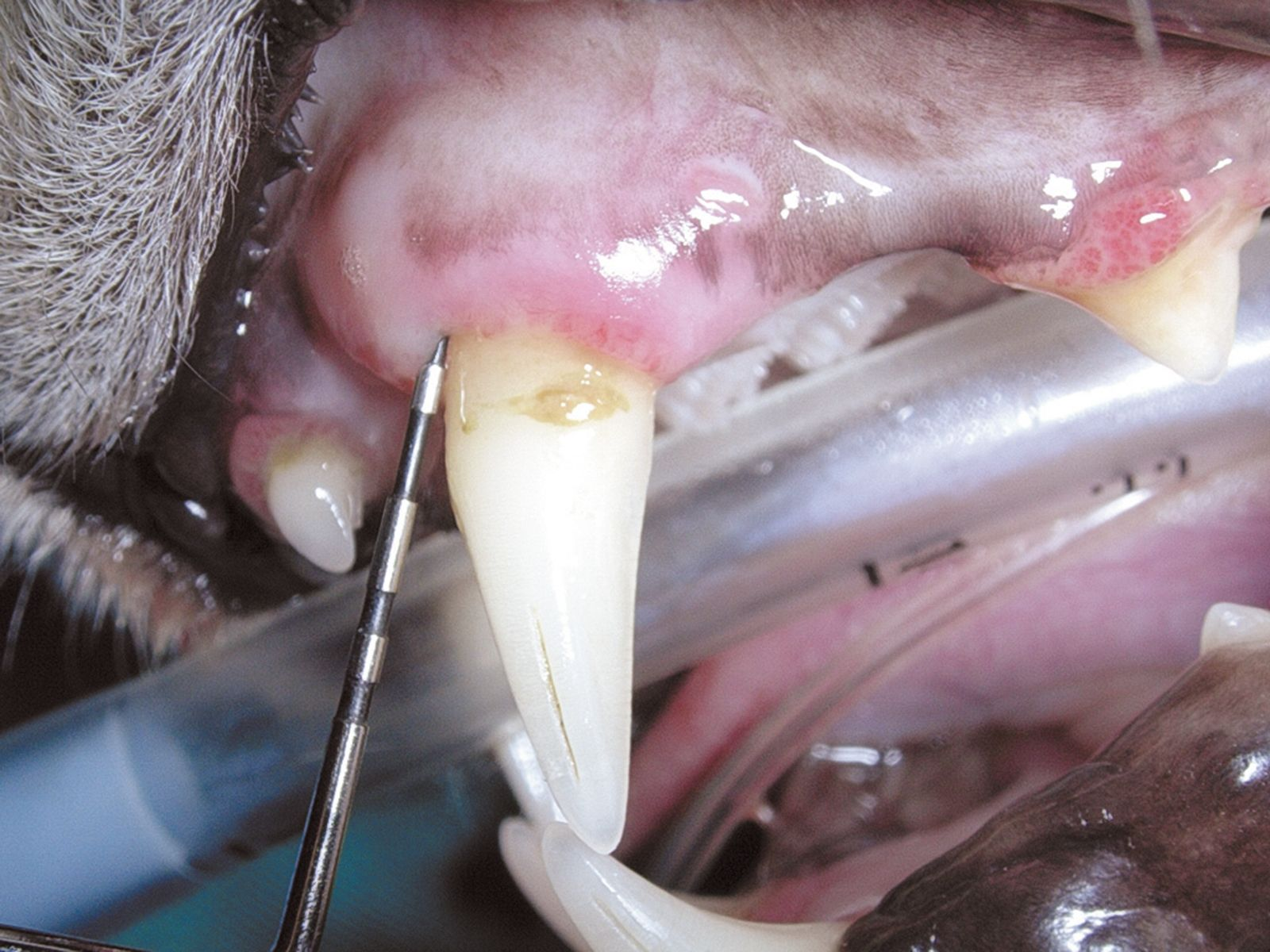
In genere, la malattia periodontale inizia con segni clinici limitati o nulli e il motivo principale perché il proprietario chieda una valutazione della cavità orale è che l’animale ha sviluppato un’alitosi. La diagnosi accurata non può basarsi esclusivamente sull’ispezione visiva della cavità orale ed è pertanto indispensabile praticare l’anestesia generale per esaminare il periodonto con una sonda (Figura 2) ed eseguire una radiografia intraorale. Sono disponibili varie sonde periodontali, ma tutte sono state progettate per misurare la profondità della tasca e valutare l’iperplasia o la retrazione gengivale. Con la sonda si può anche valutare il grado di mobilità dei denti e la presenza di lesioni della biforcazione nei denti con radici doppie o triple (Figura 3). La sonda deve essere delicatamente introdotta nel solco gengivale (Figure 4-5), valutando idealmente 4-6 punti lungo la circonferenza di ogni dente. I denti vestibolari apparentemente sani possono avere tasche profonde, a livello palatale o linguale. Tutte le osservazioni devono essere registrate su una scheda dentale per fornire una valutazione globale.

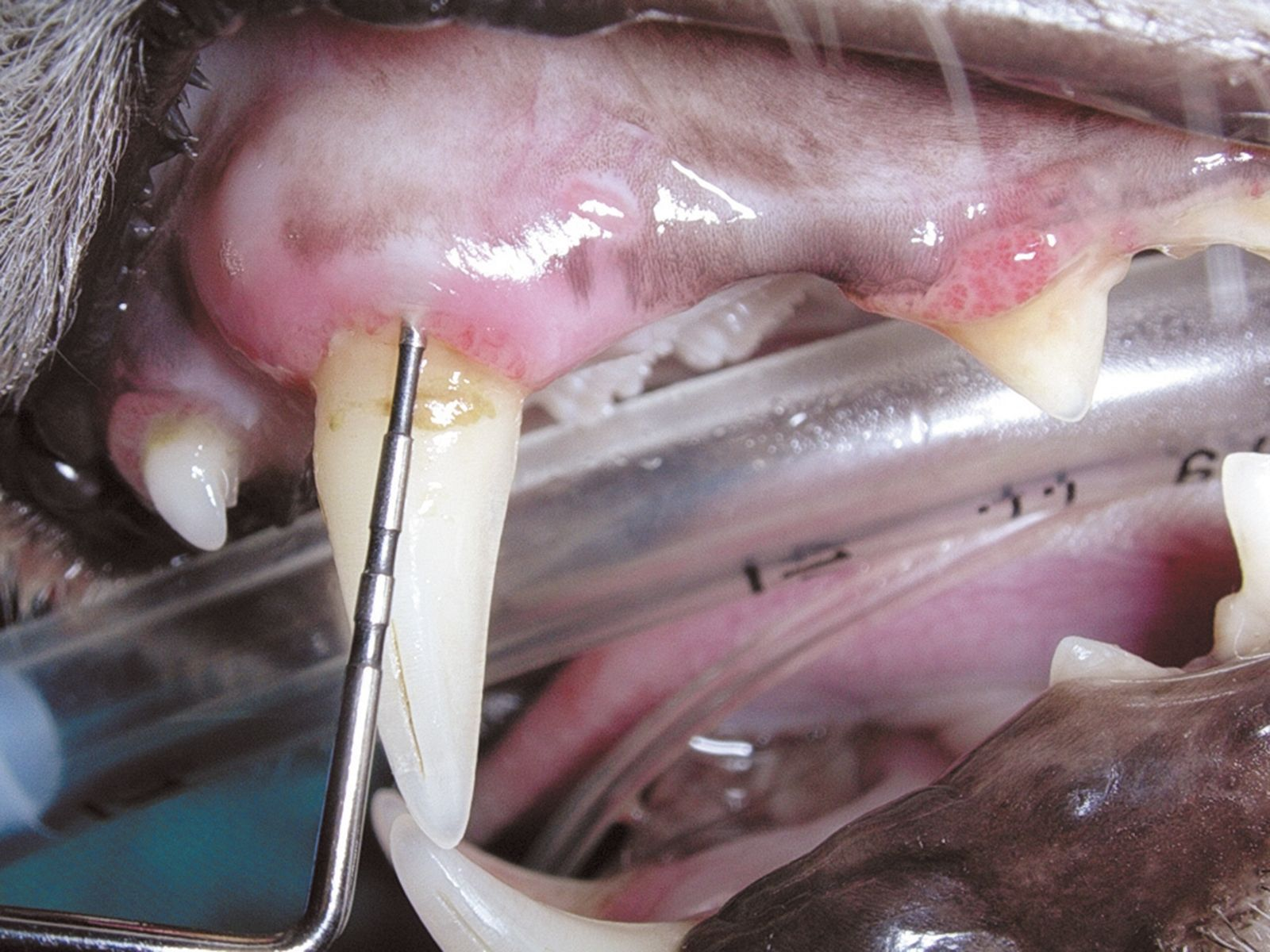
Prevenzione e trattamento della malattia periodontale
La malattia periodontale può essere prevenuta con la rimozione accurata della placca batterica mediante spazzolamento dei denti e igiene orale. Alcune diete commerciali possono aiutare a ridurre la placca coronale, ma il fattore determinante è la rimozione della placca sottogengivale. L’obiettivo non è sterilizzare la cavità orale, ma evitare che il biofilm batterico si trasformi da una popolazione commensale mista dominata dai batteri aerobi a una popolazione prevalentemente anaerobica. Il trattamento della malattia periodontale va praticato con l’animale anestetizzato e la trachea intubata. Una volta registrate accuratamente nella scheda le arcate e analizzate le radiografie intraorali (Figure 6-7) si esegue la detartrasi sopra e sottogengivale, seguita da procedure più complesse come l’estrazione del dente o la chirurgia periodontale, nei casi indicati.

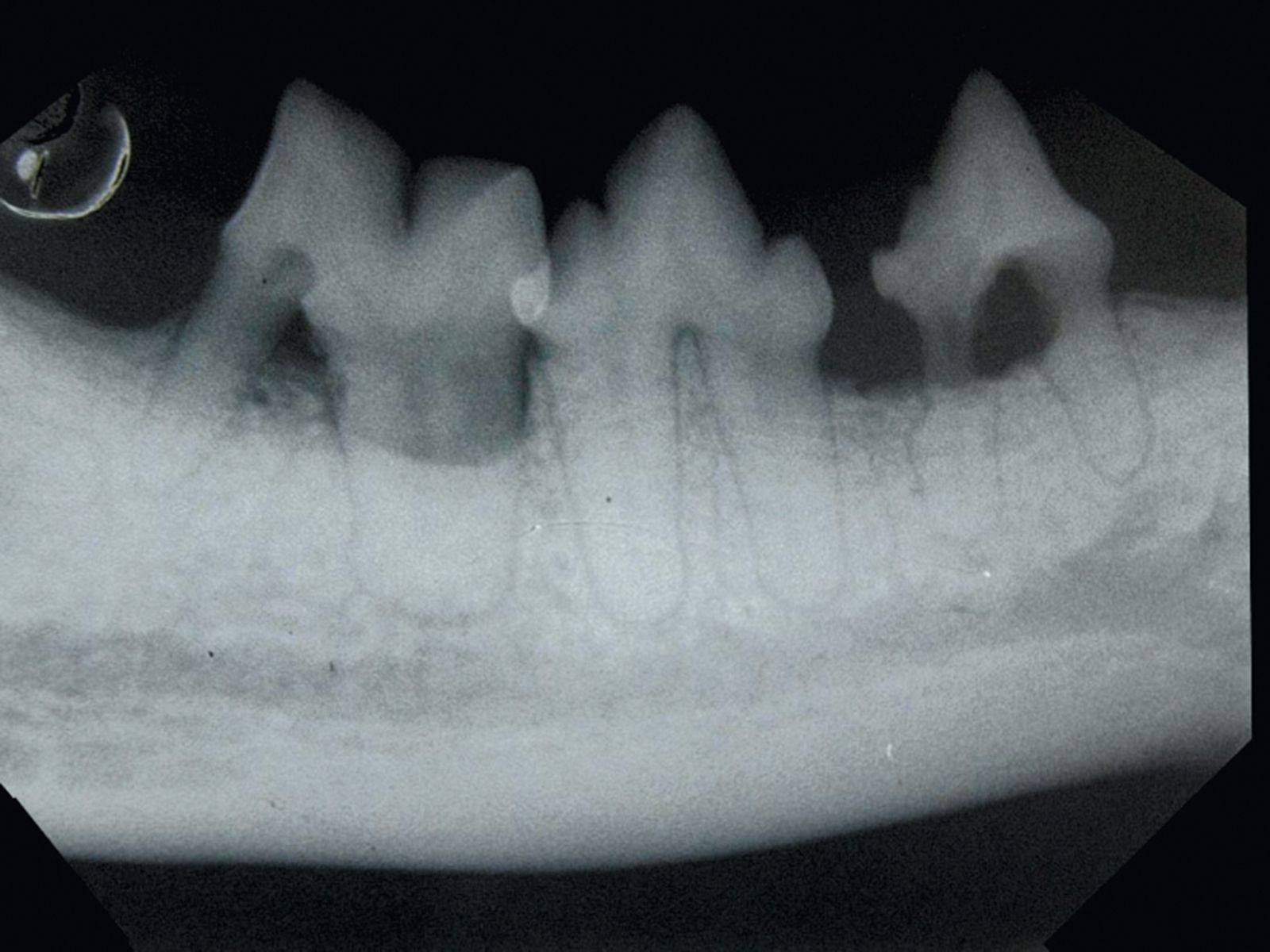
Utilizzo di antibiotici
Una malattia periodontale grave ed estesa in un soggetto altrimenti sano non va trattata con antibiotici a lungo termine. Il trattamento corretto consiste nel rimuovere la causa (placca, tartaro, denti irrimediabilmente compromessi) praticando la detartrasi e l’estrazione del dente, se necessario. Gli antibiotici devono essere utilizzati per due scopi principali: trattare l’infezione locale e prevenire batteriemia.Trattamento dell’infezione locale
Se la malattia periodontale ha causato un’osteomielite della mascella o della mandibola, è consigliabile una terapia antibiotica, iniziando un paio di giorni prima della chirurgia e proseguendo per diverse settimane dopo. L’uso di antibiotici pochi giorni prima della chirurgia trova inoltre indicazione quando si sono sviluppate lesioni gengivali ulcerative (anche con accumuli di placca limitati), nei casi di stomatite paradentale ulcerativa cronica nel cane (Figure 8a e 8b), e nei gatti con stomatite.
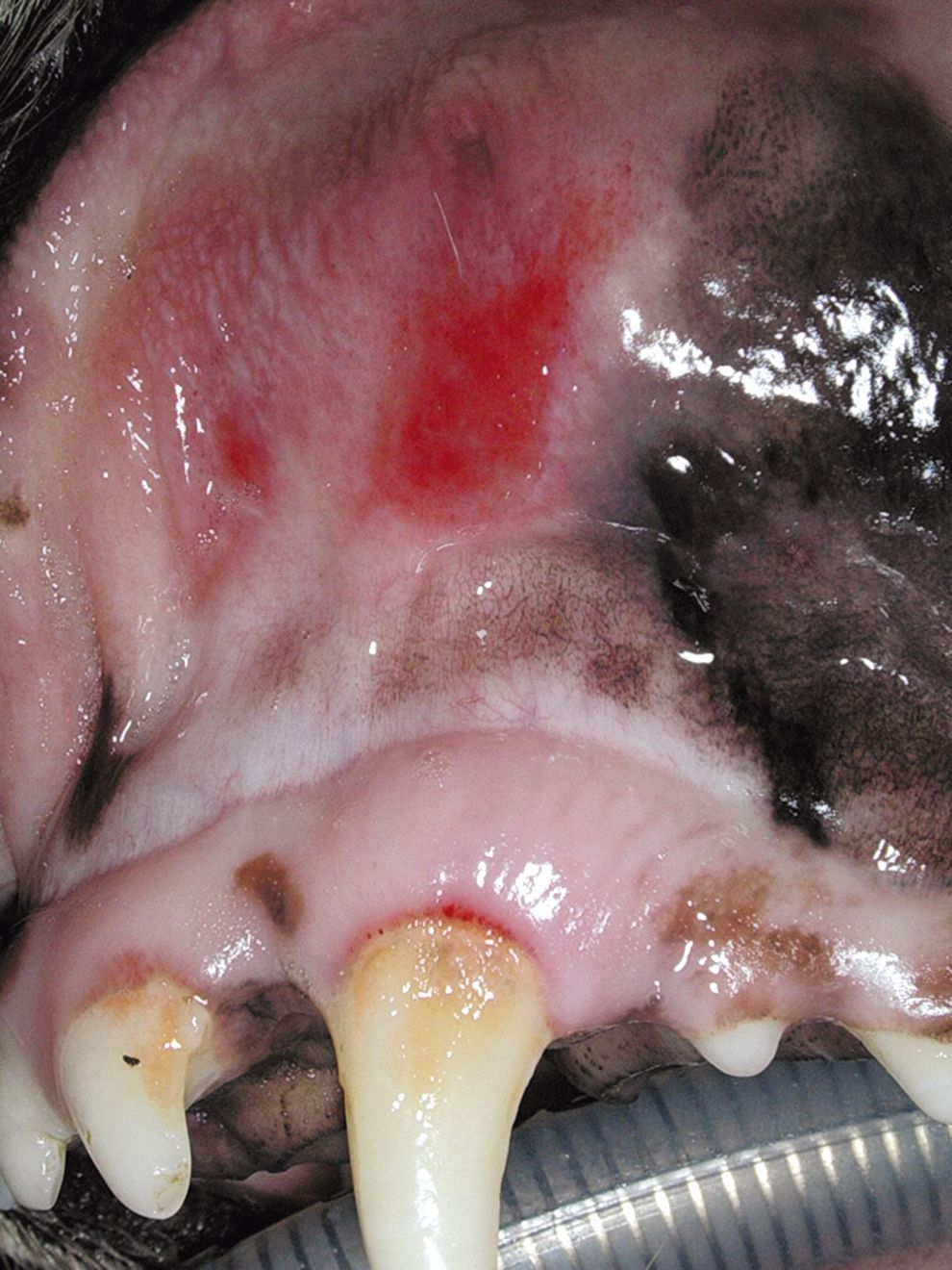
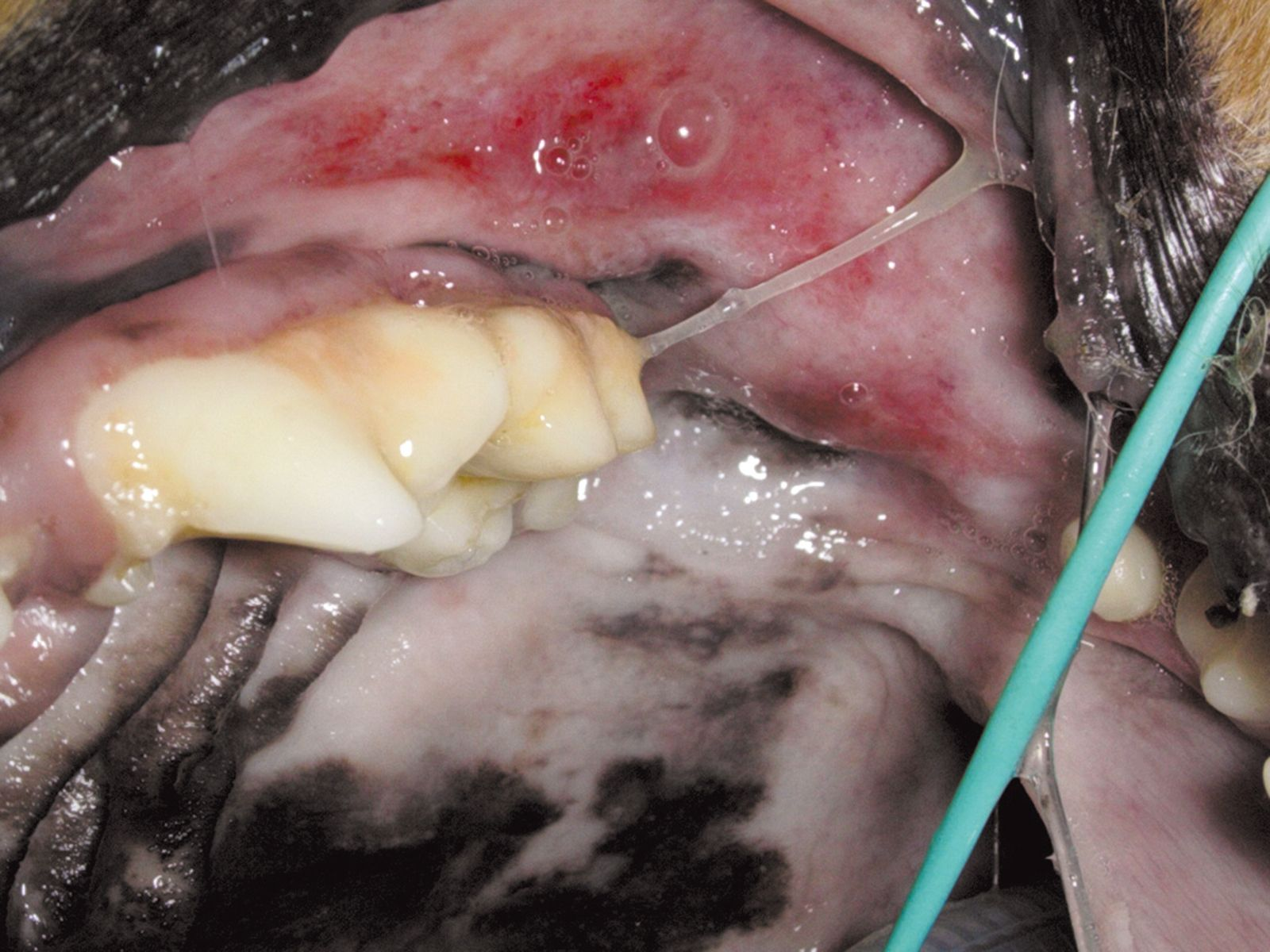
Profilassi della batteriemia
La batteriemia è comune nei pazienti con gengivite e periodontite attiva, avendo come causa le normali attività quotidiane come la tolettatura e la masticazione del cibo. Nei soggetti sani, è rapidamente contrastata dall’attività del sistema reticoloendoteliale. Nel caso di pazienti con periodontite associata a malattie sistemiche gravi, come ad esempio problemi cardiaci, nei soggetti con protesi articolari od oculari, negli animali splenectomizzati o con iperadrenocorticismo, e quando il metabolismo cellulare è depresso da una malattia sistemica, il rischio che possano essere interessati tessuti lontani dalla bocca giustifica l’uso di antibiotici perioperatori. In questi casi, la scelta è un antibiotico battericida ad ampio spettro che può essere somministrato per via endovenosa all’induzione dell’anestesia e ripetuto se l’operazione dura più di due ore. È inoltre possibile somministrare una singola dose per via orale la mattina della chirurgia.Conclusione
Al momento non vi è alcuna evidenza inequivocabile di una relazione diretta tra malattia periodontale ed effetti sistemici, anche se esistono diverse ipotesi che spiegano la relazione tra le due condizioni. Tuttavia, una notevole evidenza suggerisce che la malattia periodontale possa promuovere e mantenere l’infiammazione in organi distanti dalla bocca, e che anche nelle fasi iniziali di questa condizione il corpo possa reagire con la sintesi di proteine della fase acuta, dimostrando così la stimolazione di una malattia sistemica indotta da un’infiammazione della cavità orale.
La salute del periodonto non è importante solo per il mantenimento dei denti. La malattia periodontale può avere un impatto significativo sulla salute in generale ed essere responsabile della morbilità e mortalità, soprattutto in alcune razze di cani sensibili. La gestione della periodontite deve includere misure preventive quali l’igiene orale, l’uso di giocattoli da mordicchiare, e la somministrazione di prodotti appositamente studiati per ridurre l’accumulo della placca batterica e del tartaro. I prodotti alimentari che favoriscono la salute dentale sono solitamente costituiti da crocchette con struttura e conformazione tali da offrire un’azione abrasiva meccanica, ma alcuni prodotti contengono anche polifosfato di sodio che chela il calcio salivare, rallentando la mineralizzazione della placca e, di conseguenza, la formazione del tartaro. Questi alimenti possono quindi essere raccomandati come ausilio in un programma generico per ridurre la malattia periodontale.
Alessandro De Simoi
Med Vet, Dip. EVDC
Italia
Il Dr. De Simoi si è laureato presso l’Università di Bologna nel 1990 e ha conseguito il diploma EVDC nel 2008. I suoi interessi principali sono l’odontoiatria e la chirurgia maxillo-facciale nei piccoli animali e nel cavallo. Tra il 2001 e il 2003 ha seguito un tirocinio di formazione presso l’European School for Advanced Veterinary Studies in Lussemburgo e trascorso diversi periodi nel Regno Unito (Bell Equine Veterinary Clinic e Royal Dick School of Veterinary Studies) e negli Stati Uniti (University of Pennsylvania). Ha partecipato a numerosi congressi e conferenze nazionali e internazionali sull’odontoiatria veterinaria, e ha presentato corsi sul tema in Svizzera e in Francia. È stato segretario della Società Italiana di Odontostomatologia Veterinaria e Chirurgia orale dal 2001 al 2004, ed è attualmente vice presidente dell’associazione.
Riferimenti
- Lund EM, Armstrong PJ, Kirk CA, et al. Health status and population characteristics of dogs and cats examined at private veterinary practices in the United States. J Am Vet Med Assoc 1999;214:1336-1341.
- Haffajee AD, Socransky SS. Introduction to microbial aspects of periodontal biofilm communities, development and treatment. Periodontol 2000,2006; 42:7-12.
- Vieira CL, Caramels B. The history of dentistry and medicine relationship: could the mouth finally return to the body? Oral Dis 2009;15(8):538-46.
- Pavlica Z, Petelin M, Juntes P, et al. Periodontal disease burden and pathological changes in organs of dogs. J Vet Dent 2008;25(2):97-105.
- Silver JG, Martin L, McBride BC. Recovery and clearance of oral micro-organism following experimental bacteremia in dogs. Arch Oral Biol 1975;20:675-9.
- Glickman LT, Glickman NW, Moore GE, et al. Evaluation of the risk of endocarditis and other cardiovascular events on the basis of the severity of periodontal disease in dogs. J Am Vet Med Assoc 2009;234:486-494.
- DeBowes LJ, Mosier D, Logan E, et al. Association of periodontal disease and histologic lesions in multiple organs from 45 dogs. J Vet Dent 1996;13:57-60.
- Paquette DW. The periodontal infection-systemic disease link: a review of the truth or myth. J Int Acad Periodontol 2002;4(3):101-9.
- Janket SJ, Baird A, Chuang S, et al. Meta-analysis of periodontal disease and risk of coronary heart disease and stroke. Oral Surg Oral Med Oral Pathol 2003;95:559-596.
- Khader YS, Albashaireh ZSM, Alomari MA. Periodontal disease and the risk of coronary heart and cerebrovascular disease: a meta-analysis. J Periodontol 2004;75:1046-1153.
- Glickman LT, Glickman NW, Moore GE, et al. Association between chronic azotemic kidney disease and the severity of periodontal disease in dogs. Prev Vet Med. 2011 May 1;99(2-4):193-200. Epub 2011 Feb 23.
- Peddle GD, Drobatz KJ, Harvey CE, et al. Association of periodontal disease, oral procedures, and other clinical findings with bacterialendocarditis in dogs. J Am Vet Med Assoc. 2009 Jan 1;234(1):100-7.
- Yu G, Yu Y, Li YN, et al. Effect of periodontitis on susceptibility to atrial fibrillation in an animal model. J Electrocardiol. 2010 Jul-Aug;43(4):359-66. Epub 2009 Dec 29.
- O’Reilly PG, Claffey NM. A history of oral sepsis as a cause of disease. Periodontol 2000. 2000;23:13-18.
- Baskaradoss JK, Geevarghese A, Al Dosari AA. Causes of adverse pregnancy outcomes and the role of maternal periodontal status - a review of the literature. Open Dent J 2012;6:79-84. Epub 2012 May 9.
- van Nice E. Management of multiple dental infections in a dog with diabetes mellitus. J Vet Dent 2006;23(1):18-25.
- Yoneda M, Naka S, Nakano K, et al. Involvement of a periodontal pathogen, Porphyromonas gingivalis on the pathogenesis of non-alcoholic fatty liver disease. BMC Gastroenterol 2012;12:16.
- Ford PJ, GemmelE, Hamlet SM et al. Cross-reactivity of GroEL antibodies with human heat shock protein 60 and quantification of pathogens in arterosclerosis. Oral Microbiol Immunol 2005;20:296-302.
- Deshpande RG, KhanMB, Genco CA. Invasion of aortic and heart endothelial cells by Porphiromonas gingivalis. Infect Immun 1998;66:5337-5343.
- Franek E, Blach A, Witula A, et al. Association between chronic periodontal disease and left ventricular hypertrophy in kidney transplant recipients. Transplantation 2005;80:3-5.
- Amar S, Gokce N, Morgan S, et al. Periodontal disease is associated with brachial artery endothelial dysfunction and systemic inflammation. Arterioscler Thromb Vasc Biol 2003;23:1245-1249.
- Tonetti MS, D’Aiuto F, Nibali L, et al. Treatment of periodontitis and endothelial function. N Engl J Med 2007;356:911-920.
- Polla BS. A role for heat shock proteins in inflammation? Immunol Today 1988;9:134-137.
- Wick G, Perschinka H, Xu Q. Autoimmunity and atherosclerosis. Am Heart J 1999;138:444-449.
- Ando T, Kato T, Ishihara K,et al. Heat shock proteins in the human periodontal disease process. Microbiol Immunol 1995;39:321-327.
Altri articoli di questo numero
Condividi sui social media