เอนไซม์ตับของสุนัข - คำถามที่พบบ่อย
Written by Stefanie Klenner-Gastreich
การเก็บตัวอย่างเลือดเพื่อประเมินสถานะของตับ (liver status) เป็นหัตถการที่เกิดขึ้นในทุกๆวัน แต่การแปลผลนั้นอาจทำได้ยากกว่าที่สัตวแพทย์คิดไว้ในตอนแรก
Article
ประเด็นสำคัญ
• ผลการตรวจเอนไซม์ตับควรแปลผลโดยคำนึงถึงประวัติ อาการแสดงทางคลินิกและผลการวินิจฉัย (diagnostic findings) อื่นๆของสัตว์ป่วย
ในกรณีเนื้องอกตับ (hepatic neoplasia) การเพิ่มขึ้นของกิจกรรมเอนไซม์ตับ (liver enzyme activity) โดยรวมจะขึ้นอยู่กับระดับความเสียหายของเซลล์ตับ (hepatocellular damage) และ/หรือปริมาณของเนื้อเยื่อที่ตาย (tissue necrosis) ที่เกี่ยวข้องกับรอยโรคเนื้องอก (neoplastic lesion)
สาเหตุที่พบบ่อยของการเพิ่มขึ้นของเอนไซม์ตับคือการใช้ยา โดยเฉพาะอย่างยิ่งยาในกลุ่มกลูโคคอร์ติคอยด์ (glucocorticoids) (รวมถึงยาทาภายนอก (topical ointments)) และยากันชัก (anti-seizure drugs)
การทดสอบกระตุ้นกรดน้ำดี (bile acid stimulation tests) สามารถเป็นตัวบ่งชี้ (indicator) ของการทำงานของตับที่ดี แต่จำเป็นต้องแปลผลด้วยความระมัดระวัง
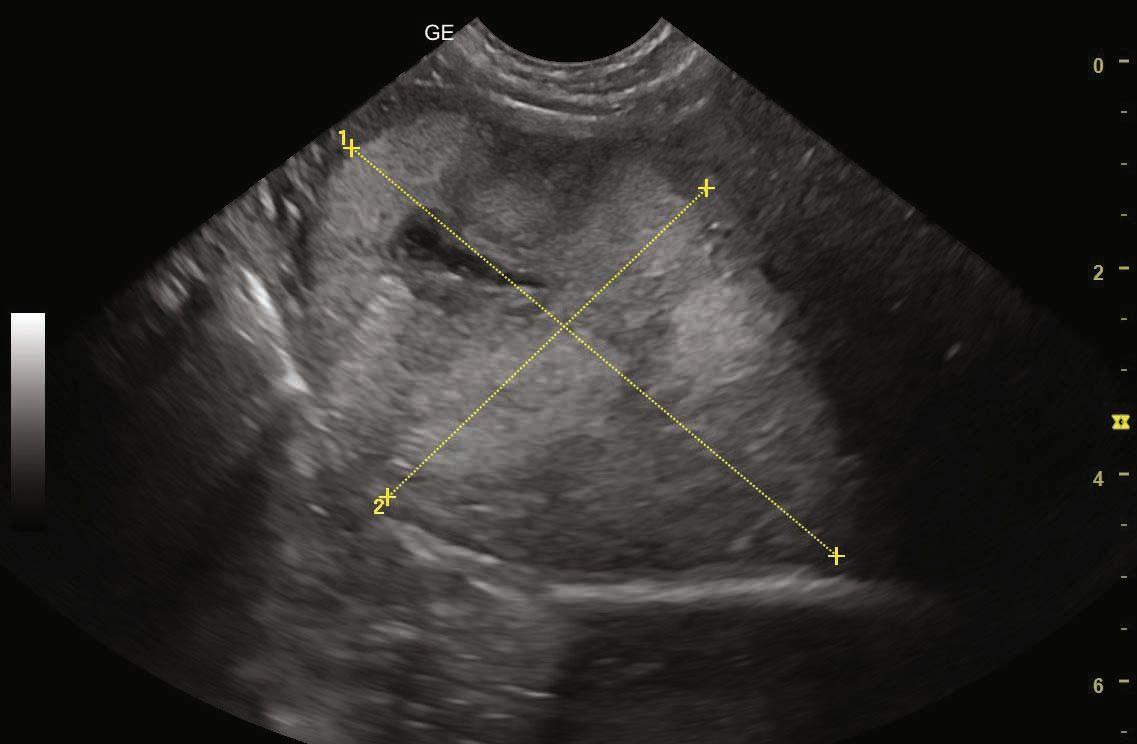
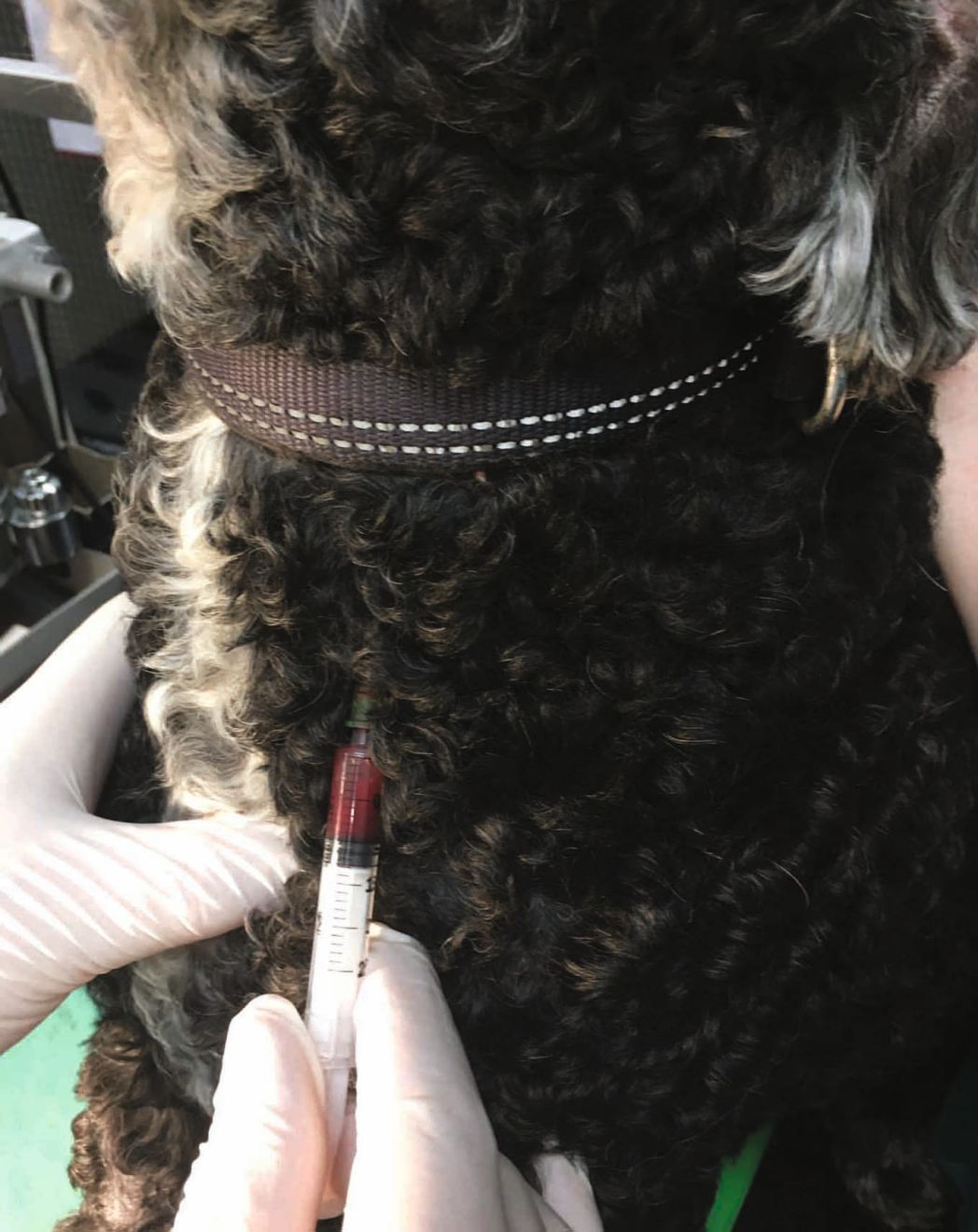
สัตวแพทย์สัตว์เล็กส่วนใหญ่จะเก็บตัวอย่างเลือดหลายครั้งต่อวันเพื่อประเมินสัตว์ป่วย (รูปภาพที่ 1) อย่างไรก็ตามการแปลผลอาจจะไม่ได้ตรงไปตรงมาเสมอไป โดยเฉพาะอย่างยิ่งเมื่อเกี่ยวข้องกับพารามิเตอร์ต่างๆของตับ อีกทั้งการทราบว่าการทดสอบใดมีประโยชน์ที่สุดเมื่อต้องวินิจฉัยหรือติดตามอาการบางอย่างก็อาจเป็นประโยชน์เช่นกัน บทความนี้จะเสนอแนวทางแบบถาม-ตอบสำหรับคำถามเกี่ยวกับเอนไซม์ตับที่พบบ่อยที่สุด
โดยทั่วไปแล้วระดับของ alanine aminotransferase (ALT) และ aspartate aminotransferase (AST) จะต้องเพิ่มสูงขึ้นสองเท่าจึงจะถือว่ามีความสำคัญ ในแง่ของพยาธิสรีรวิทยา กิจกรรมเอนไซม์ภายในเซลล์ตับ (hepatocellular enzyme) ที่เพิ่มขึ้นเป็นผลมาจากการรั่วไหลของเอนไซม์จากเซลล์ตับ (ALT, AST) หรือการเหนี่ยวนำเอนไซม์ (alkaline phosphatase (ALP)) อย่างไรก็ตามสัตวแพทย์ควรแปลผลโดยคำนึงถึงประวัติของสัตว์ป่วย อาการแสดงทางคลินิกและผลการวินิจฉัยเพิ่มเติม ตัวอย่างเช่น ผลลัพธ์อาจแตกต่างกันไปขึ้นอยู่กับว่าเป็นโรคเฉียบพลันหรือเรื้อรัง โดยโรคเรื้อรังอาจมาพร้อมกับภาวะตับฝ่อ (liver atrophy) หรือภาวะพังผืดของตับ (liver fibrosis) และในเวลาต่อมากิจกรรมเอนไซม์ตับอาจอยู่ในช่วงค่าอ้างอิง (reference interval) หรือเพิ่มขึ้นเพียงเล็กน้อย เนื่องจากการทำงานของตับ (liver function) จะลดลงเมื่อเป็นโรครุนแรง ระดับเอนไซม์ตับที่ปกติร่วมกับการเปลี่ยนแปลงค่าพารามิเตอร์ที่เกี่ยวข้องกับการทำงานของตับ (liver function parameters) (เช่น ภาวะอัลบูมินในเลือดต่ำ (hypoalbuminemia) ระดับไนโตรเจนจากยูเรียในเลือด (BUN) ลดลง ภาวะน้ำตาลในเลือดต่ำ (hypoglycemia) ภาวะบิลิรูบินในเลือดสูง (hyperbilirubinemia) เปลี่ยนแปลงระดับความเข้มข้นของคอเลสเตอรอลและไตรกลีเซอไรด์ รวมถึงระยะเวลาของการแข็งเป็นลิ่มของเลือดนานขึ้น (prolonged coagulation times)) ถือเป็นเรื่องปกติของโรครุนแรง เช่น โรคเส้นเลือดลัดข้ามตับ (portosystemic shunt) ดังนั้นข้อสรุปที่ว่ากิจกรรมเอนไซม์ตับที่ปกติบ่งชี้ว่าตับมีสุขภาพดีจึงไม่ถูกต้องนัก การแปลผลเอนไซม์ตับควรได้รับการประเมินร่วมกับค่าพารามิเตอร์ที่เกี่ยวข้องกับการทำงานของตับและความสัมพันธ์กับประวัติและอาการแสดงทางคลินิกของสัตว์ป่วยควบคู่กันเสมอ
การตรวจทางห้องปฏิบัติการที่ดีที่สุดสำหรับทางเชื่อมของตับ (liver shunt) คืออะไร ?
สัตว์ป่วยที่เป็นโรคเส้นเลือดลัดข้ามตับจะประสบกับปัญหาภาวะความผิดปกติของหลอดเลือด (vascular anomalies) โดยหลอดเลือดดำจากระบบพอร์ทัล (portal system) จะเชื่อมต่อโดยตรงกับหลอดเลือดเวนาคาวาส่วนหลัง (caudal vena cava) หรือหลอดเลือดดำอะไซกอส (azygos vein) และเพราะทางเชื่อมนี้เลือดจึงไม่สามารถไปเลี้ยงเซลล์ตับ (hepatocytes) ได้ในปริมาณที่เพียงพอ ส่งผลให้ตับเล็กและฝ่อลง การสูญเสียเซลล์ตับอาจเกี่ยวข้องกับการเปลี่ยนแปลงทางห้องปฏิบัติการที่หลากหลาย เช่น ALT หรือ AST ซึ่งเป็นเอนไซม์ไซโทตอล (cytosolic enzyme) และส่วนใหญ่จะอยู่ในไมโทคอนเดรียของเซลล์ตับ เอนไซม์เหล่านี้อาจมีระดับปกติหรือเพิ่มสูงขึ้นในสัตว์ป่วยที่ได้รับผลกระทบ อย่างไรก็ตามหากจำนวนเซลล์ตับลดลงอย่างมีนัยสำคัญ เซลล์ตับที่เหลืออยู่อาจไม่ปล่อยเอนไซม์เหล่านี้ออกมาในปริมาณที่มีนัยสำคัญส่งผลให้ระดับเอนไซม์ในซีรั่มต่ำลงหรือปกติ ทั้งนี้เมื่อมวลตับเหลือเพียงร้อยละ 20-30 อาการของภาวะตับเสื่อมหน้าที่ลง (liver insufficiency) ก็จะปรากฏชัดเจนขึ้น ในกรณีดังกล่าว ตับจะไม่สามารถรักษาการทำงานทางสรีรวิทยา (physiologic functions) ได้อีกต่อไป ส่งผลให้การเผาผลาญ (metabolism) คาร์โบไฮเดรต ไขมัน วิตามินและโปรตีนเปลี่ยนแปลงไป รวมถึงความสามารถในการกำจัดพิษ (detoxification abilities) ก็ลดลง ผลที่ตามมาจากการเสื่อมหน้าที่ของตับก็คือ ภาวะน้ำตาลในเลือดต่ำ การเปลี่ยนแปลงระดับความเข้มข้นของคอเลสเตอรอลและไตรกลีเซอไรด์ ภาวะบิลิรูบินในเลือดสูง ภาวะอัลบูมินในเลือดต่ำ ระยะเวลาของการแข็งเป็นลิ่มของเลือดนานขึ้น ระดับความเข้มข้นของยูเรียลดลงและกรดน้ำดีเพิ่มขึ้น และ/หรือภาวะแอมโมเนียในเลือดสูง (hyperammonemia) นอกจากนี้การเปลี่ยนแปลงต่างๆเหล่านี้ สัตวแพทย์ยังมักพบภาวะโลหิตจางที่มีเม็ดเลือดแดงเล็ก (microcytic anemia) และค่าความถ่วงจำเพาะของปัสสาวะต่ำกว่าปกติ
ดังนั้นการทดสอบใดคือการทดสอบที่ดีที่สุดที่จะใช้ในกรณีที่สงสัยว่ามีทางเชื่อมของตับและการทดสอบที่กล่าวถึงในข้างต้นไม่สามารถให้คำวินิจฉัยที่ชัดเจนได้จริงหรือ ? ในกรณีที่ตับเสื่อมหน้าที่ลง การประเมินกรดน้ำดีขณะอดอาหารและหลังกินอาหาร/หลังการกระตุ้นน้ำดีจะมีประโยชน์อย่างมาก แต่ต้องจำไว้ว่าหากมีภาวะบิลิรูบินในเลือดสูง ความเข้มข้นของกรดน้ำดีก็จะเพิ่มขึ้น และการทดสอบกระตุ้นกรดน้ำดีอาจไม่ได้ให้ข้อมูลเพิ่มเติมแก่สัตว์ป่วยมากนัก กลไกคือโรคที่นำไปสู่การขับบิลิรูบินที่ละลายน้ำได้ (conjugated bilirubin) จากเซลล์ตับเข้าไปในท่อน้ำดีย่อย (bile canaliculi) บกพร่องก็จะทำให้การขับกรดน้ำดีบกพร่องและระดับความเข้มข้นของพารามิเตอร์อื่นๆจะเพิ่มสูงขึ้นตามมา
สิ่งนี้สามารถเกิดขึ้นได้ ! เราควรย้อนกลับไปที่หัวข้อพยาธิสรีรวิทยาเพื่อทำความเข้าใจเกี่ยวกับกลไกที่ทำให้กิจกรรมเอนไซม์ตับเพิ่มขึ้น เอนไซม์ตับนั้นไม่ใช่กลุ่มเอกพันธุ์ (homogeneous group) โดยทั่วไป ALT และ AST นั้นถือเป็น “เอนไซม์ตับ” ในขณะที่ ALP และ gamma glutamyltransferase (GGT) ที่ถึงแม้ว่ามักจะรวมอยู่ในหมวดหมู่นี้แต่จริงๆแล้วก็มีต้นกำเนิดมาจากเยื่อหุ้มเซลล์ของเซลล์เยื่อบุท่อน้ำดี (cell membrane of the biliary epithelial cells) เพราฉะนั้นจึงเป็นตัวบ่งชี้ (markers) สำหรับความผิดปกติของการคั่งน้ำดีภายในหรือภายนอกตับ (intra- or extrahepatic cholestatic disturbances) กิจกรรมของ ALT และ AST ที่เพิ่มขึ้นเกิดจากความเสียหายของเซลล์ตับ (hepatocellular damage) แบบย้อนกลับได้ (reversible) หรือย้อนกลับไม่ได้ (irreversible) (เนื้อตาย (necrosis)) ทั้งนี้มีเนื้องอกหลายประเภทที่สามารถส่งผลต่อตับได้ เนื้องอกตับปฐมภูมิอาจเป็นเนื้องอกก้อนกลมเฉพาะจุด (focal, nodular tumor) (เช่น most hepatocellular carcinomas) หรือเจริญในรูปแบบกระจาย (diffuse pattern) แทรกเข้าไปในเนื้อตับในลักษณะลุกลาม (disseminated manner) เนื้องอกที่มีรอยโรคเฉพาะจุดอาจทำให้กิจกรรมเอนไซม์เต็มเพิ่มขึ้นอย่างมีนัยสำคัญเพราะเซลล์ตับถูกทำลายอย่างรุนแรงและมีเนื้อเยื่อตาย (tissue necrosis) แต่ระดับ ALP อาจจะปกติหรือเพิ่มสูงขึ้นก็ได้ขึ้นอยู่กับระดับของภาวะท่อน้ำดีคั่งภายในตับ (intrahepatic cholestasis) เนื้องอกชนิดเซลล์กลม (round cell tumors) ที่แทรกซึมเข้าไปในตับแบบกระจาย (เช่น lymphoma หรือ mast cell tumors) อาจไม่เกี่ยวข้องกับความเสียหายของเซลล์ตับอย่างมีนัยสำคัญ ซึ่งในกรณีดังกล่าวเอนไซม์ตับจึงอาจจะเพิ่มสูงขึ้นเพียงเล็กน้อยหรือไม่เลยก็ได้
กล่าวโดยสรุปคือการเพิ่มขึ้นกิจกรรมเอนไซม์ตับใดใดก็ตามที่เกิดจากเนื้องอกของตับ (hepatic neoplasm) จะขึ้นอยู่กับระดับความเสียหายของเซลล์ตับและการปล่อยเอนไซม์ออกมาในภายหลัง และ/หรือปริมาณเนื้อเยื่อตายที่เกี่ยวข้องกับรอยโรคเนื้องอก (neoplastic lesion) เนื้องอกที่แทรกซึมเฉพาะจุดหรือกระจายตัวอาจทำให้เอนไซม์ตับสูงขึ้นหรือไม่ก็ได้ ดังนั้นการใช้รังสีวินิจฉัย (diagnostic imaging) (อัลตราซาวด์ช่องท้อง (abdominal ultrasound)) และเจาะดูดเซลล์ด้วยเข็มขนาดเล็ก (fine-needle aspirates) จึงถือเป็นขั้นตอนเพิ่มเติมที่สำคัญในการระบุโรคตับ (รูปภาพที่ 2

โรคที่ไม่ใช่โรคตับ (non-hepatic diseases) โรคใดบ้างที่ส่งผลกระทบต่อเอนไซม์ตับอย่างมีนัยสำคัญ ?
เนื่องจากตับเป็นอวัยวะหลักในร่างกายที่รับผิดชอบในการควบคุมกระบวนการเผาผลาญ (metabolic functions) หลายอย่าง โรคตับทุติยภูมิ (secondary hepatopathies) จึงมักพบได้บ่อย เช่น
- ภาวะท่อน้ำดีคั่ง (cholestasis) ไม่ว่าจะภายในตับหรือภายหลังตับ (intra- or post-hepatic) ก็มักทำให้กิจกรรมเอนไซม์ตับเพิ่มมากขึ้น เนื่องจากเอนไซม์ ALP และ GGT อยู่ในเซลล์เยื่อบุท่อน้ำดีเพราะฉะนั้นจึงเป็นตัวบ่งชี้ที่ไว (sensitive indicators) ต่อภาวะนี้ ภาวะท่อน้ำดีคั่งภายในตับอันเป็นผลมาจากการบวมของเซลล์ตับ (hepatocellular swelling) และการอุดตันของท่อน้ำดีย่อยในภายหลังสามารถพบได้ในภาวะตับอักเสบ (hepatitis) ที่เกิดจากสาเหตุใดใดก็ตาม ในกรณีดังกล่าวระดับของเอนไซม์ ALT และ AST มักจะเพิ่มขึ้นด้วย ส่วนในกรณีภาวะท่อน้ำดีคั่งภายหลังตับนั้นจะเกิดจากการอุดตันของท่อน้ำดี (obstruction of the bile duct) ซึ่งอาจรวมถึงการอักเสบ (inflammation) เนื้องอก (neoplasia) หรือนิ่วในถุงน้ำดี (choleliths) และเนื่องจากอวัยวะทั้งสองอยู่ใกล้กันมากจึงเป็นสาเหตุที่พบบ่อยของการเกิดภาวะท่อน้ำดีคั่งภายหลังตับ และการตรวจ DGGR lipase จะมีประโยชน์ในกรณีดังกล่าว
- โรคทางระบบร่างกาย (systemic diseases) ที่อาจส่งผลกระทบต่อตับนั้นมีอยู่หลายชนิดซึ่งรวมไปถึงโรคอักเสบ (inflammatory conditions) เช่น โรคระบบทางเดินอาหาร (gastrointestinal diseases) โรคตับอ่อนอักเสบ (pancreatitis) และภาวะติดเชื้อในกระแสเลือด (sepsis) โดยไม่เพียงแต่สารอาหาร แร่ธาตุ (minerals) แร่ธาตุที่ร่างกายต้องการในปริมาณน้อย (trace elements) และวิตามินเท่านั้นที่จะถูกดูดซึมจากลำไส้และส่งไปที่ตับผ่านหลอดเลือดดำพอร์ทัล (portal vein) เท่านั้น แต่ในโรคระบบทางเดินอาหาร แบคทีเรีย สารพิษ ยาและ/หรือไซโตไคน์ (cytokines) ก็จะถูกส่งเข้าไปในตับด้วยเช่นเดียวกัน การเปลี่ยนแปลงทางเซลล์วิทยาที่เกี่ยวข้องในเซลล์ตับคือพบว่ามีสะสมของน้ำและ/หรือไกลโคเจน (glycogen) ในเซลล์ตับ ซึ่งมักจะมีลักษณะไม่รุนแรง เพราะฉะนั้นกิจกรรมเอนไซม์ ALT ที่เพิ่มขึ้นจึงมักจะไม่รุนแรงเช่นเดียวกัน โรคติดเชื้อ (infectious conditions) ซึ่งได้แก่ แบคทีเรีย (เช่น โรคฉี่หนู (leptospirosis)) ไวรัส (เช่น การติดเชื้ออะดิโนไวรัสชนิดที่ 1 ในสุนัข (canine adenovirus 1 infection)) หรือเชื้อรา (เช่น โรคฮิตโตพลาสโมซิส (histoplasmosis)) ล้วนแต่เกี่ยวข้องกับระดับเอนไซม์ตับที่เพิ่มขึ้นอย่างเห็นได้ชัด ออกซิเจน (oxygen supply) นั้นมีความสำคัญต่อตับและภาวะเนื้อเยื่อพร่องออกซิเจน (hypoxia) ซึ่งอาจเป็นผลสืบเนื่องมาจากภาวะโลหิตจาง (anemia) ภาวะเม็ดเลือดแดงแตก (hemolysis) หรือโรคหัวใจและหลอดเลือด (cardiovascular disease) อาจทำให้เซลล์ตับเกิดความเสียหายและกิจกรรมเอนไซม์ตับผิดปกติไปจากเดิมได้
- นอกจากนี้ความเสียหายของกล้าม (muscle damage) ก็เป็นสิ่งที่ควรพิจารณาร่วมด้วย กิจกรรมเอนไซม์ AST นั้นไม่จำเพาะต่อตับ (liver-specific) และอาจเพิ่มขึ้นหลังจากกล้ามเนื้อเสียหายเพราะเอนไซม์นี้อยู่ภายในเนื้อเยื่อของกล้ามเนื้อหัวใจและกล้ามเนื้อโครงร่าง (cardiac and skeletal muscle tissue) และเนื่องจาก AST นั้นเป็นเอนไซม์ที่มีลักษณะไม่จำเพาะ สัตวแพทย์จึงควรประเมินเอนไซม์นี้ร่วมกับพารามิเตอร์ทางห้องปฏิบัติการอื่นๆ เอนไซม์ ALT ก็อาจเพิ่มสูงขึ้นได้ในโรคกล้ามเนื้อเสื่อม (muscle dystrophies) บางชนิดที่หายาก โรคกล้ามเนื้อที่ยังคงดำเนินอยู่ส่วนใหญ่มักไม่เกี่ยวข้องกับการรั่วไหลของเอนไซม์ ALT ดังนั้นหากระดับเอนไซม์ ALT เพิ่มขึ้นพร้อมกัน แสดงว่าสาเหตุอาจจะมาจากตับ ในกรณีที่ประวัติและประวัติโรค (anamnesis) ของสัตว์ป่วยเผยให้เห็นว่ามีการบาดเจ็บของกล้ามเนื้อ (muscle trauma) หรือกล้ามเนื้ออักเสบ (inflammation) การตรวจวัดระดับกิจกรรมเอนไซม์ creatine kinase (CK) จะช่วยระบุโรคกล้ามเนื้อที่เป็นสาเหตุให้เอนไซม์ AST เพิ่มสูงขึ้นได้
- ภาวะเม็ดเลือดแดงแตก (Hemolytic disruption of red blood cells (RBCs)) อาจทำให้กิจกรรมของเอนไซม์ AST เพิ่มสูงขึ้นเล็กน้อยเพราะเอนไซม์ตัวนี้อยู่ในเม็ดเลือดแดง (erythrocytes) ด้วย ตัวอย่างนี้แสดงให้เห็นว่าดารประเมินทางโลหิตวิทยา (hematologic assessment) ควบคู่ไปกับผลทางชีวเคมีนั้นมีความสำคัญอย่างยิ่ง
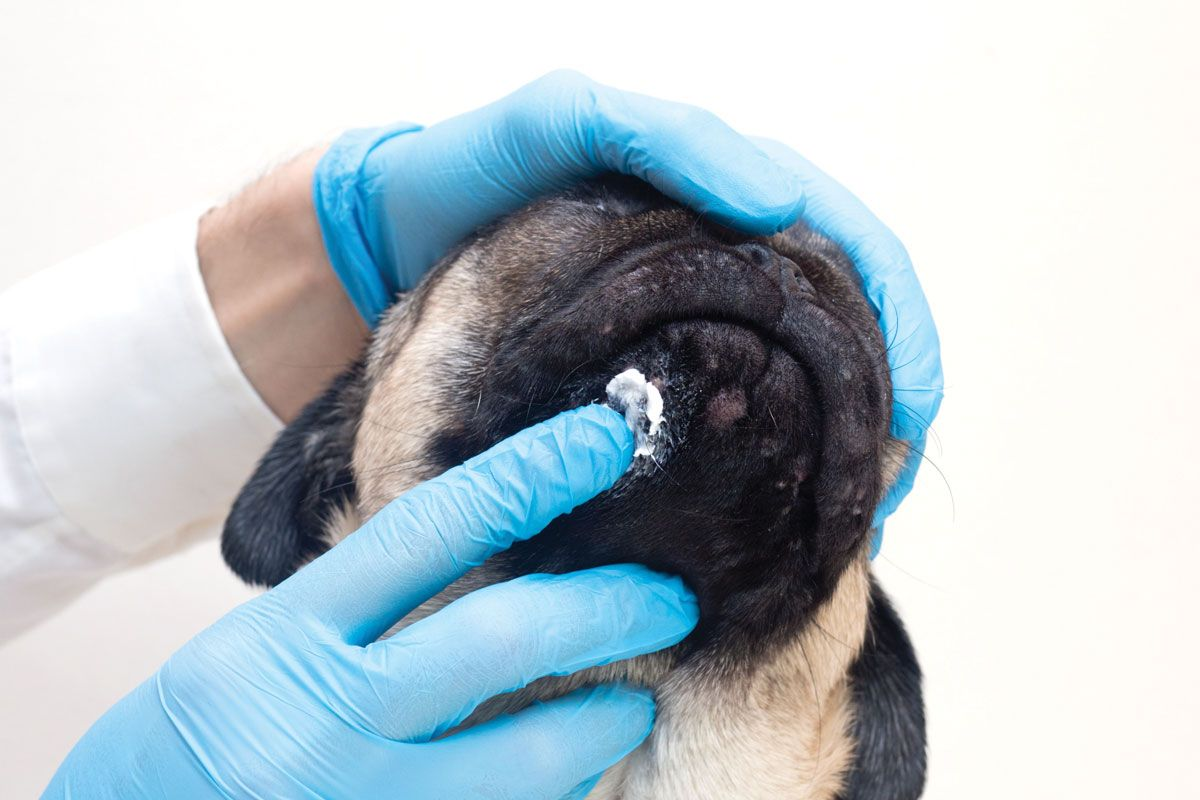
- ความเป็นพิษ (toxicities) เป็นสาเหตุที่พบได้บ่อยที่ทำให้เอนไซม์ตับเพิ่มสูงขึ้น โดยเฉพาะอย่างยิ่งจากยารักษาโรค (medical drugs) ที่ได้รับอยู่ กลไกที่สำคัญที่สุดก็คือการเหนี่ยวนำการผลิตเอนไซม์โดยสารต่างๆเหล่านี้ และความเป็นพิษก็ถือเป็นสาเหตุหลักประการหนึ่งที่ทำให้กิจกรรมเอนไซม์ ALP เพิ่มสูงขึ้น ยาที่น่าจำได้แก่ ยากันชัก (anticonvulsants) phenobarbital และ primidone รวมถึงยาในกลุ่มกลูโคคอร์ติคอยด์ (glucocorticoids) (โดยเฉพาะ prednisolone และ prednisone) ทั้งนี้เพราะถึงแม้จะเป็นยาทาภายนอก (topical ointments) ก็สามารถส่งผลต่อกิจกรรมเอนไซม์ ALP ได้ (รูปภาพที่ 3) เพราะฉะนั้นการซักประวัติสัตว์ป่วยอย่างละเอียดถี่ถ้วนจึงมีความสำคัญมากที่สุดในกรณีนี้เพราะเจ้าของสัตว์อาจคาดไม่ถึงผลของการรักษาดังกล่าวและอาจกล่าวถึงก็ต่อเมื่อถูกถามโดยเฉพาะเท่านั้น กลูโคคอร์ติคอยด์จะกระตุ้นการผลิต canine-specific corticoid-induced ALP (C-ALP) isoform โดยกิจกรรมเอนไซม์ ALP จะเพิ่มสูงขึ้นจนสังเกตเห็นได้ภายใน 7 วันหลังจากเริ่มการรักษาและอาจลดลงหลังจากหยุดการรักษาเพียง 6 สัปดาห์ การแปลผลกิจกรรมเอนไซม์ ALP ที่เกิดจากการตอบสนองต่อการรักษานั้นจะมีความซับซ้อนเนื่องจากการเปลี่ยนแปลงของเอนไซม์จะขึ้นอยู่กับชนิดของสเตียรอยด์ (steroid) และขนาดยา (dosage) ที่ใช้ ระยะเวลาของการรักษาและวิธีการบริหารยา (route of administration) (ทางการกิน (orally) ทางหลอดเลือดดำ (intravenously) หรือยาทาภายนอก (topically)) นอกจากนี้สัตว์ป่วยบางรายอาจแสดงการตอบสนองต่อการรักษาบางอย่างเป็นรายตัว ทั้งหมดที่กล่าวถึงจึงทำให้การแปลผลมีความซับซ้อนมากยิ่งขึ้น
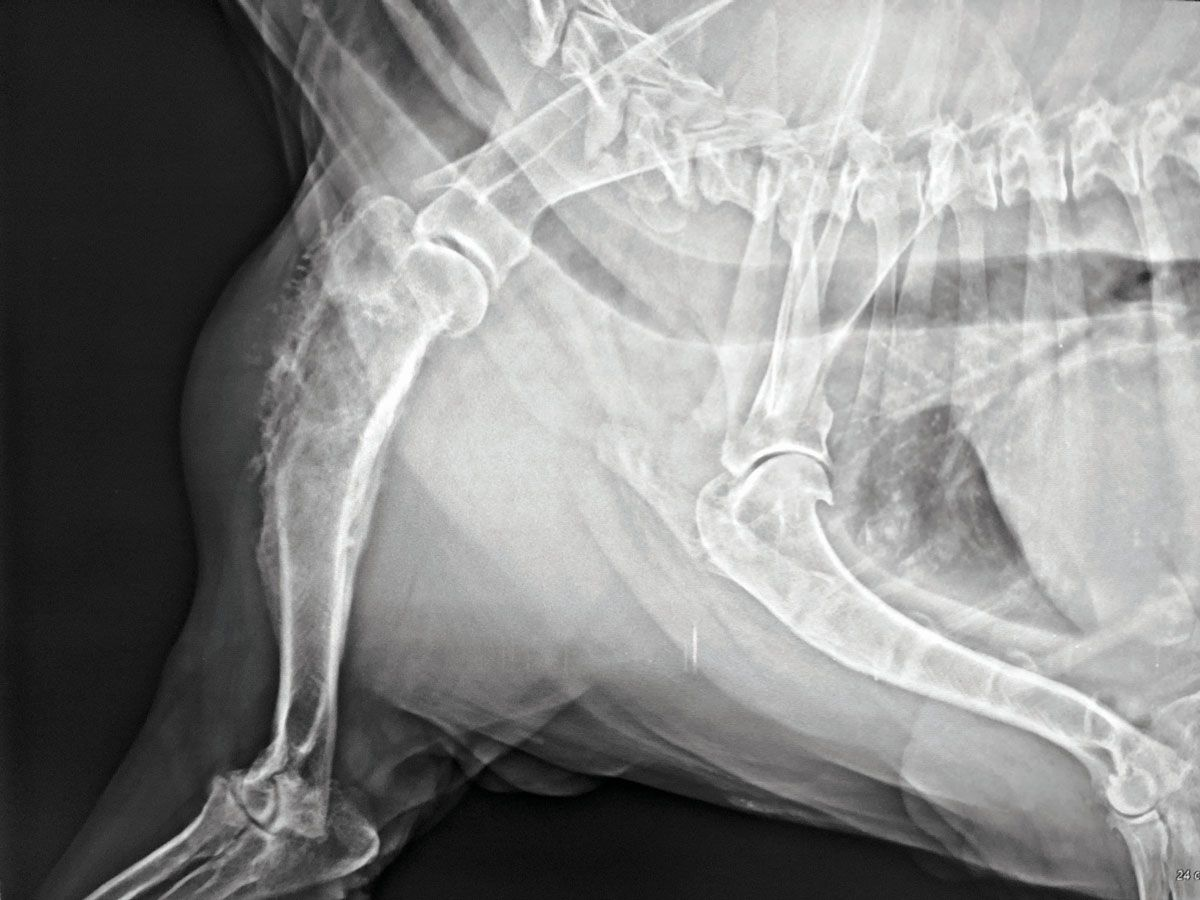
- ภาวะของกระดูก (bone conditions) ก็สามารถส่งผลต่อกิจกรรมเอนไซม์ตับได้เช่นเดียวกัน เนื่องจาก ALP มีอยู่ใน isoform ต่างๆ รวมถึง Bone-ALP ที่มีต้นกำเนิดจากเซลล์สร้างกระดูก (osteoblasts) เพราะฉะนั้นอาจพบการเพิ่มขึ้นของ isoform นี้มากถึง 3 เท่าในสัตว์อายุน้อยที่กำลังเจริญเติบโตโดยเป็นผลมาจากกิจกรรมของเซลล์สร้างกระดูกที่เพิ่มขึ้น มะเร็งกระดูก osteosarcoma ก็อาจมาพร้อมกับกระบวนการปรับแต่งกระดูก (bone remodeling) ที่เพิ่มมากขึ้น ดังนั้นเนื้องอกที่กระดูก (neoplasia of the bone) จึงเป็นหนึ่งในการวินิจฉัยโรคแยกแยะ (differentials) ในสัตว์ป่วยโตเต็มวัยที่มีระดับเอนไซม์ ALP เพิ่มสูงขึ้น (รูปภาพที่ 4) นอกจากนี้สัตวแพทย์ควรพิจารณาถึงความผิดปกติของกระดูกอื่นๆ (เช่น เนื้อตาย (necrosis) กระดูกหัก (fractures) และการผ่าตัดกระดูก (orthopedic interventions)) ร่วมด้วย
- โรคต่อมไร้ท่อ (endocrinopathies) ก็มักจะทำให้กิจกรรมเอนไซม์ตับเพิ่มขึ้นได้ ระดับกลูโคคอร์ติคอยด์จากภายในร่างกาย (endogenous glucocorticoids) ที่สูง เช่น ภาวะต่อมหมวกไตชั้นนอกทำงานมากผิดปกติ (hyperadrenocorticism (Cushing’s disease)) จะเหนี่ยวนำกิจกรรมเอนไซม์ C-ALP ซึ่งเป็นลักษณะเฉพาะที่พบในความผิดปกตินี้ ซึ่งจากข้อเท็จจริงหากสัตวแพทย์ไม่พบการเพิ่มสูงขึ้นของเอนไซม์นี้ โอกาสที่สัตว์ป่วยจะมีภาวะต่อมหมวกไตชั้นนอกทำงานมากผิดปกติก็น้อยลง แต่ในการวินิจฉัยยังคงต้องขึ้นอยู่กับอาการแสดงทางคลินิก ผลการตรวจทางห้องปฏิบัติการและผลการทดสอบเฉพาะ (specific test) เช่น low-dose dexamethasone suppression test ที่ตรงกัน นอกจากนี้ความผิดปกติของต่อมไร้ท่ออื่นๆ เช่น ภาวะพาราไทรอยด์ทำงานเกิน (hyperparathyroidism) หรือเบาหวาน (diabetes mellitus) ก็อาจเป็นปัจจัยที่สามารถเพิ่มระดับเอนไซม์ตับได้เช่นเดียวกัน
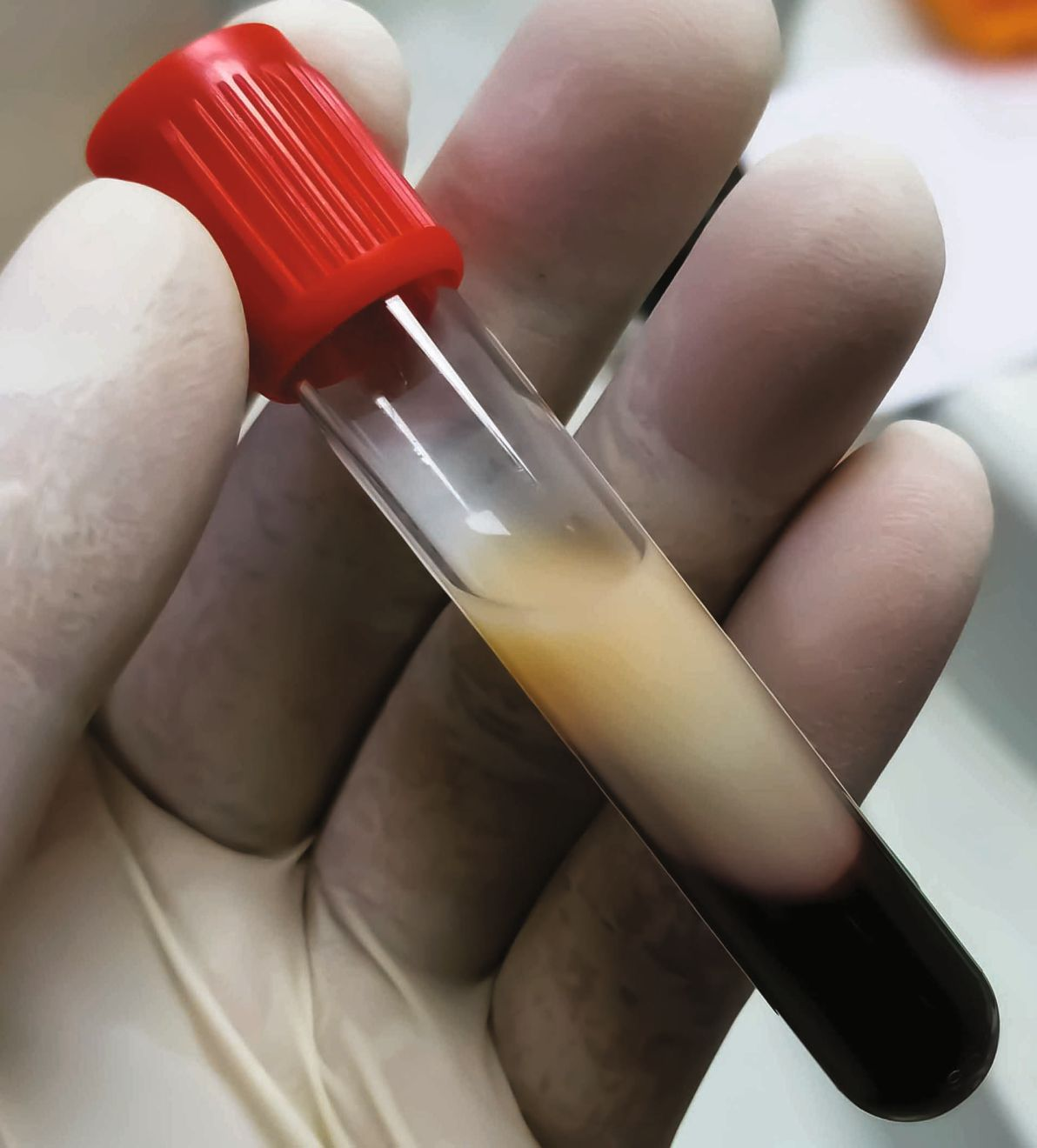
หัวใจสำคัญของการติดตามโรคเบาหวานคือการประเมินระดับกลูโคส (glucose level) อย่างไรก็ตามผู้ป่วยโรคเบาหวานมักมีการเผาผลาญไขมันที่ผิดปกติโดยส่งผลให้การเผาผลาญไขมันในตับเพิ่มขึ้น ดังนั้นการเฝ้าติดตามเอนไซม์ตับจึงเป็นประโยชน์ในการประเมินสถานะของโรค ในทางเซลล์วิทยา (cytologically) อาจพบภาวะไขมันพอกตับ (hepatic steatosis) โดยภาวะนี้จะพบได้ในแมวมากกว่าสุนัข การสะสมของไขมันในเซลล์ตับนั้นจะทำให้เซลล์ตับเสียหายและอาจพบระดับเอนไซม์ ALT หรือ ALP เพิ่มสูงขึ้น (ซึ่งเป็นตัวบ่งชี้ที่ไวต่อการตรวจจับภาวะไขมันพอกตับ (hepatic lipidosis) ในแมวเป็นพิเศษ) และตัวอย่างเลือดอาจแสดงให้เห็นภาวะไขมันในเลือดสูง (lipemia) อย่างชัดเจน (รูปภาพที่ 5)
ตามที่ได้อธิบายไว้ในข้างต้น ยากันชัก เช่น ยา phenobarbital สามารถกระตุ้นการผลิตเอนไซม์ ALP ได้ การประเมินระดับยาฟีโนบาร์บิทัล (phenobarbital levels) ระหว่างการรักษาจึงเป็นสิ่งสำคัญ เนื่องจากระดับยาที่มากกว่า 35 ไมโครกรัม/มล. จะเป็นพิษต่อตับ (hepatotoxic) ดังนั้นจึงแนะนำให้เฝ้าติดตามสุขภาพทั่วไปของตับในสุนัขที่ใช้ยา phenobarbital ต่อเนื่องปีละ 2 ครั้ง และเช่นเดิม ระดับเอนไซม์ตับที่อยู่ภายในช่วงค่าอ้างอิงไม่ได้ตัดประเด็น (rule out) เรื่องภาวะตับเสื่อมหน้าที่ลงอย่างมีนัยสำคัญ เพราะฉะนั้นสัตวแพทย์ควรทำการทดสอบกระตุ้นกรดน้ำดี (bile acid stimulation test) หากสงสัยว่าสุนัขที่ใช้ยากันชักมีภาวะตับทำงานผิดปกติ (liver dysfunction)
ฉันจำเป็นต้องตรวจประเมินปัจจัยการแข็งตัวของเลือด (clotting factors) ในกรณีที่สุนัขเป็นโรคตับหรือไม่ ?
ตับไม่เพียงแค่ผลิตปัจจัยในการแข็งตัวของเลือดเท่านั้นแต่ยังผลิตโปรตีนป้องกันการแข็งตัวของเลือด (anticoagulant proteins) ด้วย เช่น Protein S and Protein C, antithrombin และ plasminogen ดังนั้นการเปลี่ยนแปลงการทำงานของตับจึงส่งผลต่อการผลิตและการทำงานของโปรตีนที่กระตุ้นกระบวนการแข็งตัวของเลือด (procoagulant protein) และโปรตีนป้องกันการแข็งตัวของเลือด (anticoagulant proteins) ซึ่งอาจทำให้เกิดภาวะการแข็งตัวของเลือดผิดปกติ (coagulopathies) ตามมาตั้งแต่ระดับรุนแรง เช่น เลือดออกเอง (spontaneous bleeding) ไปจนถึงระยะเวลาของการแข็งเป็นลิ่มของเลือดนานขึ้นแบบไม่แสดงอาการทางคลินิกชัดเจน (subclinically prolonged clotting times) อย่างไรก็ตามการตอบสนองของสัตว์ป่วยแต่ละตัวนั้นยากต่อการคาดเดา โดยทั่วไปแล้วมวลตับ (hepatic mass) จะต้องลดลงอย่างมากและเกิดภาวะตับวายอย่างรุนแรง (severe liver failure) ตามมาจึงจะทำให้การสังเคราะห์ปัจจัยและโปรตีนที่ได้อธิบายไว้ในข้างต้นลดลงอย่างมีนัยสำคัญ โดยเนื่องจาก factor VII มีค่าครึ่งชีวิต (half-life) ที่สั้นที่สุด (6 ชั่วโมง) จากปัจจัยการแข็งตัวของเลือดทั้งหมด จึงคาดว่า prothrombin time (PT) จะเปลี่ยนแปลงตั้งแต่ในช่วงแรก
ในหลายกรณีที่สัตวแพทย์สงสัยว่าสัตว์ป่วยเป็นโรคตับ สัตวแพทย์จำเป็นต้องเจาะดูดเซลล์ด้วยเข็มขนาดเล็ก (fine-needle aspirates) หรือตัดชิ้นเนื้อ (biopsy) ที่ตับเพื่อนำไปส่งตรวจระบุลักษณะของโรคเพิ่มเติม แต่การตรวจประเมินปัจจัยการแข็งตัวของเลือด เช่น PT และ activated partial thromboplastin clotting time (aPTT) ก่อนจะทำการตัดชิ้นเนื้อจะช่วยให้สัตวแพทย์ประเมินความเสี่ยงในสัตว์ป่วยที่มีภาวะตับว่ายได้ง่ายขึ้น ถึงแม้ว่าการเชื่อมโยงผลตรวจกับแนวโน้มที่มีจะมีภาวะเลือดออกทางคลินิกที่อาจเกิดขึ้นนั้นจะไม่ใช่เรื่องง่ายก็ตาม ระยะเวลาของการแข็งเป็นลิ่มของเลือดที่นานขึ้นอย่างมากอาจเกี่ยวข้องกับภาวะเลือดออกเองหรือภาวะเลือดออกที่เกี่ยวข้องกับการตัดชิ้นเนื้อ (biopsy-related bleeding) แต่ในกรณีดังกล่าวบางครั้งก็พบว่าระยะเวลาของการแข็งเป็นลิ่มของเลือดอาจยาวนานขึ้นเพียงเล็กน้อยหรืออาจจะปกติก็ได้
ข้อสรุปที่ว่ากิจกรรมเอนไซม์ตับที่ปกติจะบ่งชี้ว่าตับมีสุขภาพที่ดีนั้นอาจไม่ถูกต้องทั้งหมด การแปลผลเอนไซม์ตับควรได้รับการประเมินควบคู่กับพารามิเตอร์การทำงานของตับและความสัมพันธ์กับประวัติและอาการแสดงทางคลินิกของสัตว์ป่วย
เกณฑ์วิธี (protocol) ที่ดีที่สุดสำหรับการทดสอบกระตุ้นกรดน้ำดี (bile acid stimulation test) คืออะไร ?
การทดสอบกระตุ้นกรดน้ำดีแบบไดนามิก (dynamic bile acid stimulation test) เป็นการทดสอบที่มีความไวสูงสุดในการประเมินกรดน้ำดีสำหรับภาวะตับเสื่อมการทำงานลงซึ่งเกี่ยวข้องกับการวัดระดับกรดน้ำดีขณะอดอาหาร (fasting bile acids) (โดยทั่วไปจะวัดหลังจากอดอาหาร 12 ชั่วโมง) และนำผลลัพธ์ที่เป็นค่าพื้นฐาน (baseline value) นี้มาเปรียบเทียบกับตัวอย่างเลือดที่เก็บ 2 ชั่วโมงหลังจากกินอาหารที่มีไขมันปริมาณปานกลาง การบริโภคอาหาร (food consumption) จะกระตุ้นการหดตัวของถุงน้ำดี (gallbladder contraction) และปล่อยกรดน้ำดีเข้าสู่ระบบไหลเวียนลำไส้-ตับ (enterohepatic circulation) ทั้งนี้แม้ว่าเวลาที่ถุงน้ำดีหดตัวจะไม่ชัดเจนจากค่าพื้นฐาน แต่ถุงน้ำดีก็มีแนวโน้มที่จะหดตัวจากการกินอาหารมากกว่า ด้วยเหตุนี้จึงทำให้สัตวแพทย์มองเห็นการทำงานของตับได้ดีขึ้น
การแปลผลการทดสอบกระตุ้นอาจเป็นเรื่องที่ค่อนข้างท้าทาย เนื่องจากสัตวแพทย์ต้องแน่ใจว่ามีการกินอาหารก่อนเป็นอันดับแรก อีกทั้งยังต้องแยกโรคระบบทางเดินอาหาร (gastrointestinal diseases) ที่อาจนำไปสู่ภาวะกระเพาะอาหารบีบตัวช้าเกินไปทำให้อาหารเกิดการคั่งค้าง (delayed gastric emptying) หรือลดการดูดซึมน้ำดีที่ลำไส้เล็กส่วนปลาย (ileal) ออกไปก่อน การหดตัวของถุงน้ำดีอาจเกิดขึ้นในช่วงเวลาที่ไม่สามารถคาดเดาได้และน้ำดีที่สะสมไว้บางส่วนก็อาจไม่ถูกปล่อยออกมา หรือถุงน้ำดีอาจไม่เต็มไปด้วยน้ำดีอย่างสมบูรณ์หลังจากน้ำดีถูกปล่อยออกมา ซึ่งทั้งหมดนี้อาจส่งผลต่อผลการทดสอบได้เช่นกัน ระบบไหลเวียนลำไส้-ตับยังได้รับอิทธิพลจากกระบวนการเผาผลาญของแบคทีเรียในลำไส้ (intestinal bacteria) หลักการทั่วไป (A general rule of thumb) ในการแปลผลการทดสอบก็คือให้ประเมินค่าสูงสุดที่ได้มาโดยไม่ต้องคำนึงว่าจะเป็นตัวอย่างค่าพื้นฐานหรือตัวอย่างที่ถูกกระตุ้น หากทั้งสองตัวอย่างแสดงให้เห็นว่ากรดน้ำดีมีค่ามากกว่า 25 ไมโครโมล/ลิตร ก็แสดงว่าสามารถวินิจฉัยภาวะตับเสื่อมการทำงานลงได้ กรดน้ำดีขณะอดอาหารอาจเพิ่มขึ้นในภาวะท่อน้ำดีคั่งหรือโรคตับทุติยภูมิอื่นๆ หากค่ากรดน้ำดีมากกว่า 50 ไมโครโมล/ลิตร ก็ยังถือว่ามีแนวโน้มที่จะเป็นความผิดปกติที่เกี่ยวข้องกับโรคตับปฐมภูมิ หากผลการตรวจระดับกรดน้ำดีก่อนและหลังกินอาหาร (pre- and postprandial bile acids) อยู่ระหว่าง 20-50 ไมโครโมล/ลิตร ก็จะถือว่าผลการทดสอบยังไม่ชัดเจนและควรวิเคราะห์ซ้ำอีกครั้งใน 2-3 สัปดาห์ อีกทั้งยังต้องพิจารณาร่วมกับผลตรวจทางห้องปฏิบัติการและ/หรือภาพวินิจฉัย (diagnostic imaging) อื่นๆด้วย สุดท้ายนี้สัตวแพทย์ควรตระหนักไว้เสมอว่าผลการตรวจกรดน้ำดีที่ผิดปกติอาจเกิดขึ้นได้เนื่องจากโรคตับและทางเดินน้ำดี (hepatobiliary diseases) ต่างๆซึ่งเป็นผลที่ไม่จำเพาะเจาะจง (non-specific finding)
เนื่องจากค่าชีวเคมี (biochemistry profile) หลายค่าที่ตรวจในสุนัขมักจะประกอบไปด้วยพารามิเตอร์ต่างๆมากมายที่สามารถใช้ประเมินการทำงานของตับได้ ดังนั้นจึงเป็นสิ่งสำคัญที่สัตวแพทย์จะต้องทราบว่าเมื่อใดที่ผลการทดสอบผิดปกติอย่างมีนัยสำคัญและเมื่อใดที่ผลการทดสอบภายในช่วงค่าอ้างอิงไม่เพียงพอที่จะตัดประเด็นการวินิจฉัยที่อาจเป็นไปได้ สัตวแพทย์จึงควรแปลผลเอนไซม์ตับควบคู่กับประวัติสัตว์ป่วยและอาการแสดงทางคลินิก และทำการทดสอบบางอย่างซ้ำอีกครั้ง รวมไปถึงหาทางเลือกในการวินิจฉัยเพิ่มเติมเมื่อใดก็ตามที่เหมาะสม
Further reading
- E. Villiers, Ristić J. BSAVA Manual of Canine and Feline Clinical Pathology, 3rd ed. Gloucester, British Small Animal Veterinary Association, 2016
- Stockham SL, Scott MA. Fundamentals of Veterinary Clinical Pathology, 2nd edition. Ames, IA; Blackwell Publishing, 2008
- Lawrence YA, Steiner JM. Laboratory evaluation of the liver; a review. Vet. Clin. North Am. Small Anim. Pract. 2017;47(3):539-553. Doi: 10.1016/j.cvsm.2016.11.005. Epub 2017 Jan 4.
- Konstantinidis AO, Patsikas MN, Papazoglou LG, et al. Congenital portosystemic shunts in dogs and cats: classification, pathophysiology, clinical presentation and diagnosis. Vet. Sci. 2023;10(2):160. Doi: 10.3390/vetsci10020160.
- Charalambous M, Muñana K, Patterson EE, et al. ACVIM Consensus Statement on the management of status epilepticus and cluster seizures in dogs and cats. J. Vet. Intern. Med. 2024;38(1):19-40. Doi: 10.1111/jvim.16928. Epub 2023 Nov 3.
Stefanie Klenner-Gastreich
DVM, Dip. ECVCP, Scil Animal Care Company GmbH, Viernheim, Germany
Germany
Dr. Klenner-Gastreich graduated in 2004 from the University of Veterinary Medicine Hannover Foundation in Germany. After completing her doctoral thesis in gastroenterology, she undertook an internship in the Small Animal Clinic at the Justus-Liebig-University in Gießen, Germany, where she also did her residency. She gained her Diplomate from the European College of Veterinary Clinical Pathology (ECVCP) in 2011. The following year she accepted a post dedicated to Point-of-Care diagnostics as the Scientific Product Manager Laboratory Diagnostic for Scil Animal Care, an Antech company. She is currently Director International Reference Laboratories at Scil and a EBVS® European Specialist in Veterinary Clinical Pathology.
Other articles in this issue
แบ่งปันบนโซเชียลมีเดีย