การรักษาผิวหนังอักเสบอะโทปีในสุนัข
สัตวแพทย์มีโอกาสพบสุนัขที่มาด้วยโรคผิวหนังอักเสบภูมิแพ้อะโทปีได้บ่อยครั้งในการทำงาน บทความนี้จะเป็นการทบทวนแนวทางการรักษาที่มีและเน้นย้ำความสำคัญของการรักษาแบบผสมผสาน(multi-modal approach) (แปลโดย น.สพ. พีระ มานิตยกุล)
Article
ประเด็นสำคัญ
โรคผิวหนังอักเสบภูมิแพ้อะโทปี(canine atopic dermatitis; CAD)หรืออะโทปีในสุนัขเป็นโรคเรื้อรังที่พบได้บ่อยและส่งผลกระทบต่อคุณภาพชีวิตของสุนัขและเจ้าของ
ปัจจัยต่างๆที่ส่งผลต่อความคันควรได้รับการจัดการพร้อมกันเพื่อให้การรักษาประสบความสำเร็จโดยเฉพาะเมื่อมีการปะทุของอาการโรคผิวหนัง
ยากดภูมิคุ้มกันและ allergen-specific immunotherapy มีบทบาทสำคัญในการควบคุมอะโทปีในสุนัขโดยสามารถใช้ร่วมกันได้
การวางแผนการรักษาควรจัดทำขึ้นสำหรับสุนัขแต่ละตัวและปรับให้เหมาะสมตามฤดูกาล สุขภาพของสุนัข หรือเมื่อมีการปะทุของอาการโรคผิวหนัง
บทนำ
โรคผิวหนังอักเสบภูมิแพ้อะโทปีหรืออะโทปีในสุนัข(canine atopic dermatitis; CAD) เป็นความผิดปกติของผิวหนังที่มีสาเหตุจากสารก่อภูมิแพ้(allergen)ในสิ่งแวดล้อมเป็นส่วนมาก ตัวอย่างเช่นไรฝุ่น ละอองจากหญ้า ต้นไม้และวัชพืชเป็นต้น สาเหตุการเกิดโรคมาจากหลายปัจจัย เริ่มจากความผิดปกติของเกราะป้องกันผิวชั้นนอก(epidermal barrier dysfunction)ร่วมกับการทำงานที่ผิดปกติของระบบภูมิคุ้มกันนำไปสู่การแสดงออกที่ผิวหนังในสุนัขที่มีประวัติพันธุกรรมของโรค CAD กรณีส่วนใหญ่เริ่มพบอาการที่สุนัขอายุน้อยแต่สร้างปัญหาผิวหนังอักเสบและอาการคันไปตลอดชีวิต
แนวทางการรักษา CAD มีหลายวิธีโดยแต่ละวิธีมีข้อดีและข้อเสียแตกต่างกันไปในแง่ของประสิทธิภาพและผลต่อสุขภาพสุนัข บทความนี้จะนำเสนอแนวทางโดยใช้หลักเหตุผลเพื่อหาจุดเริ่มต้นในการรักษา ความท้าทายไม่ได้อยู่ที่การรักษาให้ประสบความสำเร็จแต่ยังรวมถึงหลีกเลี่ยงการปะทุของอาการโรคผิวหนังด้วย จากที่กล่าวมาทำให้การรักษา CAD จำเป็นต้องใช้การรักษาผสมผสาน(รูป 1) สุนัขจะปลอดอาการเมื่อสามารถควบคุมอาการทางคลินิกและป้องกันการปะทุของอาการโรคผิวหนังได้ ทางเลือกในการรักษาจะขึ้นอยู่กับความจำเป็นของสุนัขแต่ละตัวและความรุนแรงของโรค
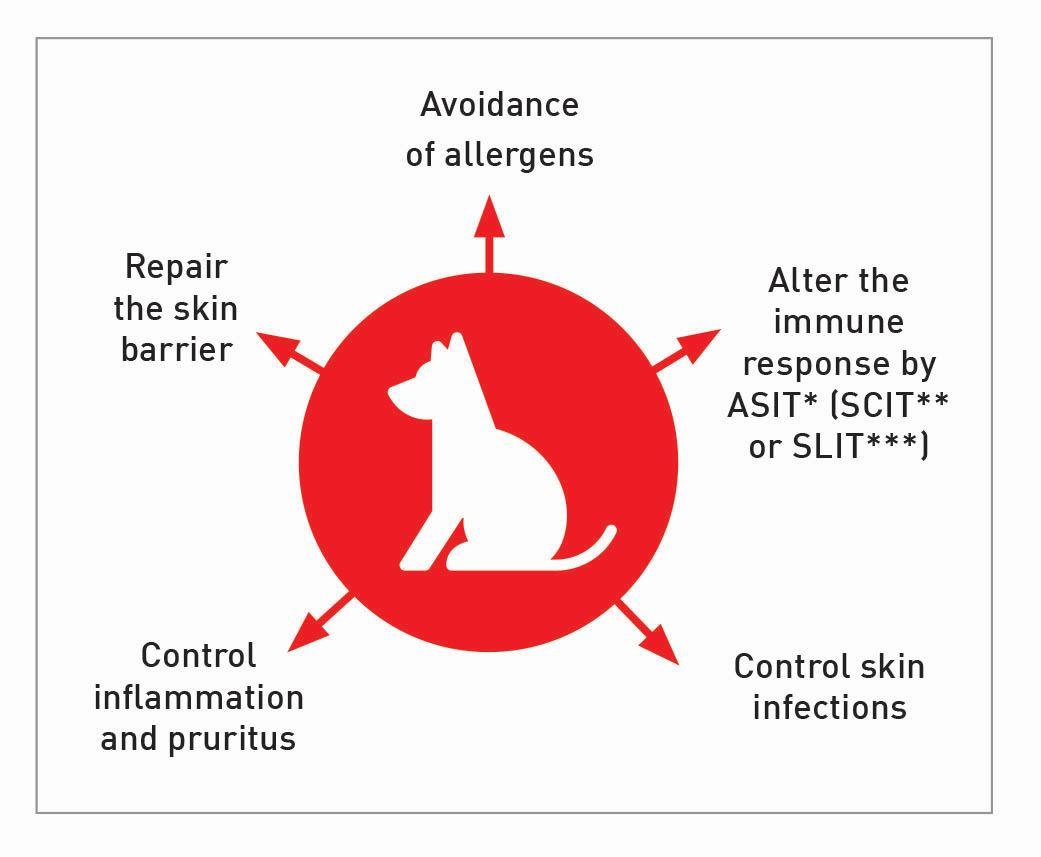
[* Allergen-specific immunotherapy** Subcutaneous immunotherapy*** Sublingual immunotherapy ]
การหลีกเลี่ยงสารก่อภูมิแพ้(avoidance of allergens)
สารก่อภูมิแพ้ที่มีความเกี่ยวข้องกับการเกิดอะโทปีที่พบบ่อยที่สุดคือไกลโคโปรตีนของไรฝุ่นและละอองเกสรต่างๆทำให้การหลีกเลี่ยงทำได้ยากมาก ในการทดลองที่ปราศจากกลุ่มควบคุมโดยใช้ยาฆ่าไรกลุ่ม benzyl benzoate ฉีดพ่นในสิ่งแวดล้อมเพื่อลดปริมาณไรฝุ่นพบว่าสุนัขที่เป็นอะโทปีมีอาการที่ดีขึ้น 1 นอกจากนี้ยังมีสเปรย์สำหรับพ่นในสิ่งแวดล้อมที่ผลิตขึ้นมาขายสำหรับคนซึ่งมีส่วนประกอบของโพรไบโอติกส์ที่สามารถสร้างเอนไซม์ซึ่งมีคุณสมบัติในการจับกับโปรตีนในอุจจาระของไรฝุ่น ความสัมพันธ์ระหว่างการลดสารก่อภูมิแพ้จากไรฝุ่นและอาการทางคลินิกที่ดีขึ้นของสุนัขที่เป็นอะโทปียังต้องการการศึกษาเพิ่มเติมที่มีกลุ่มควบคุมเพื่อยืนยันสมมติฐานนี้ ในทางเดียวกันการใช้ที่นอนที่มีคุณสมบัติป้องกันไรฝุ่น การดูดฝุ่นอย่างสม่ำเสมอ และการซักเครื่องนอนที่อุณหภูมิ 60 องศาเซลเซียสอาจมีส่วนช่วยลดการที่สุนัขมีโอกาสสัมผัสกับสารก่อภูมิแพ้ในจากไรฝุ่นได้
กรณีหนึ่งที่พบได้ยากคือการที่สุนัขแสดงอาการแพ้ต่อเศษผิวหนังชั้นนอกของสัตว์เลี้ยงชนิดอื่นในบ้านเช่น นกแก้วหรือหนูตะเภา หากเป็นเช่นนั้นแนะนำให้แยกที่อยู่อาศัย
หากสุนัขเป็นอะโทปีที่มีสาเหตุโน้มนำจากอาหารจะมีสารก่อภูมิแพ้จากทั้งอาหารและสิ่งแวดล้อมที่ส่งผลให้มีอาการทางผิวหนัง 2 สารก่อภูมิแพ้ในอาหารจะมีบทบาทมากเมื่อมีอาการปะทุของอาการโรคผิวหนัง ดังนั้นการทดสอบอาหารจึงมีความสำคัญอย่างมากในสุนัขที่เป็นอะโทปี หากสามารถระบุได้ว่าสุนัขมีการแพ้อาหารจะทำให้การหลีกเลี่ยงสารก่อภูมิแพ้ในอาหารทำได้ง่าย
การเสริมเกราะป้องกันผิวหนัง (restoring the skin barrier)
สุนัขที่ป่วยด้วยโรคอะโทปีนั้นเป็นที่ทราบกันดีว่าเกิดความผิดปกติที่เกราะป้องกันผิวหนังชั้น epidermis ส่งผลให้เกิดการสูญเสียน้ำผ่านชั้น epidermis เพิ่มมากขึ้น (transepidermal water loss; TEWL) สุนัขบางสายพันธุ์อาจพบผิวหนังมีลักษณะแห้งและมีรังแคมาก(xerosis) การเสริมเกราะป้องกันผิวหนังด้วยการทาสารให้ความชุ่มชื้น(moisturizer) เช่น glycerol glycerin propylene glycol panthenol และ urea จะช่วยเพิ่มความสามารถในการกักเก็บน้ำของชั้น epidermis โดยจะมีประสิทธิภาพดีมากหากใช้หลังการอาบน้ำ แนวคิดนี้ได้มีการทดสอบและให้ผลดีในสุนัขที่มีความผิดปกติของเกราะป้องกันผิวหนังชั้น epidermis แบบเรื้อรัง 3 ผลิตภัณฑ์ที่มีส่วนประกอบของ phytosphingosine และ ophytrium ซึ่งเป็นสารสกัดจากธรรมชาติที่พบได้ในรากของ Japanese mondo grass อาจช่วยให้ฟื้นฟูเกราะป้องกันผิวหนัง ลดอาการคัน และลดการเพิ่มจำนวนของเชื้อแบคทีเรียที่ผิวหนังชั้น epidermis ได้ 4
สุนัขที่เป็นอะโทปียังพบว่าเกิดความผิดปกติที่ intercellular lipid lamellae ในชั้น stratum corneum ของผิวหนัง การให้กรดไขมันจำเป็น(essential fatty acids; EFAs)โดยการกินไม่ว่าจะเป็นในรูปอาหารเสริมหรือเสริมลงในอาหารที่สุนัขกินมีการนำมาใช้และได้ผลการรักษาที่แตกต่างกันไป ในการศึกษาที่ดีชิ้นหนึ่งพบว่าสามารถลดขนาดยา prednisolone ชนิดกินได้อย่างมีนัยสำคัญในสุนัขที่ได้รับ EFAs เป็นเวลา 12 สัปดาห์ 5 อีกทางเลือกหนึ่งคือการใช้อาหารที่มีส่วนผสมที่ครบถ้วนในการเสริมเกราะป้องกันผิวหนัง EFAs ในรูปแบบยาภายนอกชนิดหยดหลังพบว่าให้ผลที่น่าพอใจเช่นเดียวกัน 6 แต่อาจมีค่าใช้จ่ายค่อนข้างสูงหากต้องใช้เป็นระยะเวลานาน ยาภายนอกชนิดอื่นได้แก่แชมพู สเปรย์ และโลชั่นที่มีส่วนประกอบของกรดไขมันและเซราไมด์ได้มีการนำมาใช้ในสุนัขที่ป่วยด้วยอะโทปีแต่ยังมีความไม่สม่ำเสมอในแง่ของประสิทธิภาพ สัตวแพทย์พึงระลึกว่าการเสริมเกราะป้องกันให้กับผิวชั้นนอกไม่ว่าจะด้วยวิธีใดอาจช่วยลดการเข้าถึงผิวหนังของสารก่อภูมิแพ้ในสิ่งแวดล้อมได้
การคุมการติดเชื้อแทรกซ้อนที่ผิวหนัง(controlling secondary skin infections)
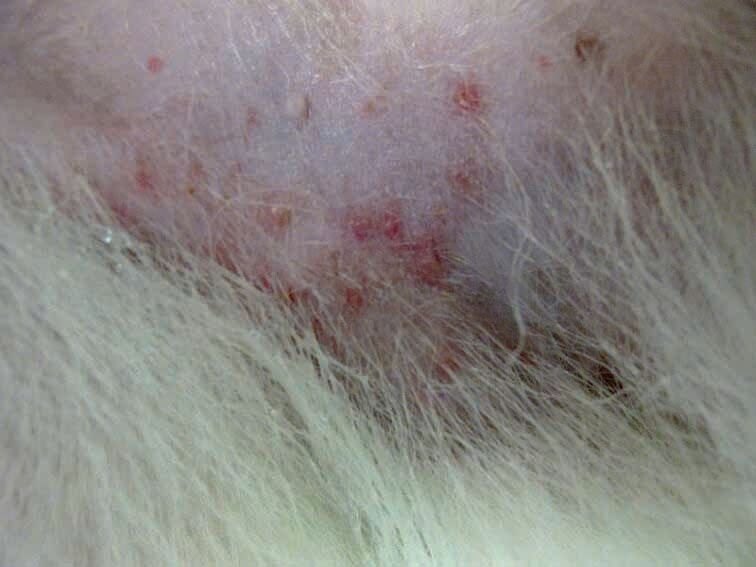
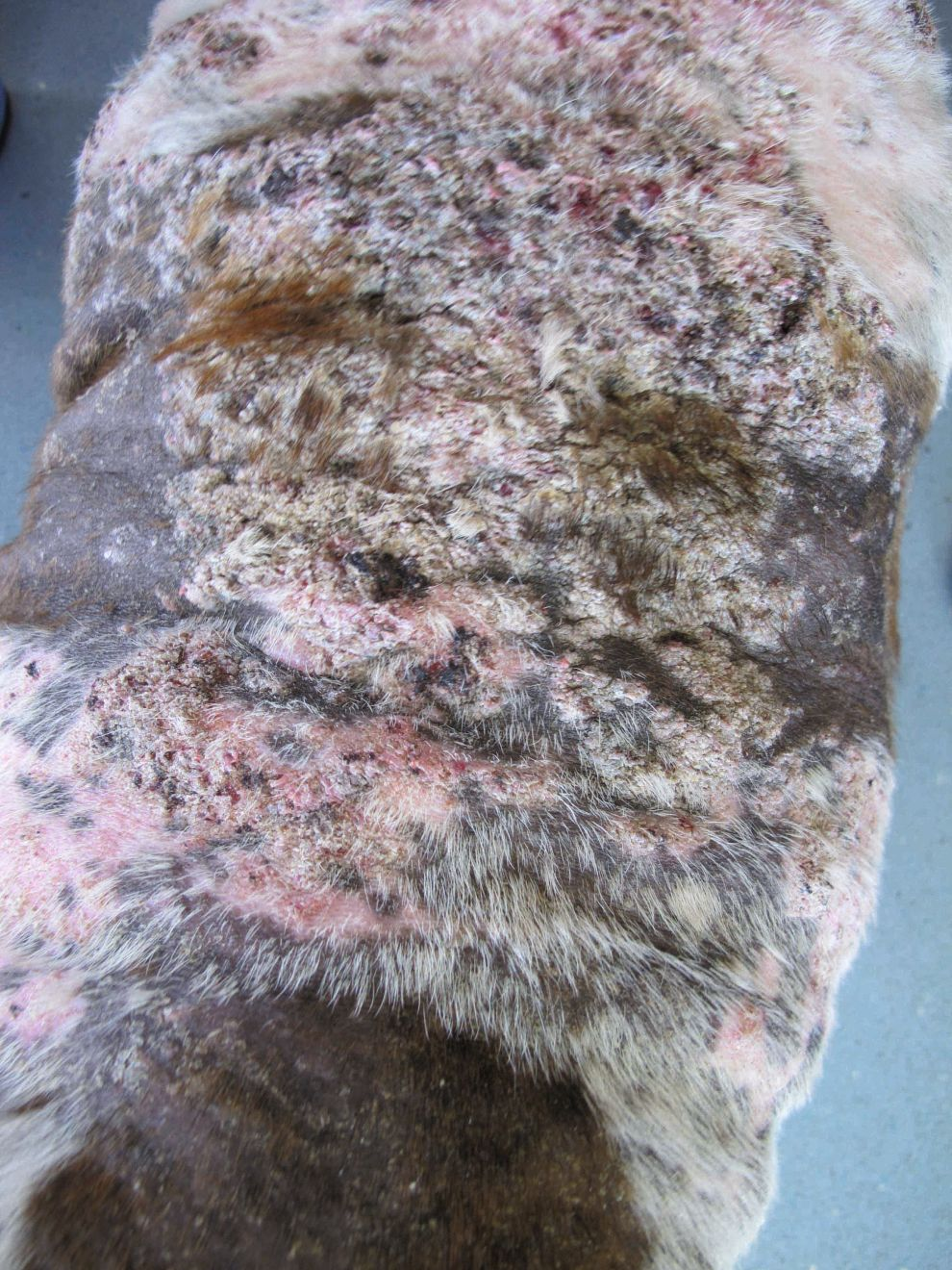
สุนัขส่วนมากที่ป่วยด้วยอะโทปีมีโอกาสกลับมามีอาการของโรคผิวหนังซ้ำเช่น superficial pyoderma papule pustule collarette squame และ seborrhea (รูป 2) การเพิ่มจำนวนของเชื้อแบคทีเรียก่อโรค Staphylococci spp. (มักเป็น S. pseudintermedius) มีมากขึ้นเทียบกับผิวหนังที่สุขภาพดีซึ่งอาจเป็นผลจากการที่โปรตีนที่ออกฤทธิ์ต้านเชื้อโรคบริเวณผิวหนังทำงานได้แย่ลง เมื่อพบการปะทุของอาการโรคผิวหนังในกรณีอะโทปีจะพบว่าเกิดความไม่สมดุลของแบคทีเรียโดยมีปริมาณเชื้อ Staphylococci เพิ่มมากขึ้น รอยโรคที่ทุเลาหลังการใช้ยาปฏิชีวนะแสดงถึงการคืนสมดุลของแบคทีเรียบนผิวหนัง 7
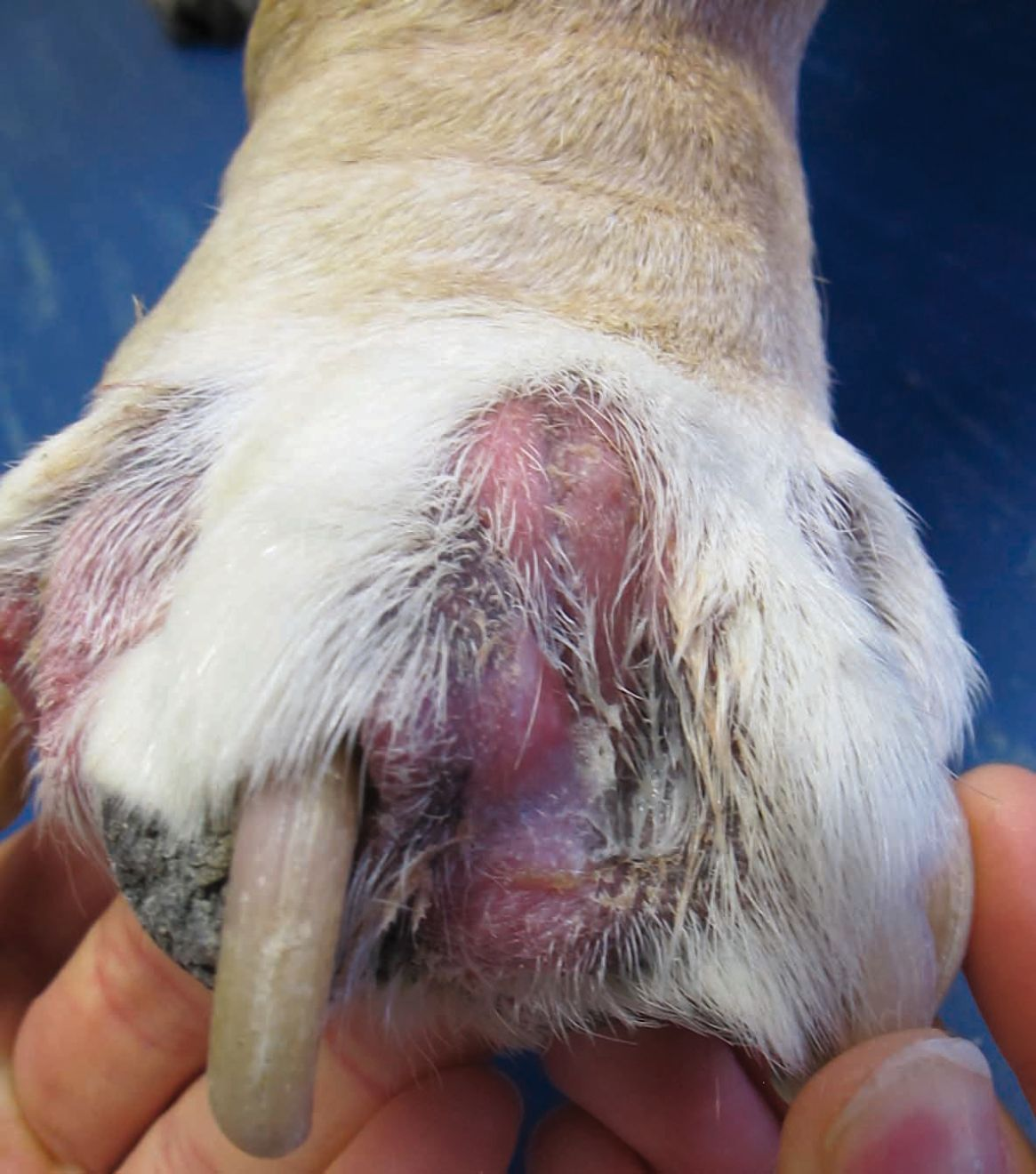
ร้อยละ 40 ของสุนัขที่เป็นอะโทปีพบการกลับมาเป็นซ้ำของการติดเชื้อยีสต์ Malassezia pachydermatis ที่ผิวหนังซึ่งจะมีกลิ่นแรง ผิวมัน รังแค และ paronychia ร่วมกับเล็บกลายเป็นสีน้ำตาล(รูป 3) การแพ้แบบ type 1 hypersensitivity ต่อ Malassezia สามารถพบได้ทำให้เกิดอาการคันอย่างมาก 8 การติดเชื้อแบคทีเรียหรือยีสต์แทรกซ้อนจำเป็นต้องได้รับการควบคุม สามารถทำได้โดยการใช้ยาภายนอกที่ออกฤทธิ์ต้านเชื้อจุลชีพซึ่งอาจอยู่ในรูปแบบแชมพู มูส สเปรย์ แผ่นเช็ดทำความสะอาดหรือเจล การฟอกด้วยแชมพูที่มีส่วนผสมของ chlorhexidine เข้มข้น 3% ให้ผลที่ดีในการจัดการเชื้อแบคทีเรียและยีสต์เช่นเดียวกับแชมพูที่มีส่วนผสมของ chlorhexidine 2% และ miconazole 9 การอาบน้ำด้วยแชมพูยาสัปดาห์ละ 2 ครั้งเพียงพอต่อการรักษา แต่ถ้ารอยโรคมีความรุนแรงมากอาจต้องใช้ยาภายนอกถี่มากขึ้นในช่วงแรกของการรักษา ผู้เขียนบทความนิยมให้อาบน้ำด้วยแชมพูยาทุกวันในสัปดาห์แรก วันเว้นวันในสัปดาห์ถัดมาและลดลงเหลือ 2 ครั้งต่อสัปดาห์ อีกวิธีหนึ่งที่ให้ผลดีพอกันคือการอาบน้ำด้วยแชมพูยาสัปดาห์ละครั้งร่วมกับการใช้ยาภายนอกชนิดอื่นเช่น มูส เจล หรือสเปรย์ที่บริเวณรอยโรคสัปดาห์ละ 2 ครั้ง
การเลือกใช้ยาปฏิชีวนะชนิดกินควรใช้เมื่อพบว่ามีลักษณะของ deep pyoderma ได้แก่ มีการกระจายตัวของรอยโรคแบบ generalized มีลักษณะเป็นฝีฝักบัว(furunculosis) หรือเมื่อเจ้าของสุนัขไม่สามารถใช้ยาภายนอกได้ตามคำแนะนำ ตัวเลือกของการใช้ยาปฏิชีวนะอาจทำตามผลการเพาะเชื้อหาความไวต่อยาปฏิชีวนะ หรืออาจเลือกใช้ยาปฏิชีวนะตามหลักที่ปฏิบัติกันได้แก่ clindamycin 10 mg/kg q12h cephalosporine(cephalexin) 10-30 mg/kg q8-12h หรือ amoxicillin- clavulanic acid 12.5 mg/kg q12h สัตวแพทย์ควรให้สุนัขกินยาปฏิชีวนะต่อเนื่องจนกว่าอาการและผล cytology ที่บ่งบอกถึง pyoderma จะหายไป ควรหลีกเลี่ยงการกลับมาใช้ยาปฏิชีวนะชนิดเดิมซ้ำเพราะอาจเพิ่มความเสี่ยงของการเกิดเชื้อดื้อยา การใช้ยาฆ่าเชื้อราชนิดกินเช่น ketoconazole 10 mg/ kg q24h หรือ 5 mg/kg q12h และ itraconazole 5 mg/kg q24h ควรสงวนไว้ใช้ในรายที่มีการติดเชื้อยีสต์รุนแรง เพราะยีสต์มีโอกาสเกิดการดื้อยาฆ่าเชื้อรากลุ่ม azole ได้แต่พบได้น้อย 10 นอกจากนี้สัตวแพทย์ยังต้องพึงระลึกถึงผลข้างเคียงจากการใช้ยาต่างๆโดยเฉพาะ ketoconazole

ความท้าทายในการรักษา CAD ไม่ได้อยู่ที่เพียงการรักษาให้หายจากอาการปัจจุบันแต่ยังต้องป้องกันการปะทุของอาการโรคผิวหนังต่างๆ เราจึงต้องใช้การรักษาแบบผสมผสานเพื่อจัดการกับ CAD
การควบคุมการอักเสบของผิวหนังและอาการคัน(controlling skin inflammation and pruritus)
ยารักษาอาการอักเสบและลดอาการคันที่ได้ผลดีในสุนัขที่เป็นอะโทปีได้แก่สเตียรอยด์ cyclosporine oclacitinib และ lokivetmab ซึ่งจะกล่าวถึงแต่ละตัวในลำดับถัดไป การป้องกันเห็บหมัดอย่างสม่ำเสมอช่วยลดการคันได้อย่างมาก ไม่มีหลักฐานที่สรุปได้ว่ายาแอนตี้ฮิสตามีน type 1 สามารถออกฤทธิ์ควบคุมอาการคันชนิดเรื้อรังและเฉียบพลันที่มีสาเหตุจาก CAD [11] หากจำเป็นต้องเลือกใช้อาจใช้ cetirizine 0.5-1.0 mg/kg q24h หรือ hydroxyzine 2 mg/kg q12h [12]
ยากลุ่มสเตียรอยด์ (glucocorticosteroids)
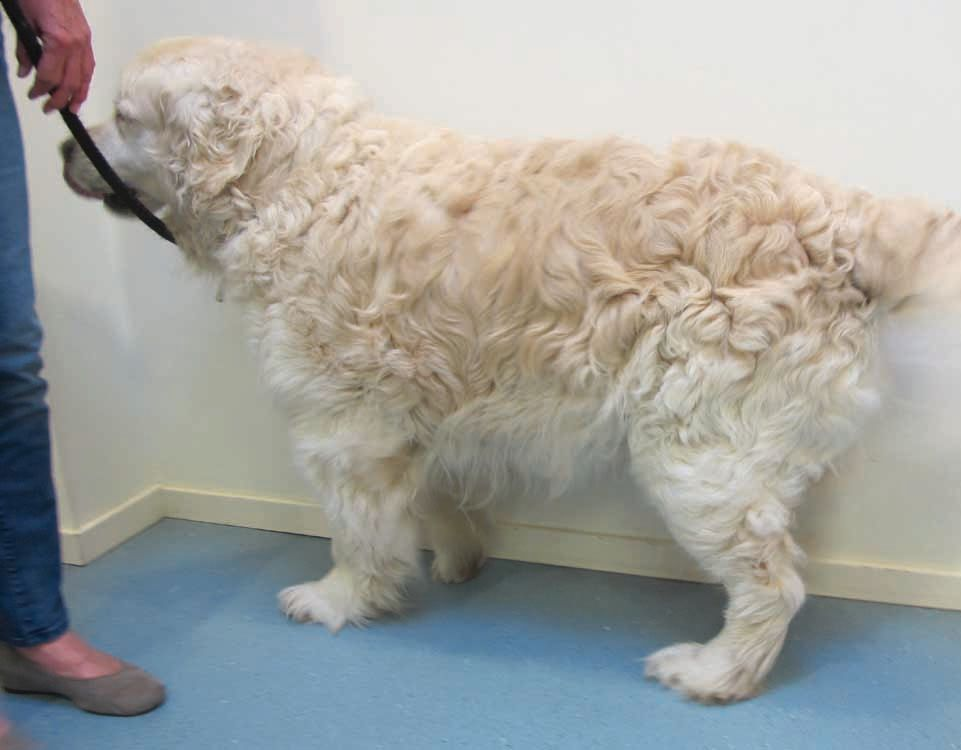
ยากลุ่มสเตียรอยด์(glucocorticosteroids หรือ GC) ออกฤทธิ์ผ่านการยับยั้ง transcription factor ทำให้กดการแสดงออกของยีนที่ส่งผลต่อการทำงานของ cytokine cytokine receptor adhesion molecule pro-inflammatory enzyme และ chemotactic protein จากที่กล่าวมาทำให้ยากลุ่มนี้ยับยั้งการทำงานของเซลล์อักเสบและลดอาการคันได้อย่างรวดเร็วซึ่งสามารถนำมาใช้ในระยะเฉียบพลันและระยะเรื้อรังของ CAD อย่างไรก็ตามจากการที่ยากลุ่มนี้ส่งผลกระบวนการต่างๆของเซลล์จึงทำให้พบผลข้างเคียงได้ง่ายหากมีการใช้เป็นระยะเวลานาน ผลข้างเคียงที่พบได้บ่อยได้แก่ กินน้ำมาก ปัสาวะมาก กินอาหารมาก กล้ามเนื้อและผิวหนังฝ่อลีบ เพิ่มความเสี่ยงต่อการติดเชื้อแบคทีเรียและเชื้อรา ไรขี้เรื้อนขุมขน และ iatrogenic hyperadrenocorticism(รูป5) ไม่แนะนำให้ใช้รูปแบบยากินเป็นระยะเวลานานแต่ควรใช้ยาสเตียรอยด์ที่ออกฤทธิ์สั้นในกรณีที่อาการทางคลินิกรุนแรง ยา prednisolone ชนิดกินขนาด 0.5-1 mg/kg q24h หรือ methylprednisolone 0.4-0.8 mg/kg q24h สามารถให้ได้เป็นระยะเวลาตั้งแต่ 5-14 วัน ขึ้นกับการตอบสนองของสุนัข จากนั้นจึงลดขนาดยาลงเรื่อยๆจนให้ได้วันเว้นวันเมื่ออาการดีขึ้น
รูปแบบของ GC ที่แนะนำให้ใช้คือยาทาภายนอก สเปรย์ และโลชั่น สเปรย์ที่มีส่วนผสมของ triamcinolone acetonide และ hydrocortisone aceponate พบว่ามีประสิทธิภาพสูงในการควบคุมรอยโรคเฉพาะที่ [13] เริ่มจากการใช้ยาภายนอกทุกวันเป็นเวลาประมาณ 2 สัปดาห์หรือจนอาการทางคลินิกลดลงจากนั้นเหลือสัปดาห์ละ 2 ครั้ง hydrocortisone aceponate อาจเหนี่ยวนำให้เกิดการสลายของผิวหนังชั้น dermis ผ่านการยับยั้ง collagen 1 และ 3 pro-peptide แต่ในการทดลองหนึ่งไม่พบการฝ่อของผิวหนังที่สังเกตได้จากการใช้ยาภายนอกเป็นเวลานาน(สองครั้งต่อสัปดาห์) [14] ยาคนในรูปแบบของครีม betamethasone และ mometasone furoate พบว่าให้ผลดีเช่นเดียวกันทางสัตวแพทย์ เป้าหมายสูงสุดของการรักษายะยาวด้วย GC ที่เป็นยาภายนอกคือการลดการปะทุของอาการโรคผิวหนังและยืดระยะเวลาปลอดอาการให้นานขึ้นแทนที่จะเน้นรักษาอาการเมื่อสุนัขเป็นมากจนสังเกตได้ [14]
Oclacitinib
Oclacitinib ทำหน้าที่เป็น janus kinase(JAK) inhibitorโดย JAK จัดเป็น nonreceptor tyrosine kinase ที่สามารถถูกกระตุ้นให้ทำงานได้โดย cytokine receptor หลายชนิด พบว่ามี JAK ในสัตว์เลี้ยงลูกด้วยนมทั้งหมด 4 ชนิดได้แก่ JAK1 JAK2 JAK 3 และ tyrosine kinase 2 ทำหน้าที่ควบคุมการแสดงออกของยีนเกี่ยวกับกระบวนการอักเสบ oclacitinib ทำการจับอย่างจำเพาะกับ cytokine ที่อาศัย JAK1 (และ JAK2 บางส่วน) ทำให้ลดผลของการอักเสบและการแพ้ของ cytokine ลงได้ จัดว่าเป็นยาที่ส่งผลต่อกระบวนการอักเสบและการแพ้อย่างกว้างขวางใน CADจากการที่ oclacitinib ออกฤทธิ์ได้อย่างรวดเร็วในการควบคุมอาการคันทำให้มีประโยชน์ในการควบคุมอาการคันที่ปะทุขึ้นมาอย่างเฉียบพลัน การให้จะเริ่มที่วันละ 2 ครั้งเป็นเวลา 14 วัน จากนั้นลดเหลือวันละ 1 ครั้ง(ขนาด 0.4-0.6 mg/kg) การให้ยาวันละ 2 ครั้งจำเป็นอย่างมากในรายที่มีอาการของโรคผิวหนังอักเสบเรื้อรัง ตัวยามีความปลอดภัยในการใช้ระยะยาวเพื่อการรักษา CAD ในสัตว์ที่อายุ 12 เดือนขึ้นไป [15] ตามทฤษฏีแล้ว oclacitinib อาจมีฤทธิ์กดภูมิคุ้มกันเมื่อใช้ในขนาดที่สูงกว่าคำแนะนำ [16] ผลของยาในสุนัขที่มีความไวต่อยาชนิดนี้อาจนำไปสู่การติดเชื้อฉวยโอกาส viral papilloma หรือไรขี้เรื้อนขุมขน หากเกิดกรณีดังกล่าวควรหยุดใช้ยาทันที สุนัขที่ได้รับยา oclacitinib ไม่จำเป็นต้องรับการตรวจเลือด ค่าเคมีในเลือด หรือการเพาะเชื้อปัสสาวะเป็นต่อเนื่องหลังได้รับยา [17]
ยา cyclosporine และ tacrolimus
Cyclosporine A อยู่ในกลุ่ม calcineurin inhibitor ที่ออกฤทธิ์กดภูมิคุ้มกันอย่างจำเพาะเจาะจงโดยการจับกับ intracellular immunophilins ส่งผลให้เกิดการยับยั้ง cytokine interleukin-2(IL-2) นำไปสู่การลดการเพิ่มจำนวนของ T cell และการผลิตแอนติบอดี้ของ B cell ที่อาศัย T-helper cell นอกจากนี้ cyclosporine ยังมีกระบวนการออกฤทธิ์อย่างกว้างขวาง ขนาดที่แนะนำคือ 5 mg/kg q24h อย่างไรก็ตามการทำงานของยาจะเห็นผลช้า โดยอาจใช้เวลานาน 4-8 สัปดาห์ก่อนที่อาการคันและผิวหนังอักเสบจะลดลง ยาชนิดนี้จึงควรใช้เพื่อการรักษาในระยะประคองอาการ การใช้ยาชนิดอื่นที่ออกฤทธิ์ได้เร็วกว่าร่วมกับ cyclosporine ในช่วงแรกของการรักษาจะให้ผลที่ดีและมีความปลอดภัยสูง อาจใช้ยา prednisolone ขนาด 1 mg/kg q24h เป็นเวลา 1 สัปดาห์จากนั้นลดลงเป็นวันเว้นวันนาน 2 สัปดาห์ในช่วง 3 สัปดาห์แรกของการใช้ยา cyclosporine 18 ในทางเดียวกันอาจใช้ oclacitinib ขนาด 0.4-0.6 mg/kg q12h เป็นเวลา 2 สัปดาห์จากนั้นลดลงเหลือวันละครั้งเป็นเวลา 1 สัปดาห์ 17 หลังจากที่สุนัขที่เป็นอะโทปีมีอาการดีขึ้นจึงค่อยๆลดขนาดของ cyclosporine ลง(ลดลง 1 mg/kg ทุก 2 สัปดาห์) หรือให้วันเว้นวันจนกว่าจะได้ขนาดที่ต่ำที่สุดที่ยังให้ผลการรักษาที่ดีได้ ผลข้างเคียงของ cyclosporine พบได้ในร้อยละ 30 ของสุนัขและสามารถหายได้เองได้แก่การอาเจียนและถ่ายเหลว พบมากในช่วงสัปดาห์แรกของการใช้ยาโดยเฉพาะในสุนัขที่มีระบบทางเดินอาหารที่อ่อนไหว ผู้เขียนบทความนิยมให้ในขนาดที่ต่ำก่อนในช่วงแรกเช่น 1.5 mg/kg q24h เป็นเวลา 3 วันจากนั้นจึงเพิ่มเป็น 3 mg/kg q24h ต่ออีก 3 วัน การให้ยาพร้อมกับอาหารอาจช่วยลดผลข้างเคียงต่อระบบทางเดินอาหารได้ ผลข้างเคียงอื่นที่พบได้น้อยกว่าซึ่งอาจขึ้นกับขนาดของยาที่ใช้ได้แก่ gingival hyperplasia ขนขึ้นมากเกินไป(รูป 6) การติดเชื้อราชนิดฉกฉวยโอกาส hyperplastic verrucous lesion และ psoriasiform-lichenoid-like dermatitis อย่างไรก็ตามผลข้างเคียงเหล่านี้มักหายได้เองหลังหยุดใช้ยา
Tacrolimus เป็นยาอีกชนิดในกลุ่ม calcineurin inhibitor ที่สามารถลดความรุนแรงของรอยโรคที่ผิวหนังได้หลังทาไปหลายสัปดาห์ 19 ถึงแม้ว่า tacrolimus อาจก่อความระคายเคืองต่อผิวหนังได้ในช่วงแรกของการทายา แต่สุนัขโดยมากทนต่อการทายาที่มีความเข้มข้นร้อยละ 0.1 วันละ 2 ครั้งได้ดี


Lokivetmab
Lokivetmab มีคุณสมบัติเป็น anti-canine interleukin-31 monoclonal antibody ซึ่งมีการทำงานที่แคบและเป็นยารักษาอะโทปีที่ออกฤทธิ์อย่างจำเพาะเจาะจงมากที่สุดและมีผลข้างเคียงน้อยที่สุด ตัวยาทำหน้าที่ยับยั้ง canine IL-31 ซึ่งเป็น cytokine ที่เกี่ยวข้องกับการคัน ความแตกต่างในการทำงานระหว่าง lokivetmab และ oclacitinib อยู่ที่ lokivetmab จะจับกับ IL-31 ก่อนที่จะมีโอกาสจับกับตัวรับทำให้หยุดกระบวนการก่อให้เกิดอาการคันที่ระดับโมเลกุล การให้ยาทำโดยการฉีด lokivetmab เข้าใต้ผิวหนังเดือนละครั้งขนาด 1-2 mg/kg (ขึ้นกับการขึ้นทะเบียนยาในแต่ละประเทศ) สุนัขบางตัวตอบสนองต่อยาในขนาดสูงได้ดีกว่า อาการของโรคจะดีขึ้นใน 4-8 สัปดาห์ ตัวยามีครึ่งชีวิตที่นานมากและมีความปลอดภัยเมื่อใช้ร่วมกับยาอื่นที่ใช้รักษา CAD ประสิทธิภาพของยาในการลดอาการคันและความรุนแรงของรอยโรค(ใช้ pruritus visual analog score; PVAS และ canine atopic dermatitis extent and severity index; CADESI) หลัง 28 วันพบว่าไม่ด้อยกว่าการใช้ยา cyclosporine lokivetmab เห็นผลค่อนข้างรวดเร็ว(ลด PVAS มากกว่าร้อยละ 50 ในสุนัขที่เป็นอะโทปีร้อยละ 77) แต่ประสิทธิภาพโดยรวมหลังการรักษา 9 เดือนพบว่าเหลือร้อยละ 59 20
Annette van der Lee
DVM, PhD, Dip. ECVD
ราชอาณาจักรเนเธอร์แลนด์
หลังจากสำเร็จการศึกษาในปี 2004 van der Lee ได้ฝึกในคลินิกหมุนวนในฐานะสัตวแพทย์ฝึกหัดในคลินิกผิวหนังที่ Utrecht University เธอได้รับใบอนุปริญญาบัตร ECVD ในปี 2009 และได้ทำงานในศูนย์ส่งต่อในเนเธอร์แลนด์นับจากนั้น แต่ในขณะเดียวกันเธอได้ร่วมทำงานวิจัยกับคลินิกสัตวแพทย์ผิวหนัง และสำเร็จการศึกษาระดับปริญญาเอกจากวิทยานิพนธ์เรื่อง T cells and immunomodulation in canine atopic dermatitis ในปี 2014 เธอได้เข้าร่วม IVC Evidensia group ในปี 2017 ที่ซึ่งเธอดำรงตำแหน่ง หัวหน้าหน่วยโรคผิวหนังในเนเธอร์แลนด์ในปัจจุบัน
แหล่งอ้างอิง
- Swinnen C, Vroom M. The clinical effect of environmental control of house dust mites in 60 house dust mite-sensitive dogs. Vet Dermatol 2004;15(1):31-36.
- Picco F, Zini E, Nett C, et al. A prospective study on canine atopic dermatitis and food-induced allergic dermatitis in Switzerland. Vet Dermatol 2008;19(3):150-155.
- Panzuti P, Vidmont E, Fantini O, et al. A moisturizer formulated with glycerol and propylene glycol accelerates the recovery of skin barrier function after experimental disruption in dogs. Vet Dermatol 2020;31:344-e89.
- Ollivier E, Zemirline C, Marchand L, et al. Effect of the ingredient A97614A1 on the adhesion and biofilm formation of Staphylococcus pseudintermedius in a model of reconstructed canine epidermis. In; Proceedings, 62nd BSAVA Congress, Birmingham, 2019.
- Saevik BK, Bergvall K, Holm BR, et al. A randomized, controlled study to evaluate the steroid sparing effect of essential fatty acid supplementation in the treatment of canine atopic dermatitis. Vet Dermatol 2004;15:137-145.
- Popa I, Remoue N, Osta B, et al. The lipid alterations in the stratum corneum of dogs with atopic dermatitis are alleviated by topical application of a sphingolipid-containing emulsion. Clin Exp Dermatol 2012;37(6):665-671.
- Bradley CW, Morris DO, Rankin SC, et al. Longitudinal evaluation of the skin microbiome and association with microenvironment and treatment in canine atopic dermatitis. J Invest Dermatol 2016;136(6):1087-1089.
- Morris DO, DeBoer DJ. Evaluation of serum obtained from atopic dogs with dermatitis attributable to Malassezia pachydermatis for passive transfer of immediate hypersensitivity to that organism. Am J Vet Res 2003;64(3):262-266.
- Maynard L, Rme CA, Viaud S. Comparison of two shampoos for the treatment of canine Malassezia dermatitis: a randomised controlled trial. J Small Anim Pract 2011;52(11):566-572.
- Kano R, Yokoi S, Kariya N, et al. Multi-azole-resistant strain of Malassezia pachydermatis isolated from a canine Malassezia dermatitis. Med Mycol 2019; 57(3):346-350.
- Olivry T, DeBoer DJ, Favrot C, et al. Treatment of canine atopic dermatitis: 2010 clinical practice guidelines from the International Task Force on Canine Atopic Dermatitis. Vet Dermatol 2010;21:233-248.
- Olivry T, DeBoer DJ, Favrot C, et al. Treatment of canine atopic dermatitis: 2015 updated guidelines from the International Committee on Allergic Diseases of Animals (ICADA). BMC Vet Res 2015;11:210.
- Nuttall T, Mueller R, Bensignor E, et al. Efficacy of a 0.0584% hydrocortisone aceponate spray in the management of canine atopic dermatitis: a randomised, double blind, placebo-controlled trial. Vet Dermatol 2009;20:191-198.
- Loureno AM, Schmidt V, So Braz B, et al. Efficacy of proactive long-term maintenance therapy of canine atopic dermatitis with 0.0584% hydrocortisone aceponate spray: a double-blind placebo-controlled pilot study. Vet Dermatol 2016; 27:88-92.
- Cosgrove SB, Cleaver DM, King VL. Long-term compassionate use of oclacitinib in dogs with atopic and allergic skin disease: safety, efficacy and quality of life. Vet Dermatol 2015;26:171-e35.
- Banovic F, Gordon H, Tarigo J, et al. Modulatory effects of oclacitinib on in vitro canine T-cell proliferation and cytokine production. Vet Dermatol 2019;30(1):17-e6.
- Panteri A, Strehlau G, Helbig R, et al. Repeated oral dose tolerance in dogs treated concomitantly with ciclosporin and oclacitinib for three weeks. Vet Dermatol 2016; 27:22-e7.
- Dip R, Carmichael J, Letellier I, et al. Concurrent short-term use of prednisolone with cyclosporine A accelerates pruritus reduction and improvement in clinical scoring in dogs with atopic dermatitis. BMC Vet Res 2013;9:173.
- Bensignor E, Olivry T. Treatment of localized lesions of canine atopic dermatitis with tacrolimus ointment: a blinded randomized controlled trial. Vet Dermatol 2005;16: 52-60.
- Moyaert H, Van Brussel L, Borowski S, et al. A blinded, randomized clinical trial evaluating the efficacy and safety of lokivetmab compared to ciclosporin in client-owned dogs with atopic dermatitis. Vet Dermatol 2017;28(6):593-e145.
- Keppel K, Campbell K, Zuckermann F, et al. Quantitation of canine regulatory T cell populations, serum interleukin-10 and allergen-specific IgE concentrations in healthy control dogs and canine atopic dermatitis patients receiving allergen-specific immunotherapy. Vet Immunol Immunopathol 2008;123:337-344.
- Loewenstein C, Mueller RS. A review of allergen-specific immunotherapy in human and veterinary medicine. Vet Dermatol 2009;20(2):84-98.
- Hobi S, Mueller RS. Efficacy and safety of rush immunotherapy with alum-precipitated allergens in canine atopic dermatitis. Tierarztl Prax Ausg K Kleintiere Heimtiere 2014;42(3):167-173.
- DeBoer DJ, Verbrugge M, Morris M. Clinical and immunological responses of dust mite sensitive, atopic dogs to treatment with sublingual immunotherapy (SLIT). Vet Dermatol 2016;27(2):82-7e23.
- Timm K, Mueller RS, Nett-Mettler CS. Long-term effects of intralymphatic immunotherapy (ILIT) on canine atopic dermatitis. Vet Dermatol 2018;29(2):123-e49.
บทความอื่นๆ ในประเด็นนี้
แบ่งปันบนโซเชียลมีเดีย