Атиповий гіпоадренокортицизм у собак
Хвороба Аддісона може бути не першим діагнозом, який спадає на думку, коли у собаки з'являються шлунково-кишкові ознаки, але цю можливість не слід ігнорувати, як описує Ромі Гайлманн.

Ключові моменти
У собак з типовим гіпоадренокортицизмом зазвичай спостерігається очевидна клінічна картина та клініко-патологоанатомічні ознаки, що дає змогу легко діагностувати захворювання..
Атиповий гіпоадренокортицизм часто асоціюється з неспецифічними хронічними шлунково-кишковими симптомами, які то посилюються, то слабшають, і які можуть бути спровоковані або загострені стресовими подіями, і часто реагують на симптоматичне лікування.
Обстеження собак з атиповим гіпоадренокортицизмом вимагає «детективного підходу» до пацієнта, щоб поставити правильний діагноз.
Обидві форми гіпоадренокортицизму, зазвичай, пов'язані з дуже добрим довгостроковим прогнозом.
Вступ
Гіпоадренокортицизм у своїй типовій формі (хвороба Аддісона) — часто простий діагноз, тобто класичні симптоми та клініко-патологічні зміни є очевидними й добре узгоджуються з анамнезом і симптомами пацієнта, тому може здатися дивним, що гастроентеролог повинен розглянути ймовірність наявності цього стану під час обстеження. Однак клінічна картина у хворих собак, особливо зі спонтанним атиповим гіпоадренокортицизмом, може бути неспецифічною. Вона часто включає хронічні шлунково-кишкові прояви, що періодично посилюються або слабшають, можуть провокуватися чи загострюватися під впливом стресових факторів і зазвичай добре реагують на інфузійну терапію та симптоматичне лікування. Отже, гіпоадренокортицизм, особливо його атипова форма, може бути схожим на первинні захворювання шлунково-кишкового тракту (ШКТ), тому його не слід відкидати під час диференціальної діагностики в собак із нечіткими й неспецифічними проявами з боку ШКТ.
Дещо про історію питання
Термінологія
Гіпоадренокортицизм, або хвороба Аддісона, розвивається, коли кора надниркових залоз не здатна виробляти й виділяти достатню кількість ендогенних глюкокортикоїдів і, особливо в типових випадках, мінералокортикоїдів. (Рис 1) [1]. На відміну від типового гіпоадренокортицизму з характерними клінічними та клініко-патологічними проявами, спричиненими одночасним дефіцитом глюкокортикоїдів і мінералокортикоїдів, випадки атипового гіпоадренокортицизму в собак складніше діагностувати, оскільки ця форма недостатності надниркових залоз не тільки є менш поширеною, але й має маловиразну, неспецифічну клінічну картину [1],[2]. Можливим є перехід від атипового до типового гіпоадренокортицизму, у звʼязку з чим за атиповими випадками слід спостерігати в динаміці [2]. У собак із типовим перебігом, коли є ймовірність розвитку клінічної декомпенсації з дегідратацією та гіповолемічним шоком (аддісоновий криз), прогресування від дефіциту одного глюкокортикоїду можна лише припустити, ґрунтуючись на ретроспективному враженні про повільний початок захворювання й пов’язані з ним клінічні симптоми. Однак при типових випадках гіпоадренокортицизму таке прогресування важко довести. Повідомляють про породну схильність у стандартних пуделів, португальських водяних собак, новошотландських ретриверів, м’якошерстих пшеничних тер’єрів і бородатих колі, але собаки будь-якої породи й віку можуть страждати на будь-яку форму цього захворювання [2],[3],[4],[5]. Порівняно з типовими випадками, собаки з атиповим гіпоадренокортицизмом зазвичай є старшими за віком.

Етіологія
Гіпоадренокортицизм може бути спричинений будь-яким станом, за якого знижується вироблення й вивільнення гормонів корою надниркових залоз. Найчастіше його спричиняє імуноопосередкований процес, який зменшує функціональну масу кори надниркових залоз, що продукує гормони, зокрема її середньої й внутрішньої частини, що продукує глюкокортикоїди (пучкову зону) [5],[6],[7]. Серед інших, менш поширених або рідкісних причин первинного гіпоадренокортицизму — гранулематозні стани (наприклад, грибкові захворювання), судинні причини (наприклад, крововиливи, ішемія), відкладення амілоїду (особливо в порід, схильних до розвитку амілоїдозу), некроз або метастатична неоплазія [8],[9],[10]. Вторинний (центральний) гіпоадренокортицизм може розвинутися внаслідок станів, що впливають на вироблення й вивільнення кортикотропін-рилізинг-гормону (КРГ) гіпоталамусом та/або адренокортикотропного гормону (АКТГ) гіпофізом, зокрема запалень, інфекцій, травм і неоплазій [1],[11].
Патофізіологія
За типової форми гіпоадренокортицизму некомпенсований дефіцит глюкокортикоїдів і мінералокортикоїдів призводить до характерних електролітних зрушень у плазмі (гіперкаліємія, гіпонатріємія) [1]. На відміну від цього, за атипової форми спостерігається або лише дефіцит глюкокортикоїдів, або комбінований дефіцит кортикостероїдів (глюкокортикоїдів і мінералокортикоїдів) без електролітних зрушень, що зумовлено незалежними від альдостерону компенсаторними механізмами (наприклад, ниркова компенсація) [1],[2].
Виявлення гіпоадренокортицизму — захворювання, яке може бути схоже на що завгодно
Клінічні симптоми
З огляду на різні ефекти глюкокортикоїдів, що вивільнюються ендогенно, на організм (рис. 2), зокрема на роботу серця й шлунково-кишкового тракту [12],[13], у собак з атиповим гіпоадренокортицизмом зазвичай спостерігаються нечіткі, неспецифічні прояви, що посилюються й слабшають, як-от зниження активності (наприклад, під час виконання вправ на аджиліті), млявість, слабкість, відсутність апетиту, втрата ваги або низький відсоток жирової тканини в тілі (рис. 3), блювання (з гематемезисом або без нього) або зригування, діарея (можливо, геморагічна), біль у животі й нетримання сечі [1],[2],[13],[14].


Лабораторна діагностика
Мінімальна база даних повинна містити повний аналіз крові, біохімічний аналіз сироватки й аналіз сечі (з оцінкою осаду сечі та, якщо показано, бактеріальним посівом, тестуванням на чутливість до антимікробних препаратів і співвідношенням білка до креатиніну в сечі). У собак з атиповим гіпоадренокортицизмом часто можна виявити незначні й неспецифічні зміни. Однак легка нерегенеративна анемія є поширеним явищем, оскільки кортизол посилює еритропоез і зменшує оборотність еритроцитів, але відсутність очікуваної стресової лейкограми (або навіть протилежні тенденції в кількості окремих клітин, що часто називають «зворотною стресовою лейкограмою») може бути ледь помітним показником, і його можна пропустити, якщо не проводити спеціальну оцінку (блок 1). Враховуючи протилежний вплив глюкокортикоїдів на кількість нейтрофілів і лімфоцитів, співвідношення нейтрофілів до лімфоцитів ≤2,3 повинно викликати підозру на гіпоадренокортицизм [15].
Блок 1. Відповідні гематологічні дані у 6-річної суки з гіпоадренокортицизмом. Зверніть увагу на наявність «зворотної стресової лейкограми» з помірним лімфоцитозом, еозинофілією та зниженим співвідношенням нейтрофілів до лімфоцитів (NLR) 1,31. Будь-яке співвідношення NLR ≤2,3 повинно викликати підозру на гіпоадренокортицизм
| Параметр | Результат | Од. вим. | Референсний інтервал |
|---|---|---|---|
| Еритрограма | |||
| Гематокрит | 33.8 | % | 37.3-61.7 |
| Середній об’єм еритроцитів | 61.2 | фл | 61.6-73.5 |
| Середній вміст гемоглобіну в еритроциті | 22.3 | пг | 21.2-25.9 |
| Лейкограма | |||
| Кількість нейтрофілів | 7.53* | x 109/л | 2.95-11.64 |
| Кількість лімфоцитів | 5.75* | x 109/л | 1.05-5.10 |
| Кількість моноцитів | 0.67 | x 109/л | 0.16-1.12 |
| Кількість еозинофілів | 1.25 | x 109/л | 0.06-1.23 |
| Кількість базофілів | 0.07 | x 109/л | 0.00-0.10 |
| Тромбоцити | |||
| Кількість тромбоцитів | 368 | тис./мкл |
148-484 |
| Середній об’єм тромбоцитів | 9.7 | фл |
8.7-13.2 |
*N/L-R = 1.31
Можуть бути виявлені гіпоглікемія (або концентрація глюкози в крові в нижніх межах норми), гіпоальбумінемія, гіпохолестеринемія, підвищення активності печінкових ферментів із підвищенням ферментів за гепатоцелюлярним типом, тобто підвищення аланінамінотрансферази (АЛТ) сироватки крові перевищує підвищення лужної фосфатази (ЛФ), а також легкою або помірною преренальною азотемією [1]. У таких випадках доцільно розглянути можливість виключення гіпоадренокортицизму перед застосуванням інвазивнішого діагностичного підходу, що передбачає загальну анестезію. Це важливо, оскільки стрес, пов’язаний з інвазивними процедурами, може потенційно поставити собаку в небезпечну для життя ситуацію декомпенсованого гіпоадренокортицизму, якщо не виявити цей стан. Гіперкаліємія й гіпонатріємія, які часто супроводжуються зниженням співвідношення натрію до калію (Na/K <27), є характерними ознаками типової форми гіпоадренокортицизму, але відсутні в разі атипової форми (блок 2) [4]. Цифрові інструменти охорони здоров’я, зокрема алгоритми, що враховують результати декількох рутинних досліджень, можуть покращити виявлення атипових випадків гіпоадренокортицизму в майбутньому [16].
Блок 2. Біохімічний аналіз сироватки крові з електролітами собаки породи боксер (рис. 3). За винятком легкої гіпоальбумінемії та низьких концентрацій холестерину й глюкози в сироватці крові, біохімічний аналіз сироватки крові цього собаки був без особливостей, і виникла підозра на ентеропатію з втратою білка.
| Параметр | Результат | Од. вим. | Референсний інтервал |
|---|---|---|---|
| Глюкоза | 97 | мг/дл | 57-126 |
| Холестерин | 167 | мг/дл | 139-398 |
| Симетричний диметиларгінін | 11 | мкг/дл | 0-14 |
| Креатинін | 1.1 | мг/дл | 0.5-1.5 |
| Креатинін і азот сечовини крові | 21 | мг/дл | 9-29 |
| Фосфат | 1.1 | ммоль/л | 0.9-1.7 |
| Кальцій | 2.3 | ммоль/л | 2.1-2.9 |
| АЛТ | 72 | од./л | 25-122 |
| Лужна фосфатаза | 37 | од./л | 14-147 |
| Загальний білок | 5.9 | г/дл | 5.4-7.6 |
| Альбумін | 2.3 | г/дл | 2.8-4.3 |
| Білірубін | 0.2 | мг/дл | 0-0.4 |
| Натрій | 145 | ммоль/л | 142-153 |
| Калій | 4.2 | ммоль/л | 3.9-5.8 |
Гормональний профіль
Вимірювання базової концентрації кортизолу в сироватці крові є корисним скринінговим тестом (блок 3). Визначення базового порогового рівня 2 мкг/дл (55 нмоль/л) виключає діагноз (чутливість 100%, специфічність 63–78%) гіпоадренокортицизму (блок 4) [17],[18]. Якщо базовий рівень становить <2 мкг/дл, слід провести тест зі стимуляцією АКТГ для діагностики або виключення гіпоадренокортицизму [1],[17],[18]. У цьому тесті рівень кортизолу в сироватці крові <2 мкг/дл є діагностичним, а рівень >6 мкг/дл - виключає гіпоадренокортицизм. Тест зі стимуляцією АКТГ низькими дозами (із використанням косинтропіну в дозі 1 мкг/кг в/в замість стандартної дози 5 мкг/кг) є ефективним для діагностування гіпоадренокортицизму в собак [19]. Вимірювання концентрації ендогенного АКТГ (еАКТГ) можна використовувати для підтвердження й подальшої класифікації гіпоадренокортицизму як первинного або вторинного (блок 5) [1],[15]. Первинний гіпоадренокортицизм (наприклад, надниркового походження) асоціюється з нормальною або високою концентрацією еАКТГ, тоді як вторинний гіпоадренокортицизм (наприклад, центрального походження за участю гіпоталамуса та/або гіпофіза) асоціюється з невизначуваною або низькою концентрацією еАКТГ.
Блок 3. Панель щитоподібної залози та шлунково-кишкова панель собаки породи боксер з атиповим гіпоадренокортицизмом на рис. 3. Виявлено низьку концентрацію загального й вільного тироксину, гіперкобаламінемію (без попереднього прийому препаратів) і гіпокортизолемію (нижче порогової концентрації в 55 нмоль/л, що використовується для скринінгу гіпоадренокортицизму). За цими результатами слід провести тест зі стимуляцією АКТГ.
| Параметр | Результат |
Од. вим. |
Референсний інтервал |
|---|---|---|---|
| Панель щитоподібної залози | |||
| Загальний T44 | 0.8 | мкг/дл | 1.0-4.0 |
| Вільний T44 | < 0.3 | нг/дл | 0.6-3.7 |
| Шлунково-кишкова панель | |||
| Специфічна ліпаза підшлункової залози собак | 142 | мкг/л | 0-200 |
| cTLI (трипсиноподібна імунореактивність у собак) | 37 | мкг/л | 8.5-35 |
| Кобаламін | 1 355 | пмоль/л | 173-599 |
| Фолат | 25.9 | нмоль/л | 21.1-54 |
| Кортизол (вихідний рівень) |
6.5
|
нмоль/л | 25-125 |


Співвідношення кортизолу до креатиніну в сечі (СКК, англ. UCCR) останнім часом привернуло увагу в діагностиці гіпоадренокортицизму в собак, а низький рівень СКК (≤2, виміряний радіоімунним методом, або ≤10, виміряний методом хемілюмінесцентного імуноаналізу) виявився високочутливим і специфічним для того, щоб відрізнити уражених собак від собак із захворюванням, схожим на гіпоадренокортицизм [20].
Дефіцит мінералокортикоїдів без гіперкаліємії та/або гіпонатріємії, який, як вважають, компенсується переважно нирковими механізмами, можна виявити шляхом вимірювання сироваткового альдостерону до й після стимуляції АКТГ (блок 6). За допомогою цього тесту можна диференціювати випадки атипового гіпоадренокортицизму з дефіцитом лише глюкокортикоїдів від комбінованого дефіциту кортикостероїдів у собак без електролітних змін [21]. Аналіз крові на функцію щитоподібної залози в собак із гіпоадренокортицизмом може показати підвищений рівень ТТГ в сироватці крові, а в деяких випадках — знижений рівень тироксину (блок 3); це не свідчить про істинний гіпотиреоз, і рівні нормалізуються впродовж декількох тижнів (до 4 місяців) після початку лікування гіпоадренокортицизму [22].
Блок 6. Рівні кортизолу й альдостерону в сироватці крові до та після стимуляції АКТГ в собаки породи боксер (рис. 3). Ні концентрація кортизолу, ні концентрація альдостерону в сироватці крові не зросла після стимуляції АКТГ, що підтверджує як глюкокортикоїдний, так і (компенсований) мінералокортикоїдний дефіцит у цього собаки.
| Параметр | Результат |
Од. вим. |
Референсний інтервал |
|---|---|---|---|
| Тест стимуляції секреції АКТГ (вихідний рівень) | |||
| Кортизол (вихідний рівень) | < 2.8 | нмоль/л | 25-125 |
| Кортизол (після стимуляції АКТГ) |
< 2.8
|
нмоль/л |
> 165
|
| Тест стимуляції секреції АКТГ (альдостерон у сироватці крові) | |||
| Альдостерон (вихідний рівень) | < 20 | пмоль/л | 0-393 |
| Альдостерон (після стимуляції АКТГ) | < 20 | пмоль/л | 82-859 |
Діагностична візуалізація
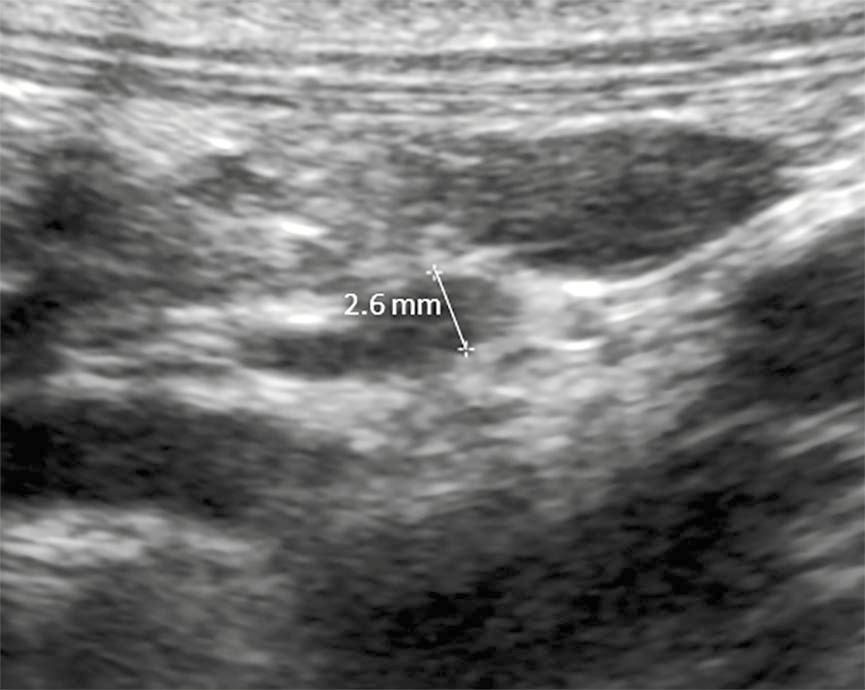
Рентгенографія грудної клітки та черевної порожнини в собак із гіпоадренокортицизмом зазвичай не дає результатів, за винятком оцінки наявності мегаезофагусу, пов’язаного з гіпоадренокортицизмом, але її можна використовувати для виключення деяких диференціальних діагнозів. Ультразвукове дослідження черевної порожнини, зокрема ретельна оцінка обох надниркових залоз, часто також не є показовим, але може виявити гіпоадренокортицизм за малого діаметра надниркової залози (рис. 4). Ультразвукове дослідження також рекомендують у випадках сумнівів для діагностики або виключення неоплазії надниркових залоз, інфаркту або крововиливу [1].
Лікування атипового гіпоадренокортицизму
Початок лікування
Собаки з атиповим гіпоадренокортицизмом зазвичай є клінічно стабільними, і їх можна лікувати амбулаторно. Однак, ознаки зневоднення під час фізичного огляду вимагають принаймні короткого періоду стаціонарного лікування з інфузійною замісною терапією (із використанням збалансованого розчину електролітів) і додаткового симптоматичного лікування (наприклад, застосування протиблювотних і гастропротекторних препаратів) за показаннями. Гіпоглікемію слід коригувати внутрішньовенним введенням глюкози (розчин декстрози), також слід контролювати рівень глюкози в крові.
Преднізолон (або преднізон) є препаратом першої лінії для заміщення ендогенного дефіциту глюкокортикоїдів [1],[2],[3]. Глюкокортикоїди швидкої дії (наприклад, дексаметазон, гідрокортизон) частіше використовують для інтенсивної замісної глюкокортикоїдної терапії в пацієнтів з аддісоновим кризом. Преднізон або преднізолон спочатку [1],[2]. вводять у низькій протизапальній дозі (0,3-0,5 мг/кг п/о кожні 12–24 години) упродовж кількох днів (1,2). Після цієї короткої індукційної фази дозу поступово знижують до найнижчого можливого («фізіологічного») рівня, який досі ефективно усуває ендогенний дефіцит глюкокортикоїдів, не призводячи до явних побічних ефектів, і продовжують лікування в режимі підтримувальної терапії. Підбір оптимальної дози для конкретного собаки потребує певного часу (і терпіння з боку власника), але зазвичай вона становить 0,05–0,2 мг/кг п/о кожні 24 години залежно від розміру та віку собаки (блок 7). Залежно від характеру й темпераменту собаки, у періоди очікуваного стресу можна розглянути можливість короткочасного збільшення підтримувальної дози преднізону / преднізолону [1],[2].
Блок 7. Рекомендовані коригування дози глюкокортикоїдів з огляду на клінічні симптоми й підозру на недостатнє дозування або надмірне введення.
|
• Помітні побічні ефекти глюкокортикоїдів → Зменшення дози (приблизно на 10–25%) • Рецидив клінічних симптомів (млявість, анорексія, діарея) → збільшення дози (приблизно на 50%) |
|
• Очікуваний значний стрес (наприклад, випробування на аджиліті, святковий феєрверк, планове хірургічне втручання)
→ Розгляньте можливість короткочасного збільшення дози (приблизно на 100–200%) для окремих собак |
Замісна терапія мінералокортикоїдами показана у випадках типового гіпоадренокортицизму (тобто для собак, у яких спостерігаються електролітні зміни, що вказують на супутній дефіцит мінералокортикоїдів), але ймовірність її наявності слід ретельно розглядати в собак із діагнозом атипового гіпоадренокортицизму залежно від ендогенного мінералокортикоїдного статусу. Якщо концентрація альдостерону в сироватці крові низька або не визначається, слід ретельно контролювати рівень електролітів у сироватці крові. Як альтернативу можна розглянути призначення низьких доз мінералокортикоїдів (дезоксикортикостерону півалат у початковій дозі 1,5 мг/кг п/ш кожні 25–28 днів) (23). Хоча це, принаймні теоретично, може послабити механізми, що компенсують (вимірюваний) дефіцит мінералокортикоїдів, довготривала замісна терапія мінералокортикоїдами також вимагає ретельного моніторингу пацієнта (електроліти в сироватці крові, системний артеріальний тиск) і може нести ризик розвитку потенційних побічних ефектів [24]. Собаки з діагнозом атипового гіпоадренокортицизму з нормальною базовою та/або стимульованою АКТГ концентрацією альдостерону в сироватці крові потребують лише замісної терапії глюкокортикоїдами, але в таких собак слід регулярно контролювати рівень електролітів у сироватці крові.
Моніторинг лікування
Небажані реакції на глюкокортикоїди (наприклад, полідипсія / поліурія, поліфагія, збільшення ваги, втрата м’язової маси, задишка, зміни шкіри й шерсті, зміни поведінки) усе ще можуть виникати за дуже низьких доз преднізону / преднізолону й вимагають зниження дози приблизно на 10–15% (блок 7). Питання про те, чи може гідрокортизон бути гарною альтернативою глюкокортикоїдним добавкам для деяких собак, потребує подальшого дослідження. Млявість, слабкість, гіпорексія або анорексія, блювота й діарея можуть свідчити про неоптимальну глюкокортикоїдну замісну терапію у собак із гіпоадренокортицизмом і потребують збільшення дози приблизно на 50% [1],[2],[3].
Собак з атиповим гіпоадренокортицизмом, які отримують замісну терапію мінералокортикоїдами, слід спочатку перевіряти кожні 2–4 тижні (зазвичай через 1014 днів і знову через 25–28 днів після початку прийому дезоксикортикостерону півалату) [23]. Якщо концентрація електролітів (натрію й калію) у сироватці крові перебуває в межах цільових діапазонів, системний артеріальний тиск у нормі, а дозу дезоксикортикостерону останнім часом не коригували, моніторинг лікування рекомендовано продовжувати кожні 1–3 місяці (залежно від того, чи може власник робити ін’єкції мінералокортикоїдів вдома), а для собак, які перебувають під належним контролем, — кожні 3–6 місяців (за винятком випадків, коли щомісячну ін’єкцію дезоксикортикостерону доводиться проводити у ветеринарній клініці). Виявлення гіпокаліємії, гіпернатріємії або системної гіпертензії (систолічний артеріальний тиск >140 мм рт.ст.) вимагає зменшення дози дезоксикортикостерону півалату приблизно на 10–20% або принаймні тимчасової його відміни [23]. Собаки з гіпоадренокортицизмом потребують ретельної оцінки будь-яких потенційних побічних ефектів лікування. Поліурія й полідипсія, які зазвичай інтерпретують як побічний ефект від надлишку преднізо(ло)ну, можуть також свідчити про передозування мінералокортикоїдів (наприклад, дезоксикортикостерону) [1], [23].
Собаки з атиповим гіпоадренокортицизмом зазвичай клінічно стабільні, і їх можна лікувати амбулаторно. Однак ознаки зневоднення під час медичного огляду вимагають принаймні короткотривалого стаціонарного лікування із замісною інфузійною терапією
Прогноз для випадків гіпоадренокортицизму
За умови належної глюкокортикоїдної та (якщо показано або вибрано) мінералокортикоїдної терапії й регулярного спостереження за пацієнтом довгостроковий прогноз атипового гіпоадренокортицизму зазвичай є дуже добрим (рис. 5) [1], [2], [25]. Моніторинг прогресування до типового гіпоадренокортицизму (тобто розвитку гіперкаліємії та/або гіпонатріємії) є важливим аспектом у довгостроковому лікуванні собак з атиповим гіпоадренокортицизмом, які отримують монотерапію глюкокортикоїдами [2], [21]. У таких випадках авторка рекомендує повторно перевіряти рівень електролітів у сироватці крові кожні 3–6 місяців, але настанови щодо частоти моніторингу або початку введення мінералокортикоїдів у собак із дефіцитом альдостерону без будь-яких змін електролітів наразі відсутні.

Висновок
Власники часто ретроспективно розпізнають повільний початок гіпоадренокортицизму та пов’язані з ним ледь помітні клінічні зміни, коли в їхнього улюбленця спостерігається швидке покращення й підвищення якості життя у відповідь на лікування. Захворювання вимагає пожиттєвої терапії та контролю, і це часто сприймається як зміцнення зв’язку між твариною і людиною, але деякі власники побоюються розвитку аддісонового кризу й не бажають залишати собаку без нагляду. Однак більшість власників почуваються дуже комфортно, лікуючи в домашніх умовах собаку, який має будь-яку форму спонтанного гіпоадренокортицизму, а також знають або незабаром дізнаються, за чим слід спостерігати, щоб виявити зміни в якості життя, які потребують подальшої ветеринарної допомоги.
Ромі М. Гайльманн
Професор, доктор ветеринарної медицини, доктор філософії (PhD), дипломант Американського коледжу ветеринарної внутрішньої медицини (внутрішня медицина дрібних тварин), дипломант Європейської колегії з внутрішніх хвороб дрібних тварин (ECVIM-CA), член колегії ветеринарних вчених Австралії та Нової Зеландії («Медицина дрібних тварин»), Кафедра дрібних тварин, Ветеринарна навчальна лікарня, Коледж ветеринарної медицини, Лейпцизький університет, НімеччинаНімеччина
Професор Ромі Гайльманн — сертифікований лікар-терапевт дрібних тварин, дипломант Американського коледжу ветеринарної внутрішньої медицини (ACVIM) та Європейської колегії з внутрішніх хвороб дрібних тварин (ECVIM-CA). Її професійні інтереси охоплюють гастроентерологію, гепатологію, клінічну імунологію, інтервенційну радіологію та ендоскопію. Після закінчення університету у 2005 році вона працювала у клініці дрібних тварин у Німеччині, а згодом повернулася до академічної діяльності, щоб здобути науковий ступінь доктора філософії. Пізніше пройшла ротаційне стажування у Швейцарії, після чого вступила до Техаського університету A&M на комбіновану програму з внутрішньої медицини дрібних тварин (ACVIM-SAIM) та PhD. У 2015 році повернулася до Європи, де обійняла посаду головного лікаря-терапевта у швейцарському спеціалізованому ветеринарному та реферальному центрі. З 2016 року обіймає посаду професора і керівника служби внутрішньої медицини дрібних тварин у Лейпцизькому університеті (Німеччина). Її наукові дослідження спрямовані на розробку нових підходів до діагностики та лікування хронічних гастроентеропатій у собак і котів, а також інших первинних запальних захворювань
Джерела
- Kalenyak K, Heilmann RM. Canine hypoadrenocorticism an update on pathogenesis, diagnosis and treatment. Tierarztl Prax. Ausg. K. Kleintiere Heimtiere 2018;46(3):163-175.
- Thompson AL, Scott-Moncrieff JC, Anderson JD. Comparison of classic hypoadrenocorticism with glucocorticoid-deficient hypoadrenocorticism in dogs: 46 cases (1985-2005). J. Am. Vet. Med. Assoc. 2007;230:1190-1194.
- Schofield I, Woolhead V, Johnson A, et al. Hypoadrenocorticism in dogs under UK primary veterinary care: frequency, clinical approaches and risk factors. J. Small Anim. Pract. 2021;62(5):343-350.
- Gershony LC, Belanger JM, Hytönen MK, et al. Genetic characterization of Addison’s disease in Bearded Collies. BMC Genomics 2020;21(1):833.
- Treeful AE, Rendahl AK, Friedenberg SG. DLA class II haplotypes show sex-specific associations with primary hypoadrenocorticism in Standard Poodle dogs. Immunogenetics 2019;71(5-6):373-382.
- Boag AM, Short A, Kennedy LJ, et al. Polymorphisms in the CTLA4 promotor sequence are associated with canine hypoadrenocorticism. Canine Med. Genet. 2020;7:2.
- Boag AM, Christie MR, McLaughlin KA, et al. Autoantibodies against cytochrome P450 side-chain cleavage enzyme in dogs (Canis lupus familiaris) affected with hypoadrenocorticism (Addison’s disease). PLoS One 2015;10(11):e0143458.
- Labelle P, DeCock HEV. Metastatic tumors to the adrenal glands in domestic animals. Vet. Pathol. 2005;42:52-58.s
- Buckley ME, Chapman PS, Walsh A. Glucocorticoid-deficient hypoadrenocorticism secondary to intravascular lymphoma in the adrenal glands of a dog. Aust. Vet. J. 2017;95(3):64-67.
- Lee N, Choi J, Yoon J. Presumptive nontraumatic adrenal hemorrhage preceding hypoadrenocorticism in a dog. J. Vet. Intern. Med. 2022;DOI: 10.1111/jvim.16531.
- Polledo L, Oliveira M, Adamany J, et al. Hypophysitis, panhypopituitarism, and hypothalamitis in a Scottish Terrier dog. J. Vet. Intern. Med. 2017;31(5):1527-1532.
- Gunasekaran T, Sanders RA. Ventricular systolic dysfunction in dogs diagnosed with hypoadrenocorticism. J. Vet. Cardiol. 2022;41:231-235.
- Hauck C, Schmitz SS, Burgener IA, et al. Prevalence and characterization of hypoadrenocorticism in dogs with signs of chronic gastrointestinal disease: a multicenter study. J. Vet. Intern. Med. 2020;34(4):1399-1405.
- Gallego AF, Gow AG, Boag AM. Evaluation of resting cortisol concentration testing in dogs with chronic gastrointestinal signs. J. Vet. Intern. Med. 2022;36(2):525-531.
- Zeugswetter FK, Schwendenwein I. Diagnostic efficacy of the leukogram and the chemiluminometric ACTH measurement to diagnose canine hypoadrenocorticism. Tierarztl. Prax. Ausg. K. Kleintiere Heimtiere 2014;42(2):223-230.
- Reagan KL, Reagan BA, Gilor C. Machine learning algorithm as a diagnostic tool for hypoadrenocorticism in dogs. Domest. Anim. Endocrinol. 2020;72:106396.
- Lennon EM, Boyle TE, Hutchins RG, et al. Use of basal serum or plasma cortisol concentrations to rule out a diagnosis of hypoadrenocorticism in dogs: 123 cases (2000-2005). J. Am. Vet. Med. Assoc. 2007;231(3):413-416.
- Bovens C, Tennant K, Reeve J, et al. Basal serum cortisol concentration as a screening test for hypoadrenocorticism in dogs. J. Vet. Intern. Med. 2014;28(5):1541-1545.
- Botsford A, Behrend EN, Kemppainen RJ, et al. Low-dose ACTH stimulation testing in dogs suspected of hypoadrenocorticism. J. Vet. Intern. Med. 2018;32(6):1886-1890.
- Moya MV, Refsal KR, Langlois DK. Investigation of the urine cortisol to creatinine ratio for the diagnosis of hypoadrenocorticism in dogs. J. Am. Vet. Med. Assoc. 2022;260(9):1041-1047.
- Baumstark ME, Sieber-Ruckstuhl NS, Müller C, et al. Evaluation of aldosterone concentrations in dogs with hypoadrenocorticism. J. Vet. Intern. Med. 2014;28(1):154-159.
- Reusch CE, Fracassi F, Sieber-Ruckstuhl NS, et al. Altered serum thyrotropin concentrations in dogs with primary hypoadrenocorticism before and during treatment. J. Vet. Intern. Med. 2017;31(6):1643-1648.
- Sieber-Ruckstuhl NS, Reusch CE, Hofer-Inteeworn N, et al. Evaluation of a low-dose desoxycorticosterone pivalate treatment protocol for long-term management of dogs with primary hypoadrenocorticism. J. Vet. Intern. Med. 2019;33(3):1266-1271.
- Casado Diaz JI, Sieber-Ruckstuhl NS, Boretti FS, et al. Evaluation of symmetric dimethylarginine and creatinine in dogs with primary hypoadrenocorticism receiving long-term mineralocorticoid replacement therapy. Vet. Rec. 2022;190(1):e242.
- Hupfeld J, Dölle M, Volk H, et al. Effect of long-term management of hypoadrenocorticism on the quality of life of affected dogs and their owners. Vet. Rec. 2022;8:e1977.
Інші статті в цьому випуску
Поділіться в соціальних мережах